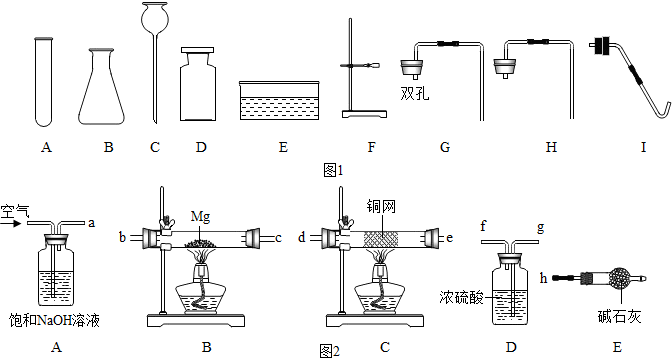
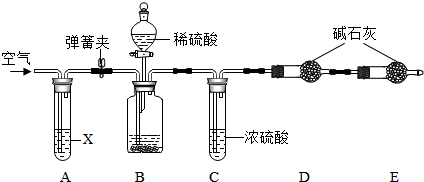
11.用分子的观点对下列现象的解释,错误的是( )
| A. | 湿衣服晾干--分子不断运动 | |
| B. | 水受热变为水蒸气--分子间间隙变大 | |
| C. | 食物腐败--分子本身发生变化 | |
| D. | 热胀冷缩--分子大小随温度改变而改变 |
10.如图所示实验操作错误的是( )
| A. |  | B. | 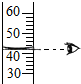 | C. | 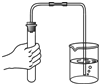 | D. |  |
9.科学探究是奇妙的过程,请你一起参与实验探究,并填写下列空白.
(1)[提出问题]小森同学在滴加FeCl3溶液时,不小心把滴加FeCl3溶液的滴管放入到盛“双氧水”(过氧化氢)的试剂瓶中,发现有大量的气泡产生.小森联想到二氧化锰可作过氧化氢分解的催化剂,FeCl3溶液是否也可以作过氧化氢分解的催化剂呢?于是他做了以下探究.
(2)[猜想与假设]FeCl3溶液能作过氧化氢分解的催化剂.
(3)[设计与实验]
(4)[讨论与反思]
已知FeCl3溶液中含有H2O、Fe3+和Cl -三种粒子,小森同学又做了三种猜想:
猜想1:真正催化H2O2分解的是FeCl3溶液中的H2O;
猜想2:真正催化H2O2分解的是FeCl3溶液中的Fe3+;
猜想3:真正催化H2O2分解的是FeCl3溶液中的Cl -;
你认为最不可能的是哪一种猜想?猜想1,理由是过氧化氢溶液中有水.
小森同学又对余下的猜想进行了实验探究,请你帮助他填写下表:
你认为小森同学的哪一种猜想正确?猜想2,理由是盐酸溶液中有水分子和氯离子,实验中无明显现象.
(1)[提出问题]小森同学在滴加FeCl3溶液时,不小心把滴加FeCl3溶液的滴管放入到盛“双氧水”(过氧化氢)的试剂瓶中,发现有大量的气泡产生.小森联想到二氧化锰可作过氧化氢分解的催化剂,FeCl3溶液是否也可以作过氧化氢分解的催化剂呢?于是他做了以下探究.
(2)[猜想与假设]FeCl3溶液能作过氧化氢分解的催化剂.
(3)[设计与实验]
| 实验步骤 | 实验现象 | 实验结论 |
| 在一支试管中加入5mL15%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管. | FeCl3溶液可以作H2O2分解的催化剂 |
已知FeCl3溶液中含有H2O、Fe3+和Cl -三种粒子,小森同学又做了三种猜想:
猜想1:真正催化H2O2分解的是FeCl3溶液中的H2O;
猜想2:真正催化H2O2分解的是FeCl3溶液中的Fe3+;
猜想3:真正催化H2O2分解的是FeCl3溶液中的Cl -;
你认为最不可能的是哪一种猜想?猜想1,理由是过氧化氢溶液中有水.
小森同学又对余下的猜想进行了实验探究,请你帮助他填写下表:
| 实验步骤 | 实验现象 | 实验结论 |
| 向盛有5mL15%的H2O2溶液的试管中加入少量的盐酸,然后把带火星的木条伸入试管中. | 无明显现象 |
3.某化学兴趣小组的学生,发现金属R不在初中学到的金属活动性顺序表中,该小组为了了解R与常见金属铝、铜的金属活动性顺序,进行如下探究活动:
【作出猜想】他们考虑到铝的活动性比铜强,对三种金属的活动性顺序作出如下猜想:
猜想一:Al>Cu>R,猜想二:Al>R>Cu,猜想三:R>Al>Cu,
【查阅资料】R是一种银白色的金属,在R的盐溶液中只有+2价,R的盐溶液呈蓝色,常温下铝的表面会形成一层致密的氧化膜;硫酸铝、氯化铝、硝酸铝的溶液均为无色.
【实验探究】为了探究哪一种猜想成立,甲、乙、丙三位同学分别针对猜想一、猜想二、猜想三设计实验方案并展开实验探究.
【交流反思】
究竟哪种猜想成立?三位同学经讨论交流,发现丙同学在实验前没有打磨铝丝,这可能会导致实验结论错误.于是他们先打磨铝丝,再将其插入到丙同学做实验用过的溶液中,一段时间后,溶液的颜色变浅或颜色逐渐褪去;进而确认猜想三不成立,猜想二成立.
探究结束后,他们总结得出:通过金属与酸溶液反应或金属与盐溶液反应可以比较金属活动性强弱.
0 146181 146189 146195 146199 146205 146207 146211 146217 146219 146225 146231 146235 146237 146241 146247 146249 146255 146259 146261 146265 146267 146271 146273 146275 146276 146277 146279 146280 146281 146283 146285 146289 146291 146295 146297 146301 146307 146309 146315 146319 146321 146325 146331 146337 146339 146345 146349 146351 146357 146361 146367 146375 211419
【作出猜想】他们考虑到铝的活动性比铜强,对三种金属的活动性顺序作出如下猜想:
猜想一:Al>Cu>R,猜想二:Al>R>Cu,猜想三:R>Al>Cu,
【查阅资料】R是一种银白色的金属,在R的盐溶液中只有+2价,R的盐溶液呈蓝色,常温下铝的表面会形成一层致密的氧化膜;硫酸铝、氯化铝、硝酸铝的溶液均为无色.
【实验探究】为了探究哪一种猜想成立,甲、乙、丙三位同学分别针对猜想一、猜想二、猜想三设计实验方案并展开实验探究.
| 猜想 | 主要操作 | 主要现象 | 实验结论 |
| 猜想一 | 打磨R丝,并将其插入到硫酸铜溶液中 | R丝表面覆盖了一层红色的物质 | 猜想一不成立(填“成立”或“不成立”) |
| 猜想二 | 打磨粗细相同的R丝、铝丝、铜丝,分别将它们插入到体积相同、溶质质量分数也相同的稀硫酸中 | ①R丝表面产生气泡缓慢,溶液由无色逐渐变成蓝色 ②铝丝表面产生气泡较快 ③铜丝表面没有气泡产生 | 猜想二成立. R与稀硫酸反应的化学方程式为 R+H2SO4=RSO4+H2↑ |
| 猜想三 | 将铝丝插入到RSO4溶液中 | 无明显现象 | 猜想三成立 |
究竟哪种猜想成立?三位同学经讨论交流,发现丙同学在实验前没有打磨铝丝,这可能会导致实验结论错误.于是他们先打磨铝丝,再将其插入到丙同学做实验用过的溶液中,一段时间后,溶液的颜色变浅或颜色逐渐褪去;进而确认猜想三不成立,猜想二成立.
探究结束后,他们总结得出:通过金属与酸溶液反应或金属与盐溶液反应可以比较金属活动性强弱.
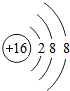 表示的粒子S2-.
表示的粒子S2-.