16.下列元素符号中书写正确的是( )
| A. | MG | B. | CA | C. | Fe | D. | f |
15.下列选项不属于模型的是( )
| A. |  警告标志 警告标志 | B. |  足球烯 足球烯 | C. |  地球仪 地球仪 | D. |  玩具机器人 玩具机器人 |
13. 归纳总结是学习化学的重要方法.请回答下列问题:
归纳总结是学习化学的重要方法.请回答下列问题:
(1)“一碳化学”是以一个分子中只含有一个碳原子的化合物为原料合成一系列化工原料和燃料的化学.
①甲烷的化学式是CH4;
②炼铁时用一氧化碳还原氧化铁的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
③在催化剂初中的条件下,用CO和H2合成甲醇(CH4O),写出反应的化学方程式CO+2H2$\frac{\underline{\;催化剂\;}}{\;}$CH4O;
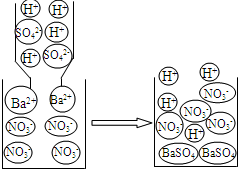
(2)酸碱盐之间能相互反应,碱与盐之间若有气体生成,反应就能发生,请写出该气体的化学式NH3.酸与盐之间能发生反应,分析如图,写出反应的化学方程式Ba(NO3)2+H2SO4=BaSO4↓+2HNO3.
(4)金属活动顺序有重要的应用.
①将一段锌片插入到CuSO4溶液中,观察到明显的现象,反应的化学方程式Zn+CuSO4═ZnSO4+Cu.
②金属分别与水、水蒸气的反应的情况如下表:
根据金属活动性顺序和表中的信息,推断“镁与水蒸气”的反应合理的是CD(填写代号);
A.不反应 B.缓慢反应 C.比镁与冷水反应快 D.比铁与水蒸气反应快
③已知在加热的条件下铁与水蒸气反应生成四氧化三铁和氢气,该反应的化学方程式为:
3Fe+4H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2↑.
 归纳总结是学习化学的重要方法.请回答下列问题:
归纳总结是学习化学的重要方法.请回答下列问题:(1)“一碳化学”是以一个分子中只含有一个碳原子的化合物为原料合成一系列化工原料和燃料的化学.
①甲烷的化学式是CH4;
②炼铁时用一氧化碳还原氧化铁的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
③在催化剂初中的条件下,用CO和H2合成甲醇(CH4O),写出反应的化学方程式CO+2H2$\frac{\underline{\;催化剂\;}}{\;}$CH4O;
(2)酸碱盐之间能相互反应,碱与盐之间若有气体生成,反应就能发生,请写出该气体的化学式NH3.酸与盐之间能发生反应,分析如图,写出反应的化学方程式Ba(NO3)2+H2SO4=BaSO4↓+2HNO3.
(4)金属活动顺序有重要的应用.
①将一段锌片插入到CuSO4溶液中,观察到明显的现象,反应的化学方程式Zn+CuSO4═ZnSO4+Cu.
②金属分别与水、水蒸气的反应的情况如下表:
| 物质 | 镁与冷水 | 铁与冷水 | 铁与水蒸气 | 铜与冷水 | 铜与水蒸气 |
| 反应情况 | 缓慢反应 | 不反应 | 能反应 | 反应 | 不反应 |
A.不反应 B.缓慢反应 C.比镁与冷水反应快 D.比铁与水蒸气反应快
③已知在加热的条件下铁与水蒸气反应生成四氧化三铁和氢气,该反应的化学方程式为:
3Fe+4H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2↑.
11. 某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的溶液,他们对此产生了兴趣.
某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的溶液,他们对此产生了兴趣.
【提出问题】这瓶溶液究竟是什么?
经过询问实验老师平时的药品保管得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的某一种.为了确定该药品,他们首先进行了理论分析:
(1)小明根据标签上的组成元素认为一定不可能是NaCl.(填化学式)
(2)小英提出,碳酸氢钠、NaNO3 (填化学式)也不可能,他们设计了如下实验.
【设计实验】
【实验结论】
(3)该瓶无色溶液是碳酸钠(填化学式).生成白色沉淀过程的化学方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl;产生大量气泡的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑.
【实验反思】
(4)小强认为上述设计实验还可简化,仍能达到目的.小强的实验操作是取上述无色溶液少许于试管中,滴加少量的稀盐酸,如果产生大量气泡,则是碳酸钠溶液;如果没有明显现象则是硫酸钠溶液.
 某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的溶液,他们对此产生了兴趣.
某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的溶液,他们对此产生了兴趣.【提出问题】这瓶溶液究竟是什么?
经过询问实验老师平时的药品保管得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的某一种.为了确定该药品,他们首先进行了理论分析:
(1)小明根据标签上的组成元素认为一定不可能是NaCl.(填化学式)
(2)小英提出,碳酸氢钠、NaNO3 (填化学式)也不可能,他们设计了如下实验.
【设计实验】
| 实验操作 | 实验现象 |
| 取少量样品于试管中,慢慢滴加BaCl2溶液,静置一段时间,倾去上层清液,向沉淀中继续滴加稀盐酸 | 先出现沉淀,后产生大量气泡 |
(3)该瓶无色溶液是碳酸钠(填化学式).生成白色沉淀过程的化学方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl;产生大量气泡的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑.
【实验反思】
(4)小强认为上述设计实验还可简化,仍能达到目的.小强的实验操作是取上述无色溶液少许于试管中,滴加少量的稀盐酸,如果产生大量气泡,则是碳酸钠溶液;如果没有明显现象则是硫酸钠溶液.
8.下列变化属于化学变化的是( )
| A. | 海水晒盐 | B. | 干冰冷藏食品 | C. | “可燃冰”燃烧 | D. | 用洗洁剂除油污 |
7.同学们对制作糕点常用膨松剂Na2CO3或NaHCO3进行了下列探究.
【查阅资料】
表1
表2
【探究一】NaHCO3和Na2CO3性质差异的探究
(1)现有20℃时溶质质量分数为8%的Na2CO3和NaHCO3溶液酸碱性:取样于试管中,分别滴加紫色石蕊试液,均显蓝色;酸碱度:NaHCO3溶液<Na2CO3溶液(填“>”或”“<”).
(2)稳定性:按图1,实验中可观察乙烧杯中的石灰水变浑浊,对应试管中发生反应的化学方程式为:
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
结论:在受热条件下,碳酸钠比碳酸氢钠稳定性强(填“强”或“弱”).
(3)利用溶解度鉴别NaHCO3和Na2CO3:分别取Xg两种固体粉末加入20℃,10g水中充分溶解,通过观察溶解现象来区分,X可以是下列的A.(选填A、B或C)
A.2g B.0.96g C.0.5g
【问题讨论】
(4)实验结束时,应先B(选填A或B).
A.熄灭酒精灯 B.将甲、乙烧杯移开
(5)甲认为探究稳定性实验中,由于受热时两物质温度不同,不能得到(2)中的结论,经对装置设计讨论后一致认为可以得到上述结论,理由是碳酸氢钠的受热温度低于碳酸钠的受热温度.
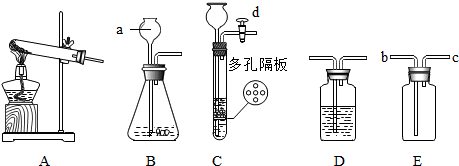
【探究二】测定NaHCO3和Na2CO3混合物10.0g中NaHCO3的质量分数(图2,夹持装置略)
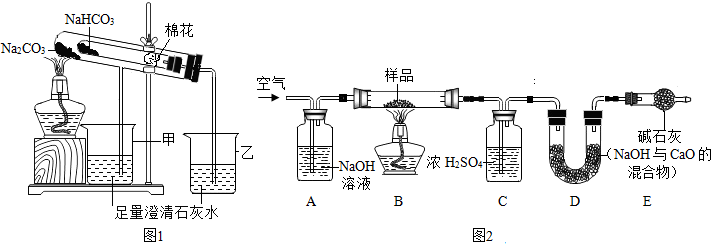
【问题讨论】
(6)实验前先通一段时间的空气的目的是把装置中的二氧化碳排尽;
(7)A的作用是吸收空气中的二氧化碳,若没有装置E,NaHCO3的质量分数测定结果会偏大(填“偏大”、“不变”或“偏小”).
(8)停止加热后,仍继续通入空气一段时间,目的是把反应生成的二氧化碳完全排入D中.
【含量测定】
(9)测得装置D的质量实验前为122.2g,实验后为124.4g,计算该样品中NaHCO3的质量分数.(要有计算过程)
【知识拓展】
(10)向Na2CO3溶液中通入CO2气体可以生成NaHCO3,该反应的化学反应方程式为:Na2CO3+CO2+H2O=2NaHCO3.
0 146105 146113 146119 146123 146129 146131 146135 146141 146143 146149 146155 146159 146161 146165 146171 146173 146179 146183 146185 146189 146191 146195 146197 146199 146200 146201 146203 146204 146205 146207 146209 146213 146215 146219 146221 146225 146231 146233 146239 146243 146245 146249 146255 146261 146263 146269 146273 146275 146281 146285 146291 146299 211419
【查阅资料】
表1
| 20℃ | 8%Na2CO3溶液 | 8%NaHCO3溶液 |
| pH | 10.6 | 8.0 |
| 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
(1)现有20℃时溶质质量分数为8%的Na2CO3和NaHCO3溶液酸碱性:取样于试管中,分别滴加紫色石蕊试液,均显蓝色;酸碱度:NaHCO3溶液<Na2CO3溶液(填“>”或”“<”).
(2)稳定性:按图1,实验中可观察乙烧杯中的石灰水变浑浊,对应试管中发生反应的化学方程式为:
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
结论:在受热条件下,碳酸钠比碳酸氢钠稳定性强(填“强”或“弱”).
(3)利用溶解度鉴别NaHCO3和Na2CO3:分别取Xg两种固体粉末加入20℃,10g水中充分溶解,通过观察溶解现象来区分,X可以是下列的A.(选填A、B或C)
A.2g B.0.96g C.0.5g
【问题讨论】
(4)实验结束时,应先B(选填A或B).
A.熄灭酒精灯 B.将甲、乙烧杯移开
(5)甲认为探究稳定性实验中,由于受热时两物质温度不同,不能得到(2)中的结论,经对装置设计讨论后一致认为可以得到上述结论,理由是碳酸氢钠的受热温度低于碳酸钠的受热温度.
【探究二】测定NaHCO3和Na2CO3混合物10.0g中NaHCO3的质量分数(图2,夹持装置略)

【问题讨论】
(6)实验前先通一段时间的空气的目的是把装置中的二氧化碳排尽;
(7)A的作用是吸收空气中的二氧化碳,若没有装置E,NaHCO3的质量分数测定结果会偏大(填“偏大”、“不变”或“偏小”).
(8)停止加热后,仍继续通入空气一段时间,目的是把反应生成的二氧化碳完全排入D中.
【含量测定】
(9)测得装置D的质量实验前为122.2g,实验后为124.4g,计算该样品中NaHCO3的质量分数.(要有计算过程)
【知识拓展】
(10)向Na2CO3溶液中通入CO2气体可以生成NaHCO3,该反应的化学反应方程式为:Na2CO3+CO2+H2O=2NaHCO3.