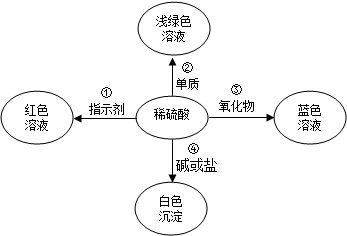
8.能证明20℃时某一硝酸钾溶液已达到饱和的方法是( )
| A. | 在20℃时,向该溶液中加入少量水,溶液变稀 | |
| B. | 取少量溶液降温至10℃有固体析出 | |
| C. | 在20℃时,向该溶液中加入少量硝酸钾晶体 | |
| D. | 取少量溶液加热至50℃无固体析出 |
7.在一定温度下,向盛有氯化钠饱和溶液的烧杯中加入氯化钠固体后,则( )
| A. | 固体质量不变 | B. | 固体质量减少 | ||
| C. | 氯化钠溶解度增大 | D. | 溶质质量分数增大 |
6.如图甲是氢气和氧化铜反应的实验,如图乙是木炭和氧化铁反应的实验.
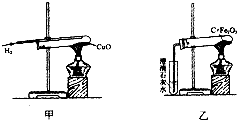
(1)在上述两个实验中,氢气和木炭表现出相同的化学性质是还原性.
(2)某同学正确操作做完乙实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色,取少量黑色粉末,加入足量稀硫酸充分振荡,但她惊讶地发现黑色粉末没有溶解,试管中 也未产生预期的气泡,这说明该反应并没有生成铁.
(3)该同学查阅资料,得到关于铁的氧化物如下信息:
根据以上信息,试写出乙实验试管中反应的化学方程式C+6Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$4Fe3O4+CO2↑.
经分析后,该同学试着提高反应温度后,实验出现了预期的现象.

(1)在上述两个实验中,氢气和木炭表现出相同的化学性质是还原性.
(2)某同学正确操作做完乙实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色,取少量黑色粉末,加入足量稀硫酸充分振荡,但她惊讶地发现黑色粉末没有溶解,试管中 也未产生预期的气泡,这说明该反应并没有生成铁.
(3)该同学查阅资料,得到关于铁的氧化物如下信息:
| 铁的氧化物化学式 | Fe2O3 | Fe3O4 | FeO |
| 颜色 | 红 | 黑 | 黑 |
| 化学性质 | 可溶于酸 | 常温下不溶于稀酸 | 可溶于酸 |
经分析后,该同学试着提高反应温度后,实验出现了预期的现象.
4.某化学兴趣小组回收利用废旧干电池.
实验 1 回收填料中的二氧化锰和氯化铵
查阅资料:废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可于水.兴趣小组的同学们设计回收物质的流程如图1所示.

(1)操作1 和操作2 的名称都是过滤,该操作中玻璃棒的作用是引流.
(2)灼烧滤渣 l 的目的是除去炭粉.
(3)己知滤液 1 中氯化铵和氯化锌的浓度相近.在某温度下蒸发滤液1 时,大量的氯化铵晶体先析出,说明该温度下氯化铵溶解度<氯化锌的溶解度(填“<”、“=”或“>”).
实验 2 利用外壳回收物锌制取氢气及相关探究
(4)用锌和稀硫酸制取氢气.己知氢气密度比空气小且难溶于水,提供装置如图2.
①应选择:发生装置为B(填编号),排空气法收集装置为D(填编号).
②若用排水法收集并测定气体的体积,气体从装置B导管口b(填“a”或“b”) 进;选用仪器 F 测量排出水的体积,仪器 F 名称是量筒.
(5)探究影响锌与稀硫酸反应快慢的因素.反应过程中,用前 10min 内收集的氢气体积比较反应的快慢.控制其他条件相同,进行下表四组实验,获得数据如表.
①比较实验 a 和实验 b,可以得到的结论是与同体积同浓度的稀硫酸反应,含杂质的锌比纯锌反应速率要快.
②为了研究硫酸浓度对反应快慢的影响,需比较实验a和实验c(填编号).
③控制其他条件相同,需控制的条件是锌粒形状大小(例举一种条件即可).
实验 1 回收填料中的二氧化锰和氯化铵
查阅资料:废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可于水.兴趣小组的同学们设计回收物质的流程如图1所示.

(1)操作1 和操作2 的名称都是过滤,该操作中玻璃棒的作用是引流.
(2)灼烧滤渣 l 的目的是除去炭粉.
(3)己知滤液 1 中氯化铵和氯化锌的浓度相近.在某温度下蒸发滤液1 时,大量的氯化铵晶体先析出,说明该温度下氯化铵溶解度<氯化锌的溶解度(填“<”、“=”或“>”).
实验 2 利用外壳回收物锌制取氢气及相关探究
(4)用锌和稀硫酸制取氢气.己知氢气密度比空气小且难溶于水,提供装置如图2.
①应选择:发生装置为B(填编号),排空气法收集装置为D(填编号).
②若用排水法收集并测定气体的体积,气体从装置B导管口b(填“a”或“b”) 进;选用仪器 F 测量排出水的体积,仪器 F 名称是量筒.
(5)探究影响锌与稀硫酸反应快慢的因素.反应过程中,用前 10min 内收集的氢气体积比较反应的快慢.控制其他条件相同,进行下表四组实验,获得数据如表.
| 验实号编 | 试剂 | 前10 min内产生的氢气体积(mL) | |
| 不同纯度的锌 | 不同体积和浓度的稀硫酸 | ||
| a | 纯锌 | 30 mL 30% | 564.3 |
| b | 含杂质的锌 | 30 InL 30% | 634.7 |
| c | 纯锌 | 30 mL 20% | 449.3 |
| d | 纯锌 | 40 mL 30% | 602.8 |
②为了研究硫酸浓度对反应快慢的影响,需比较实验a和实验c(填编号).
③控制其他条件相同,需控制的条件是锌粒形状大小(例举一种条件即可).
1.欲除去下列物质中的少量杂质,所用试剂正确的是( )
0 146077 146085 146091 146095 146101 146103 146107 146113 146115 146121 146127 146131 146133 146137 146143 146145 146151 146155 146157 146161 146163 146167 146169 146171 146172 146173 146175 146176 146177 146179 146181 146185 146187 146191 146193 146197 146203 146205 146211 146215 146217 146221 146227 146233 146235 146241 146245 146247 146253 146257 146263 146271 211419
| 物质 | 杂质 | 试剂 | |
| A | CO2 | HCl气体 | NaOH溶液 |
| B | CuO | C | O2(灼烧) |
| C | 稀盐酸溶液 | CuCl2 | KOH溶液 |
| D | NaNO3溶液 | Na2SO4溶液 | Ba(OH)2溶液 |
| A. | A | B. | B | C. | C | D. | D |