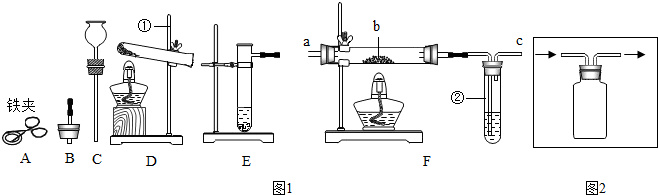
16. 南南同学看到“好想你”红枣袋中装有一袋防腐剂,品名为
南南同学看到“好想你”红枣袋中装有一袋防腐剂,品名为
“504双吸剂”,其标签如图所示.南南和北北对这包久置的“504双吸剂”
固体样品很好奇,设计如下实验进行探究.
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验探究】
南南同学的方案
北北同学认为南南同学的实验并不能得出一定不含Fe2O3的结论,理由是氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色,并设计如下实验方案继续验证.
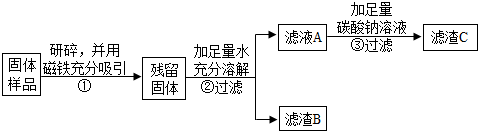
(1)步骤①样品用磁铁吸引前需经过研碎,其中研碎的目的是增大接触面积,使反应充分.
(2)步骤②中固体溶解时放出大量热,由此可以判断固体中一定含有CaO.写出该过程中的化学方程式CaO+H2O=Ca(OH)2.
(3)步骤③中反应的化学方程式是Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
北北同学对滤渣B又进行探究.
【实验结论】综合上述实验及所给数据,该久置固体中一定含有的物质是Fe、Fe2O3、CaO、CaCO3.
 南南同学看到“好想你”红枣袋中装有一袋防腐剂,品名为
南南同学看到“好想你”红枣袋中装有一袋防腐剂,品名为“504双吸剂”,其标签如图所示.南南和北北对这包久置的“504双吸剂”
固体样品很好奇,设计如下实验进行探究.
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验探究】
南南同学的方案
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体放于试管中,滴加足量的稀盐酸 | 固体逐渐消失,有无色气体产生,得到浅绿色溶液 | 固体有一定含有Fe, 一定不含Fe2O3 |

(1)步骤①样品用磁铁吸引前需经过研碎,其中研碎的目的是增大接触面积,使反应充分.
(2)步骤②中固体溶解时放出大量热,由此可以判断固体中一定含有CaO.写出该过程中的化学方程式CaO+H2O=Ca(OH)2.
(3)步骤③中反应的化学方程式是Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
北北同学对滤渣B又进行探究.
| 实验操作 | 实验现象 | 实验结论 |
| ①取滤渣B于试管中,加入适量稀盐酸 ②生成的气体通入澄清石灰水 | ①固体减少,有气泡冒出,溶液变为黄色②该溶液变浑浊. | 固体中一定含有CaCO3 和Fe2O3. |
12.向盛有10ml稀盐酸(其中滴有少量紫色石蕊试液)的烧杯中加入氢氧化钠溶液,用pH计(测pH值的仪器)测定溶液的pH,所得数据如下.请分析并回答下列问题:
(1)当加入氢氧化钠溶液的体积为10mL时,稀盐酸和氢氧化钠溶液恰好完全反应,参加反应的稀盐酸的溶质与其氢氧化钠溶液的溶质的质量之比为36.5:40.
(2)当加入氢氧化钠溶液的体积为13mL时,溶液显蓝色.
| 加入NaOH溶液的体积/ml | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.0 | 7.0 | 11.0 | 12.2 |
(2)当加入氢氧化钠溶液的体积为13mL时,溶液显蓝色.
11.向盛有酚酞和NaOH溶液的烧杯中滴加稀盐酸,直至液体呈无色.为探究反应后溶液中溶质的组成,所选试剂不正确的是( )
| A. | 氢氧化钠溶液 | B. | 锌粒 | C. | 碳酸钠溶液 | D. | 紫色石蕊溶液 |
10.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH═Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,同学们产生了疑问:反应后的溶液中溶质是什么呢?
【假设猜想】针对疑问,大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是猜想四或四.
【实验探究】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,则甲组猜想中的NaOH或氢氧化钠不正确.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,进行如下三个方案的探究.
【得出结论】通过探究,全班同学一致确定猜想二是正确的.
【评价反思】老师指出【实验探究】(2)中存在两处明显错误,只有一个方案和操作都正确,请
大家反思后,写出该方案中反应的化学方程式:Na2CO3+H2SO4═Na2SO4+H2O+CO2↑.
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH═Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,同学们产生了疑问:反应后的溶液中溶质是什么呢?
【假设猜想】针对疑问,大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是猜想四或四.
【实验探究】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,则甲组猜想中的NaOH或氢氧化钠不正确.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,进行如下三个方案的探究.
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaC12溶液 |
| 实验操作 | 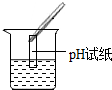 | 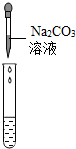 | 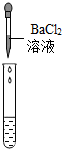 |
| 实验现象 | 试纸变色,对比标准比色卡,pH<7 | 产生无色气泡有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【评价反思】老师指出【实验探究】(2)中存在两处明显错误,只有一个方案和操作都正确,请
大家反思后,写出该方案中反应的化学方程式:Na2CO3+H2SO4═Na2SO4+H2O+CO2↑.
9.某课外兴趣小组的同学绘制四种实验数据的变化趋势图象,其中正确的是( )
| A. |  某温度下,向一定量接近饱和的硝酸钾溶液中不断加入硝酸钾晶体 | |
| B. |  向硫酸铜溶液中加入过量的氢氧化钠溶液 | |
| C. |  向足量且溶质质量分数相等的稀硫酸中分别加入等质量的金属镁和铁 | |
| D. |  现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量碳酸钠溶液 |
8.某一种或几种物质的水溶液中,可能含有以下几种离子:K+、Cl-、Ca2+、Ba2+、SO42-、CO32-.现取两份100mL溶液进行如下实验:(1)第一份加入AgNO3溶液有沉淀产生.(2)第二份加足量的Ba(NO3)2溶液,有白色沉淀产生,再加入过量的稀硝酸,沉淀部分溶解.根据上述实验,以下推测正确的是( )
| A. | 一定存在Cl- | B. | 一定存在CO32-,可能存在Ba2+ | ||
| C. | 一定存在K+ | D. | 一定存在SO42-可能存在Ca2+ |
7.下列说法中,正确的是( )
0 146013 146021 146027 146031 146037 146039 146043 146049 146051 146057 146063 146067 146069 146073 146079 146081 146087 146091 146093 146097 146099 146103 146105 146107 146108 146109 146111 146112 146113 146115 146117 146121 146123 146127 146129 146133 146139 146141 146147 146151 146153 146157 146163 146169 146171 146177 146181 146183 146189 146193 146199 146207 211419
| A. | 向某一固体中滴加稀盐酸,产生气泡,则该固体中一定含有CO32-或HCO3- | |
| B. | 塑料、合成橡胶、合金、玻璃钢属于复合材料 | |
| C. | 区别NH4Cl和KCl粉末,可用分别加熟石灰研磨并闻气味的方法 | |
| D. | 向某溶液中滴入BaCl2溶液,有白色沉淀生成,该溶液中一定有SO42- |