16. 向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌,发现开始没产生气泡,盐酸加到一定程度才产生气泡.随着盐酸的加入,溶液中离子数目也相应地发生变化.(提示:先后发生的反应为:
向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌,发现开始没产生气泡,盐酸加到一定程度才产生气泡.随着盐酸的加入,溶液中离子数目也相应地发生变化.(提示:先后发生的反应为:
①K2CO3+HCl═KHCO3+KCl,②KHCO3+HCl═KCl+H2O+CO2↑).
如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是
( )
 向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌,发现开始没产生气泡,盐酸加到一定程度才产生气泡.随着盐酸的加入,溶液中离子数目也相应地发生变化.(提示:先后发生的反应为:
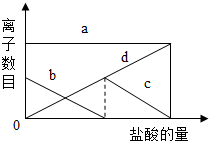
向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌,发现开始没产生气泡,盐酸加到一定程度才产生气泡.随着盐酸的加入,溶液中离子数目也相应地发生变化.(提示:先后发生的反应为:①K2CO3+HCl═KHCO3+KCl,②KHCO3+HCl═KCl+H2O+CO2↑).
如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是
( )
| A. | a:K+; b:CO32-; c:HCO3-; d:Cl- | |
| B. | a:K+; b:CO32-; c:Cl-; d:HCO3- | |
| C. | a:Cl-; b:K+; c:CO32-; d:HCO3- | |
| D. | a:K+; b:HCO3-; c:Cl-; d:CO32- |
12.(1)根据如图回答问题:

①仪器a的名称是集气瓶.
②实验室用过氧化氢制取氧气的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,选用的收集装置是C(填字母序号,下同).如图E所似乎实验中,热水的作用是使温度达到白磷的着火点,使水中的白磷与氧气隔绝;
③实验室用大理石和稀盐酸制取二氧化碳选用的发生装置是B.如图F所示,将二氧化碳倒入烧杯中,观察到棉芯自下而上熄灭,说明二氧化碳具有的性质是密度比空气大,不能燃烧,不支持燃烧.
(2)某同学在电视寻宝节目中,看到一些铜制文物上有绿色的锈迹,并对绿色锈迹产生了探究兴趣.
【查阅资料】
①绿色锈迹是碱式碳酸铜[Cu2(OH)2CO3],受热易分解.
②无水硫酸铜为白色粉末,遇水变蓝.
③碱石灰是CaO和NaOH的固体混合物,NaOH与CO2反应生成碳酸钠固体和水.
④氧化铜与稀硫酸反应生成蓝色溶液,碳粉不与稀硫酸反应也不溶解在稀硫酸中.
【发现问题】
查阅资料后,该同学将少量碱式碳酸铜放入试管中加热,发现试管中的固体由绿色变成黑色,同时试管壁上有无色液滴生成.
为了进一步确定碱式碳酸铜受热分解的产物,进行了如下探究:
探究一:碱式碳酸铜受热分解生成的黑色固体的成分.
【猜想与假设】该黑色固体可能是①碳粉;②氧化铜;③碳和氧化铜的混合物.
【设计方案】请帮助该同学完成下述实验报告.
探究二:碱式碳酸铜受热分解还会生成CO2和H2O.
【进行实验】选择如图2所示装置进行验证.
步骤一:连接A和B,打开活塞,通入一段时间的空气.
步骤二,关闭活塞,依次连接装置A→B→D→C(填“C”、“D”).
步骤三:点燃酒精灯,观察到明显现象后,停止加热.
【解释与结论】
①当观察到D中无水硫酸铜变成蓝色,C中澄清石灰水变浑浊,说明碱式碳酸铜受热分解生成了CO2和H2O,写出C中反应的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O.
②Cu2(OH)2CO3受热分解的化学方程式Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑.
【反思与评价】
上述装置中A的作用是除去空气中的水蒸气和二氧化碳.

①仪器a的名称是集气瓶.
②实验室用过氧化氢制取氧气的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,选用的收集装置是C(填字母序号,下同).如图E所似乎实验中,热水的作用是使温度达到白磷的着火点,使水中的白磷与氧气隔绝;
③实验室用大理石和稀盐酸制取二氧化碳选用的发生装置是B.如图F所示,将二氧化碳倒入烧杯中,观察到棉芯自下而上熄灭,说明二氧化碳具有的性质是密度比空气大,不能燃烧,不支持燃烧.
(2)某同学在电视寻宝节目中,看到一些铜制文物上有绿色的锈迹,并对绿色锈迹产生了探究兴趣.
【查阅资料】
①绿色锈迹是碱式碳酸铜[Cu2(OH)2CO3],受热易分解.
②无水硫酸铜为白色粉末,遇水变蓝.
③碱石灰是CaO和NaOH的固体混合物,NaOH与CO2反应生成碳酸钠固体和水.
④氧化铜与稀硫酸反应生成蓝色溶液,碳粉不与稀硫酸反应也不溶解在稀硫酸中.
【发现问题】
查阅资料后,该同学将少量碱式碳酸铜放入试管中加热,发现试管中的固体由绿色变成黑色,同时试管壁上有无色液滴生成.
为了进一步确定碱式碳酸铜受热分解的产物,进行了如下探究:
探究一:碱式碳酸铜受热分解生成的黑色固体的成分.
【猜想与假设】该黑色固体可能是①碳粉;②氧化铜;③碳和氧化铜的混合物.
【设计方案】请帮助该同学完成下述实验报告.
| 实验操作与现象 | 实验结论 |
| 实验操作:取黑色固体适量于试管中,加入足量稀硫酸; 实验现象:黑色固体全部溶解,形成蓝色溶液 | 猜想②正确 |
【进行实验】选择如图2所示装置进行验证.
步骤一:连接A和B,打开活塞,通入一段时间的空气.
步骤二,关闭活塞,依次连接装置A→B→D→C(填“C”、“D”).
步骤三:点燃酒精灯,观察到明显现象后,停止加热.
【解释与结论】
①当观察到D中无水硫酸铜变成蓝色,C中澄清石灰水变浑浊,说明碱式碳酸铜受热分解生成了CO2和H2O,写出C中反应的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O.
②Cu2(OH)2CO3受热分解的化学方程式Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑.
【反思与评价】
上述装置中A的作用是除去空气中的水蒸气和二氧化碳.
8.下列实验操作能达到预期目的是( )
0 146009 146017 146023 146027 146033 146035 146039 146045 146047 146053 146059 146063 146065 146069 146075 146077 146083 146087 146089 146093 146095 146099 146101 146103 146104 146105 146107 146108 146109 146111 146113 146117 146119 146123 146125 146129 146135 146137 146143 146147 146149 146153 146159 146165 146167 146173 146177 146179 146185 146189 146195 146203 211419
| A. | 用10mL的量筒量取9.0mL水 | |
| B. | 用100mL的量筒量取2.0mL水 | |
| C. | 用托盘天平称取10.58g碳酸钠粉末 | |
| D. | 用150mL酒精和50mL水精确配制200mL医用消毒酒精 |
 现有铜与金属镁、铁、锌中的一种组成的混合物,兴趣小组的同学欲测定其组成.进行以下实验,取该混合物粉末8.0g放入烧杯中,将140.0g 溶质的质量分数为14.0%的稀硫酸平均分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如图.请你通过计算回答:
现有铜与金属镁、铁、锌中的一种组成的混合物,兴趣小组的同学欲测定其组成.进行以下实验,取该混合物粉末8.0g放入烧杯中,将140.0g 溶质的质量分数为14.0%的稀硫酸平均分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如图.请你通过计算回答: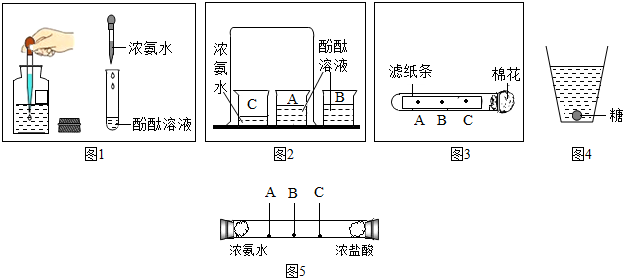
 如图是实验室中过滤操作示意图,回答下列问题:
如图是实验室中过滤操作示意图,回答下列问题: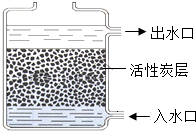 水是生命之源,没有水就没有生命.
水是生命之源,没有水就没有生命.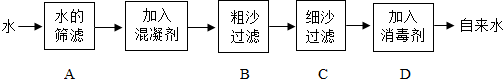
 某班同学做验证铁、铜、银的金属活动性顺序的实验,用到的药品有铁丝、铜丝、银丝、稀硫酸和硫酸铜溶液.实验结束后,化学兴趣小组的同学欲对该实验的废液进行探究,请你一起参与.
某班同学做验证铁、铜、银的金属活动性顺序的实验,用到的药品有铁丝、铜丝、银丝、稀硫酸和硫酸铜溶液.实验结束后,化学兴趣小组的同学欲对该实验的废液进行探究,请你一起参与.