12.取以下食物的汁液,测得它们的PH范围如下:牛奶6.3-6.6,葡萄汁3.5-4.5,玉米粥6.8-8.0,苹果汁2.9-3.3,其中酸性最强的食物汁液是( )
| A. | 苹果汁 | B. | 牛奶 | C. | 玉米粥 | D. | 葡萄汁 |
10.化学与实验.
(一)气体的制取和收集
现有如图所示的实验装置:

(1)A装置可用于制氢气、氧气、二氧化碳气体,反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑、2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$H2O+O2↑、CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)实验室需少量甲烷气,可用加热无水醋酸钠与碱石灰的固体混合物制得.制甲烷气的发生装置应选用B(填字母)装置;收集甲烷气可选用C或E装置,由此推断甲烷气具有的物理性质是不溶于水,密度比空气小.
(3)实验室用A装置制取气体前,先向长颈漏斗中加水淹没长颈漏斗的下端,其目的是为了防止气体从长颈漏斗逸出.
(4)用B、D组合制取制氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,检验氧气已集满的方法是带火星的木条放在瓶口来验满,如果带火星的木条在瓶口能复燃,则证明该瓶氧气已经收集满了.
(二)某食品包装袋中有一个小纸袋,上面写“生石灰干燥剂,请勿食用”.该食品已放置两月有余.请你对下列问题进行探究.
(1)小纸袋中的物质能否继续作干燥剂?
(2)猜想:小纸袋中的物质除含有CaO外,还可能含有Ca(OH)2和CaCO3;
(3)请设计实验证明(2)中你所填的物质是否存在加入足量的盐酸,观察是否产生气泡.
(一)气体的制取和收集
现有如图所示的实验装置:

(1)A装置可用于制氢气、氧气、二氧化碳气体,反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑、2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$H2O+O2↑、CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)实验室需少量甲烷气,可用加热无水醋酸钠与碱石灰的固体混合物制得.制甲烷气的发生装置应选用B(填字母)装置;收集甲烷气可选用C或E装置,由此推断甲烷气具有的物理性质是不溶于水,密度比空气小.
(3)实验室用A装置制取气体前,先向长颈漏斗中加水淹没长颈漏斗的下端,其目的是为了防止气体从长颈漏斗逸出.
(4)用B、D组合制取制氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,检验氧气已集满的方法是带火星的木条放在瓶口来验满,如果带火星的木条在瓶口能复燃,则证明该瓶氧气已经收集满了.
(二)某食品包装袋中有一个小纸袋,上面写“生石灰干燥剂,请勿食用”.该食品已放置两月有余.请你对下列问题进行探究.
(1)小纸袋中的物质能否继续作干燥剂?
| 实验步骤 | 实验现象 | 结论 |
| 取足量的小纸袋中的固体放入 烧杯中,加入适量的水,触摸杯壁 | 杯壁变热 | 可继续作干燥剂 |
(3)请设计实验证明(2)中你所填的物质是否存在加入足量的盐酸,观察是否产生气泡.
8.从宏观和微观的不同角度认识物质的变化和性质
(1)①气体X在氧气中燃烧生成氮气和水,X分子中一定含有的原子是N、H(填符号).
②胃酸过多须服用抗酸药.下表为两种抗酸药的有效成分及其构成微粒:
由于抗酸药有效成分不同,起抗酸作用(即消耗胃液中盐酸)的微粒也有差异. Mg(OH)2起抗酸作用的微粒是OH-.铝碳酸镁与盐酸的反应为:AlMg(OH)3CO3+5HCl═MgCl2+AlCl3+4H2O+CO2↑.
则铝碳酸镁起抗酸作用的微粒是OH-、CO32-(填微粒符号).
(2)如图1所示

粒子A最外层电子数是7,在化学反应中容易得填“得”或“失”)电子;微粒A、B、C、D、E中,对应单质化学性质最稳定的是B(填编号,下同),属于同一种元素的是CE D位于元素周期表中第三周期.
(3)如图2所示
图①:从微观角度看,盐酸和氢氧化钠发生中和反应的实质是氢氧根离子和氢离子结合形成水分子.
写出与上述反应本质完全相同的另一个化学方程式2HCl+Ca(OH)2═CaCl2+H2O.
图②:古代字画能够保存很长时间不褪色的原因是常温下碳的化学性质不活泼.
(1)①气体X在氧气中燃烧生成氮气和水,X分子中一定含有的原子是N、H(填符号).
②胃酸过多须服用抗酸药.下表为两种抗酸药的有效成分及其构成微粒:
| 抗胃酸药 | 复方氢氧化镁片剂 | 铝碳酸镁片 |
| 有效成分 | Mg(OH)2 | AlMg(OH)3CO3 |
| 构成微粒 | Mg2+、OH- | Al3+、Mg2+、OH-、CO32- |
则铝碳酸镁起抗酸作用的微粒是OH-、CO32-(填微粒符号).
(2)如图1所示

粒子A最外层电子数是7,在化学反应中容易得填“得”或“失”)电子;微粒A、B、C、D、E中,对应单质化学性质最稳定的是B(填编号,下同),属于同一种元素的是CE D位于元素周期表中第三周期.
(3)如图2所示
图①:从微观角度看,盐酸和氢氧化钠发生中和反应的实质是氢氧根离子和氢离子结合形成水分子.
写出与上述反应本质完全相同的另一个化学方程式2HCl+Ca(OH)2═CaCl2+H2O.
图②:古代字画能够保存很长时间不褪色的原因是常温下碳的化学性质不活泼.
7. 甲、乙两种物质的溶解度曲线如图所示.下列说法正确的是( )
甲、乙两种物质的溶解度曲线如图所示.下列说法正确的是( )
 甲、乙两种物质的溶解度曲线如图所示.下列说法正确的是( )
甲、乙两种物质的溶解度曲线如图所示.下列说法正确的是( )| A. | 甲的溶解度大于乙的溶解度 | |
| B. | t1℃时,甲、乙饱和溶液的溶质质量分数相等 | |
| C. | t2℃时,30g甲溶解在50g水中形成80g溶液 | |
| D. | t2℃时,甲饱和溶液溶质质量分数为50% |
6.除去下列物质中的少量杂质,方法错误的是( )
| 选项 | 物质 | 所含杂质 | 除杂质的方法 |
| A | CO | CO2 | 通过足量的氢氧化钠溶液,干燥 |
| B | Cu | Fe | 加入足量的稀硫酸,过滤,洗涤,干燥 |
| C | CaO | CaCO3 | 加入适量的稀盐酸,过滤,洗涤,干燥 |
| D | KCl溶液 | CuCl2 | 加入适量的氢氧化钾溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
5.下列实验操作符合安全要求的是( )
| A. |  验证氢气的可燃性 | B. |  闻气体气味 | ||
| C. |  移走蒸发皿 | D. |  稀释浓硫酸 |
4.下列有关水的说法中,不正确的是( )
| A. | 雨水的pH一定为7 | |
| B. | 硬水和软水可用肥皂水来区别 | |
| C. | 水是一种常用溶剂 | |
| D. | 电解水时正、负极产生气体的体积比为 1:2 |
3.下列关于物质的变化、性质和用途说法正确的是( )
0 145998 146006 146012 146016 146022 146024 146028 146034 146036 146042 146048 146052 146054 146058 146064 146066 146072 146076 146078 146082 146084 146088 146090 146092 146093 146094 146096 146097 146098 146100 146102 146106 146108 146112 146114 146118 146124 146126 146132 146136 146138 146142 146148 146154 146156 146162 146166 146168 146174 146178 146184 146192 211419
| A. | CO+CuO═Cu+CO2属于置换反应 | |
| B. | 碳酸氢钠能与盐酸发生反应,可治疗胃酸过多 | |
| C. | 氢氧化钠固体能吸水,可用作食品干燥剂 | |
| D. | 动植物的呼吸属于物理变化 |
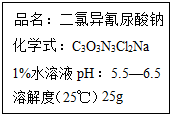 (1)二氯异氰脲酸钠(C3O3N3Cl2Na)是一种预防H7N9禽流感的有效消毒剂.如图为某工厂生产的二氯异氰脲酸钠产品的标签.
(1)二氯异氰脲酸钠(C3O3N3Cl2Na)是一种预防H7N9禽流感的有效消毒剂.如图为某工厂生产的二氯异氰脲酸钠产品的标签. 化学与生活密不可分
化学与生活密不可分