12.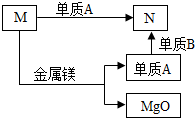 纯净物M、N之间存在着如图所示的转化关系,且反应物和生成物均表示在图示中.单质A和单质B分别由A、B元素组成.据此,有以下的说法:①M是氧化物;②M、N中只有N含有A元素;③N不是氧化物;④M与镁的反应是置换反应;在这些说法中正确的有( )
纯净物M、N之间存在着如图所示的转化关系,且反应物和生成物均表示在图示中.单质A和单质B分别由A、B元素组成.据此,有以下的说法:①M是氧化物;②M、N中只有N含有A元素;③N不是氧化物;④M与镁的反应是置换反应;在这些说法中正确的有( )
 纯净物M、N之间存在着如图所示的转化关系,且反应物和生成物均表示在图示中.单质A和单质B分别由A、B元素组成.据此,有以下的说法:①M是氧化物;②M、N中只有N含有A元素;③N不是氧化物;④M与镁的反应是置换反应;在这些说法中正确的有( )
纯净物M、N之间存在着如图所示的转化关系,且反应物和生成物均表示在图示中.单质A和单质B分别由A、B元素组成.据此,有以下的说法:①M是氧化物;②M、N中只有N含有A元素;③N不是氧化物;④M与镁的反应是置换反应;在这些说法中正确的有( )| A. | ①② | B. | ②④ | C. | ①④ | D. | 只有④正确 |
11.已知浓硫酸比稀硫酸的密度大,质量分数分别为85%和5%的两种硫酸溶液等体积混合后所得溶液的质量分数为( )
| A. | 大于45% | B. | 等于45% | C. | 小于45% | D. | 无法确定 |
8.我校初二学生去桐庐瑶琳仙境春游,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的稀盐酸与样品充分反应来进行实验测定(样品中的杂质不溶于水,且不与盐酸反应),测得如表数据,试回答:
(1)丁同学的实验中稀盐酸有剩余,甲、乙同学的实验中碳酸钙有剩余.
(2)样品中碳酸钙的质量分数是90%,同学们使用的稀盐酸的溶质质量分数是14.6%.
| 甲同学 | 乙同学 | 丙同学 | 丁同学 | |
| 石灰石样品的质量(g) | 10.0 | 10.0 | 10.0 | 10.0 |
| 加入稀盐酸的质量(g) | 20.0 | 30.0 | 45.0 | 50.0 |
| 剩余固体的质量(g) | 6.0 | 4.0 | 1.0 | 1.0 |
(2)样品中碳酸钙的质量分数是90%,同学们使用的稀盐酸的溶质质量分数是14.6%.
5.化学小组同学对酸的性质很感兴趣,向老师提出研究硝酸的性质,老师高兴答应并带领同学们进行了硝酸性质的实验探究.
【实验设计】
(1)将石蕊试液滴入稀硝酸中,预计石蕊试液由紫色变红色.
(2)将Zn片投入稀硝酸中,预计将产生氢气.
【实验验证】同学们按上述设计做了实验,却发现石蕊变色后一会儿即褪去,Zn片投入稀HNO3后,溶液中冒出气泡,产生无色气体A,在试管口气体A变成红棕色有刺激性气味的气体B.
【提出问题】
(1)石蕊试液变色后为何会褪色?
(2)上述产生的无色气体是什么?硝酸具有哪些特性?
【查阅资料】看到如此异常的现象,在老师的指导下,同学们上网查到了下列资料:
(1)硝酸可与Zn、Cu等多种金属反应生成相应的硝酸盐,但不生成H2.
(2)含有氮元素的某些气态物质的物理性质
【猜想与分析】
(1)小明同学认为石蕊变色后又褪色的原因是由于试管不干净,含有其他杂质造成的,要证明小明的观点,应进行的操作是取少量稀HNO3于干净的试管中,滴入石蕊试液.观察实验现象.
(2)大家一致认同了红棕色气体B是NO2,但对于无色气体A及变化的原因有不同的看法:
①小丽同学认为A是NH3,但遭到大家的一致反对,原因是NH3极易溶于水,大多数气体会溶解在稀HNO3中.且在常温下NH3不易被氧化成NO2;
②小强同学认为A是N2,也遭到大家的一致反对,原因是N2的化学性质比较稳定,常温下,N2在空气中不能氧化成NO2;
③经讨论,最终大家获得了“A是NO”的共识.NO遇氧变成NO2的化学方程式为2NO+O2=2NO2.
【实验探究】小红同学对硝酸能与Cu反应很感兴趣,便取了一小块铜片投入稀HNO3中,发现Cu溶解,也出现上述Zn与稀HNO3反应的类似现象,确证生成了NO,并在老师的帮助下,测出恰好反应的Cu和HNO3的质量比为8:21,由此获得了Cu与稀HNO3的反应方程式为3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O.
【交流反思】根据探究结果可知,稀HNO3能跟铜反应的原因是硝酸具有氧化性.
0 145897 145905 145911 145915 145921 145923 145927 145933 145935 145941 145947 145951 145953 145957 145963 145965 145971 145975 145977 145981 145983 145987 145989 145991 145992 145993 145995 145996 145997 145999 146001 146005 146007 146011 146013 146017 146023 146025 146031 146035 146037 146041 146047 146053 146055 146061 146065 146067 146073 146077 146083 146091 211419
【实验设计】
(1)将石蕊试液滴入稀硝酸中,预计石蕊试液由紫色变红色.
(2)将Zn片投入稀硝酸中,预计将产生氢气.
【实验验证】同学们按上述设计做了实验,却发现石蕊变色后一会儿即褪去,Zn片投入稀HNO3后,溶液中冒出气泡,产生无色气体A,在试管口气体A变成红棕色有刺激性气味的气体B.
【提出问题】
(1)石蕊试液变色后为何会褪色?
(2)上述产生的无色气体是什么?硝酸具有哪些特性?
【查阅资料】看到如此异常的现象,在老师的指导下,同学们上网查到了下列资料:
(1)硝酸可与Zn、Cu等多种金属反应生成相应的硝酸盐,但不生成H2.
(2)含有氮元素的某些气态物质的物理性质
| NH3 | N2 | NO | NO2 | |
| 顏色 | 无色 | 无色 | 无色 | 红棕色 |
| 溶解性 | 极易溶于水 | 不溶于水 | 不溶于水 | 可溶于水或硝酸 |
(1)小明同学认为石蕊变色后又褪色的原因是由于试管不干净,含有其他杂质造成的,要证明小明的观点,应进行的操作是取少量稀HNO3于干净的试管中,滴入石蕊试液.观察实验现象.
(2)大家一致认同了红棕色气体B是NO2,但对于无色气体A及变化的原因有不同的看法:
①小丽同学认为A是NH3,但遭到大家的一致反对,原因是NH3极易溶于水,大多数气体会溶解在稀HNO3中.且在常温下NH3不易被氧化成NO2;
②小强同学认为A是N2,也遭到大家的一致反对,原因是N2的化学性质比较稳定,常温下,N2在空气中不能氧化成NO2;
③经讨论,最终大家获得了“A是NO”的共识.NO遇氧变成NO2的化学方程式为2NO+O2=2NO2.
【实验探究】小红同学对硝酸能与Cu反应很感兴趣,便取了一小块铜片投入稀HNO3中,发现Cu溶解,也出现上述Zn与稀HNO3反应的类似现象,确证生成了NO,并在老师的帮助下,测出恰好反应的Cu和HNO3的质量比为8:21,由此获得了Cu与稀HNO3的反应方程式为3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O.
【交流反思】根据探究结果可知,稀HNO3能跟铜反应的原因是硝酸具有氧化性.
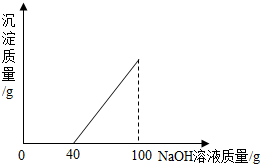 在硫酸与硫酸铜的混合溶液200克中,滴入40%的氢氧化钠溶液100克,恰好完全反应.记录反应过程,得到的沉淀与所加的氢氧化钠溶液的质量关系如图所示.
在硫酸与硫酸铜的混合溶液200克中,滴入40%的氢氧化钠溶液100克,恰好完全反应.记录反应过程,得到的沉淀与所加的氢氧化钠溶液的质量关系如图所示.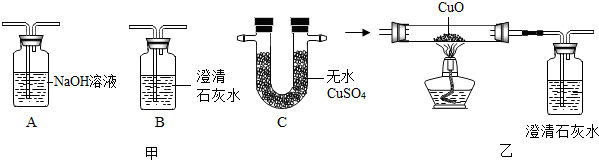
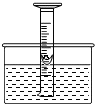 某化学兴趣小组,设计了如图所示装置来研究空气中氮气的体积分数,用一个50mL量筒倒扣在水中,使量筒内内外液面均位于40mL处.量筒内浮着一个铜制的小船,船中放有足量白磷.现把浓硫酸缓缓倒入水中并搅拌.一会儿,白磷发生自燃,量筒内液面上升,向水槽内加水直至量筒内外液面相平,读出此时液面所对刻度.
某化学兴趣小组,设计了如图所示装置来研究空气中氮气的体积分数,用一个50mL量筒倒扣在水中,使量筒内内外液面均位于40mL处.量筒内浮着一个铜制的小船,船中放有足量白磷.现把浓硫酸缓缓倒入水中并搅拌.一会儿,白磷发生自燃,量筒内液面上升,向水槽内加水直至量筒内外液面相平,读出此时液面所对刻度.