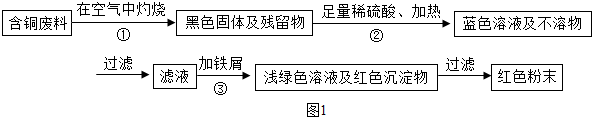
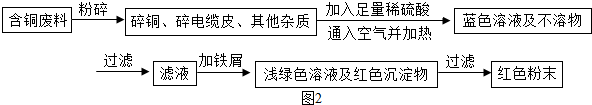
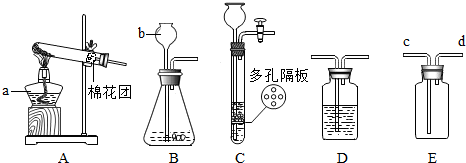
9.在一个密闭容器中放入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如表:
下列说法中,不正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 25 | 15 | 1 | 5 |
| 反应后质量/g | 11 | 未测 | 1 | 22 |
| A. | 未测值为12 | B. | 丙一定是催化剂 | ||
| C. | 乙全部发生了反应 | D. | 甲与乙反应的质量比为14:3 |
5.每年的3月22日是“世界水日”,水与人类生活和生产密切相关.请回答以下问题:
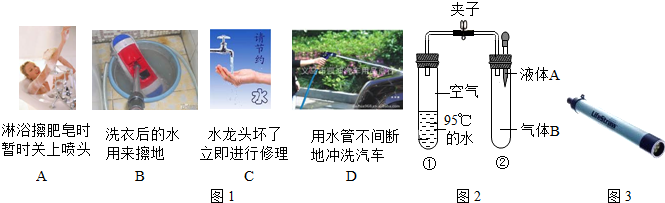
(1)水是生命之源,保护水资源、节约用水是我们义不容辞的责任.如图1所示做法不能节约用水的是D.
(2)通常条件下水的沸点是100℃,随着压强增大,水的沸点会逐渐升高.如图2是研究水沸点的实验.夹子开始处于关闭状态,将液体 A滴入试管②,打开夹子,试管①内的水立刻沸腾.则液体A和气体B的组合可能是B(填序号).并写出试管②中发生反应的方程式CO2+2NaOH=Na2CO3+H2O
(3)“生命吸管”(如图3)是一种可以随身携带的小型水净化器,里面装有网丝、注入活性炭和碘的树脂等.其中活性炭起到吸附作用.
①该装置能否将硬水转化为软水否(填“能”或“否”).
②可用肥皂水来检验净化后的水是硬水还是软水.
③家庭中,要降低水的硬度,通常采用煮沸.

(1)水是生命之源,保护水资源、节约用水是我们义不容辞的责任.如图1所示做法不能节约用水的是D.
(2)通常条件下水的沸点是100℃,随着压强增大,水的沸点会逐渐升高.如图2是研究水沸点的实验.夹子开始处于关闭状态,将液体 A滴入试管②,打开夹子,试管①内的水立刻沸腾.则液体A和气体B的组合可能是B(填序号).并写出试管②中发生反应的方程式CO2+2NaOH=Na2CO3+H2O
| 序号 | A | B | C |
| 液体A | 水 | 氢氧化钠溶液 | 水 |
| 气体B | 氮气 | 二氧化碳 | 一氧化碳 |
①该装置能否将硬水转化为软水否(填“能”或“否”).
②可用肥皂水来检验净化后的水是硬水还是软水.
③家庭中,要降低水的硬度,通常采用煮沸.
3.鱼类腥味产生的原因是由于鱼身上存在有机化学物质甲胺,甲胺易溶于乙醇,因此,煮鱼时加些酒,能使甲胺等溶于乙醇并随加热后挥发逸去,经过这样烹饪的鱼就不再有腥味了.下列过程与上面所述原理不相似的是( )
| A. | 用洗涤剂洗碗 | B. | 用白醋除去水垢 | ||
| C. | 用汽油除去衣服上的油污 | D. | 用酒精将试管壁上的碘洗掉 |
2.下列实验现象描述正确的是( )
| A. | 甲烷在空气中燃烧生成水和二氧化碳 | |
| B. | 镁带在空气中燃烧生成黑色固体 | |
| C. | 硫在空气中燃烧,发出淡蓝色火焰 | |
| D. | 米汤中滴加碘盐溶液,会变蓝 |
1.下列不符合“节能减排”主题的是( )
0 145850 145858 145864 145868 145874 145876 145880 145886 145888 145894 145900 145904 145906 145910 145916 145918 145924 145928 145930 145934 145936 145940 145942 145944 145945 145946 145948 145949 145950 145952 145954 145958 145960 145964 145966 145970 145976 145978 145984 145988 145990 145994 146000 146006 146008 146014 146018 146020 146026 146030 146036 146044 211419
| A. | 用旧报纸制铅笔杆 | B. | 参加“地球熄灯一小时”活动 | ||
| C. | 开发回收利用二氧化碳的新技术 | D. | 深秋时节焚烧落叶 |
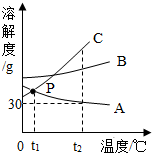 如图是A、B、C三种物质的溶解度曲线,据图回答:
如图是A、B、C三种物质的溶解度曲线,据图回答: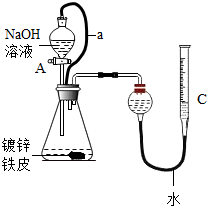 “白铁皮”是一种广泛应用于生产生活的金属材料. 某班级分两个兴趣小组开展了对“白铁皮”相关性质及应用的调查研究活动.
“白铁皮”是一种广泛应用于生产生活的金属材料. 某班级分两个兴趣小组开展了对“白铁皮”相关性质及应用的调查研究活动.