11.学习化学的目的是要善于用化学知识去分析、解决生产生活中的问题.从化学的角度看,下列说法中不正确的是( )
| A. | 夜晚发现厨房煤气管道漏气,立即关闭阀门并开窗通风 | |
| B. | 人们每天的饮食中都应有蔬菜、水果,其目的是补充蛋白质 | |
| C. | 扑灭电器、图书档案等火灾最适宜的灭火器是液态二氧化碳灭火器 | |
| D. | 若不慎将燃着的酒精灯碰倒,洒出的酒精在桌上燃烧,应立刻用湿抹布扑盖 |
10.下列有关实验现象的描述正确的是( )
| A. | 红磷在氧气中燃烧产生大量的白烟 | |
| B. | 铁丝在空气中剧烈燃烧时,火星四射,生成黑色固体 | |
| C. | 打开盛有浓硫酸的试剂瓶的瓶盖,瓶口上方出现大量白雾 | |
| D. | 将碘酒滴入淀粉溶液中,溶液变紫色 |
9.下列对实验结果推测正确的是( )
| A. | 无色气体在空气中燃烧产生蓝色火焰,说明气体是甲烷 | |
| B. | 某固体中加入稀盐酸,产生无色,无味的气体,该固体中不一定含有CO32- | |
| C. | 往溶液中滴加氯化钡溶液有白色沉淀,该沉淀一定是BaSO4 | |
| D. | 某无色溶液中滴入无色酚酞试液,显无色,该溶液一定不是酸溶液 |
8.饮用水可用二氧化氯(ClO2)来做消毒剂.用氯酸钠(NaClO3)和盐酸反应可制得二氧化氯,反应方程式:2NaClO3+4HCl═2ClO2↑+Cl2↑+2X+2NaCl,请推断出X的化学式为( )
| A. | H2O | B. | NaOH | C. | HClO | D. | HClO3 |
7.碘盐中的碘是人体必需的微量元素之一.下列说法错误的是( )
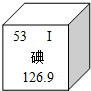

| A. | 食用加碘食盐可以预防“大脖子病” | B. | 碘原子的质子数为53 | ||
| C. | 碘元素的相对原子质量为126.9 | D. | 碘原子的中子数为53 |
5.下列烹饪用的调味品与足量水充分搅拌,不能形成溶液的是( )
| A. | 食盐 | B. | 黄酒 | C. | 花生油 | D. | 白糖 |
4.我国著名的闽籍制碱专家侯德榜,在纯碱制造方面做出了重大贡献.用“侯氏制碱法”制得的纯碱中常含有氯化钠等杂质,化学兴趣小组欲对某品牌纯碱样品中碳酸钠的质量分数进行实验探究,在老师的指导下,他们设计了下列两种实验方案进行试验.
资料摘要:
Ⅰ.碳酸钠和氯化钙能发生复分解反应.
Ⅱ.浓硫酸具有很强的吸水性;碱石灰常用于吸收水蒸气和二氧化碳.
[方案一]样品与氯化钙溶液反应,测定Na2CO3的质量分数
(1)样品与氯化钙溶液的反应实验(杂质不与氯化钙溶液反应):
(2)分析滴加的CaCl2溶液要过量的原因:与碳酸钠充分反应;
(3)将反应后的混合物进行过滤,把获得的沉淀物进行洗涤、干燥、称量.利用沉淀物质量计算Na2CO3的质量分数为91%.如果不洗涤沉淀物会造成测定结果大于91%,这是因为不洗涤碳酸钙表面可能会附着一层可溶性物质使沉淀物质量增加,所以使得计算出的碳酸钠的质量增大.
[方案二]样品与稀盐酸反应,测定Na2CO3的质量分数
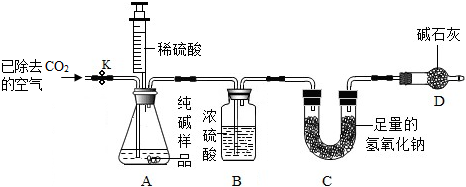
利用如图所示实验装置(铁架台略去)和试剂,通过测定样品和稀盐酸反应产生的CO2气体的质量,计算Na2CO3的质量分数(装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的).
(4)打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置A和B中含有的二氧化碳,再接上装置C和D.
(5)关闭止水夹K,加入足量的稀盐酸(杂质不与盐酸反应),装置A中样品产生气体的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(6)待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一会儿.根据质量守恒 定律,装置C(填标号)在反应前后的质量差就是产生CO2的质量,由此计算出该样品中Na2CO3的质量分数.若没有装置D,将会使测定结果偏大(选填“偏大”或“偏小”).

资料摘要:
Ⅰ.碳酸钠和氯化钙能发生复分解反应.
Ⅱ.浓硫酸具有很强的吸水性;碱石灰常用于吸收水蒸气和二氧化碳.
[方案一]样品与氯化钙溶液反应,测定Na2CO3的质量分数
(1)样品与氯化钙溶液的反应实验(杂质不与氯化钙溶液反应):
| 实验操作 | 实验现象 | 实验结论 |
| 取一定量纯碱样品配成溶液后,滴加过量的CaCl2溶液. | 产生白色沉淀 | 反应的化学方程式: Na2CO3+CaCl2═CaCO3↓+2NaCl |
(3)将反应后的混合物进行过滤,把获得的沉淀物进行洗涤、干燥、称量.利用沉淀物质量计算Na2CO3的质量分数为91%.如果不洗涤沉淀物会造成测定结果大于91%,这是因为不洗涤碳酸钙表面可能会附着一层可溶性物质使沉淀物质量增加,所以使得计算出的碳酸钠的质量增大.
[方案二]样品与稀盐酸反应,测定Na2CO3的质量分数
利用如图所示实验装置(铁架台略去)和试剂,通过测定样品和稀盐酸反应产生的CO2气体的质量,计算Na2CO3的质量分数(装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的).
(4)打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置A和B中含有的二氧化碳,再接上装置C和D.
(5)关闭止水夹K,加入足量的稀盐酸(杂质不与盐酸反应),装置A中样品产生气体的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(6)待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一会儿.根据质量守恒 定律,装置C(填标号)在反应前后的质量差就是产生CO2的质量,由此计算出该样品中Na2CO3的质量分数.若没有装置D,将会使测定结果偏大(选填“偏大”或“偏小”).
3.用一种试剂就能鉴别硫酸钾、硫酸铵、氯化钾和氯化铵四瓶无色溶液,该试剂是( )
| A. | 氢氧化钠溶液 | B. | 硝酸钡溶液 | C. | 硝酸银溶液 | D. | 氢氧化钡溶液 |
2.下列实验方案中,可行的是( )
0 145827 145835 145841 145845 145851 145853 145857 145863 145865 145871 145877 145881 145883 145887 145893 145895 145901 145905 145907 145911 145913 145917 145919 145921 145922 145923 145925 145926 145927 145929 145931 145935 145937 145941 145943 145947 145953 145955 145961 145965 145967 145971 145977 145983 145985 145991 145995 145997 146003 146007 146013 146021 211419
| A. | 用细铁丝在密闭容器中燃烧,除尽密闭容器内空气中的氧气 | |
| B. | 向某种溶液中加入氯化钡溶液,产生白色沉淀,证明该溶液一定是硫酸盐 | |
| C. | 按溶解、过滤、蒸发的操作顺序可以分离CaCl2、CaCO3的混合物 | |
| D. | 用玻璃棒蘸取食用白醋滴在润湿pH试纸上,测定其pH |