2. 按如图所示装置进行实验(图中铁架台均已略去).先在试管Ⅱ中加入试剂乙,然后在试管Ⅰ中加入试剂甲,立即塞紧橡皮塞,一段时间后,观察到试管Ⅱ中有白色沉淀生成.符合以上实验现象的一组试剂是( )
按如图所示装置进行实验(图中铁架台均已略去).先在试管Ⅱ中加入试剂乙,然后在试管Ⅰ中加入试剂甲,立即塞紧橡皮塞,一段时间后,观察到试管Ⅱ中有白色沉淀生成.符合以上实验现象的一组试剂是( )
 按如图所示装置进行实验(图中铁架台均已略去).先在试管Ⅱ中加入试剂乙,然后在试管Ⅰ中加入试剂甲,立即塞紧橡皮塞,一段时间后,观察到试管Ⅱ中有白色沉淀生成.符合以上实验现象的一组试剂是( )
按如图所示装置进行实验(图中铁架台均已略去).先在试管Ⅱ中加入试剂乙,然后在试管Ⅰ中加入试剂甲,立即塞紧橡皮塞,一段时间后,观察到试管Ⅱ中有白色沉淀生成.符合以上实验现象的一组试剂是( )| A. | 甲:Na2CO3、稀HCl;乙:NaOH溶液 | B. | 甲:NaOH溶液、稀盐酸;乙:AgNO3 | ||
| C. | 甲:Mg、稀H2SO4;乙:Ba(NO3)2溶液 | D. | 甲:Cu、稀H2SO4;乙:BaCl2溶液 |
1.碳及其化合物的相互转化关系如下所示:下列叙述正确的是( )
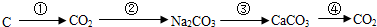
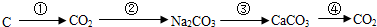
| A. | ①这步转化发生的一定是化合反应 | |
| B. | ②这步转化发生的一定是复分解反应 | |
| C. | ③这步转化发生的一定不是复分解反应 | |
| D. | ④这步转化发生的可能是复分解反应 |
20.每年的6月1日为“世界牛奶日”.某品牌牛奶富含蛋白质、糖类、无机盐等营养物质.下列叙述错误的是( )
| A. | 蛋白质、糖类都属于有机物 | |
| B. | 青少年常饮牛奶有利于骨骼生长 | |
| C. | 可用新制的氢氧化铜悬浊液来检验葡萄糖 | |
| D. | 牛奶中的蛋白质能使碘液变蓝色 |
19.下列实验操作正确的是( )
| A. | 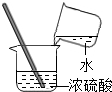 稀释浓硫酸 | B. | 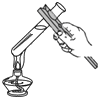 加热液体 | ||
| C. | 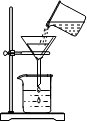 过滤 | D. | 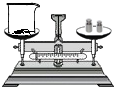 称量氢氧化钠固体 |
18.某“暖手包”中发热剂的成分为:铁粉、活性炭及氯化钠三种物质.这些物质对“暖手包”发热有什么作用?小科在老师的指导下,在一隔热的密闭容器中进行了下列实验,并测定了密闭容器内的空气湿度、O2的体积分数及上升温度(△t)等数据,结果如下:
(1)第1、2、3组的实验说明,“暖手包”中能更好吸收空气中的水蒸气的物质是活性炭;
(2)上述实验说明,“暖手包”发热时实际上是Fe粉与氧气、水蒸气共同作用的结果.
(3)为进一步测定发热剂中活性炭的质量分数,小科和同学们分别称取等质量的两份发热剂,设计了两种方案准备进行实验.
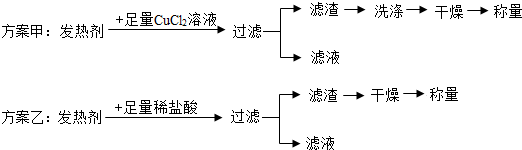
但老师指出,这两种方案都有不足,最终会导致测定结果偏大.请你分析:
方案甲的不足之处是Fe与CuCl2溶液会反应生成Cu;
方案乙的不足之处是滤渣没有洗涤.
| 组别 | 时间 | 铁 | 活性炭 | 空气湿度 | O2的体积分数 | 上升温度(△t) |
| 1 | 30min | 0 | 0 | 70% | 21% | 0 |
| 2 | 30min | 0 | 0.6g | 40% | 21% | 0 |
| 3 | 30min | 1.0g | 0 | 66% | 20% | 3.2℃ |
| 4 | 30min | 1.0g | 0.6g | 40% | 17% | 10.7℃ |
(2)上述实验说明,“暖手包”发热时实际上是Fe粉与氧气、水蒸气共同作用的结果.
(3)为进一步测定发热剂中活性炭的质量分数,小科和同学们分别称取等质量的两份发热剂,设计了两种方案准备进行实验.

但老师指出,这两种方案都有不足,最终会导致测定结果偏大.请你分析:
方案甲的不足之处是Fe与CuCl2溶液会反应生成Cu;
方案乙的不足之处是滤渣没有洗涤.
17.某化学兴趣小组要用80克10%的氢氧化钠溶液来制作“叶脉书签”,如图是他配置氢氧化钠溶液的操作示意图.

(1)称量氢氧化钠固体时,不能将固体直接放在纸上称量的原因是氢氧化钠固体易潮解,具有腐蚀性;
(2)在配置上述溶液时,下列操作失误,会引起溶质质量分数降低的是a;
a.用量筒量取水时,仰视读数
b.将量筒中的水倒入烧杯中时,有少量的水溅出
(3)一周后,化学兴趣小组整理实验室时,发现上周实验时取用氢氧化钠固体后忘记盖上瓶盖,老师告知,此瓶氢氧化钠固体已经变质,但未知变质程度,为此,该化学兴趣小组在老师的指导下进行有关实验探究.
【查阅资料】CaCl2溶液和BaCl2溶液都呈中性
【提出问题】
①氢氧化钠固体变质的原因?用化学方程式表示2NaOH+CO2=Na2CO3+H2O;
②氢氧化钠固体变质程度如何?
【实验设计】
化学兴趣小组分成甲、乙两组进行实验探究.
甲组方案:取少量固体样品于烧杯中,加蒸馏水完全溶解,然后滴入Ca(OH)2溶液,直到不再产生沉淀为止,静置,滴入无色酚酞试液,溶液变红,说明氢氧化钠固体部分变质.
乙组不同意甲组的观点,请说明理由:溶液变红,有可能是因为氢氧化钙与碳酸钠反应生成氢氧化钠导致的.
乙组方案:根据如下提供的药品设计实验方案,请你完成下表.
提供的药品:酚酞试液,CaCl2溶液,Ca(OH)2溶液,稀盐酸,BaCl2溶液,蒸馏水.

(1)称量氢氧化钠固体时,不能将固体直接放在纸上称量的原因是氢氧化钠固体易潮解,具有腐蚀性;
(2)在配置上述溶液时,下列操作失误,会引起溶质质量分数降低的是a;
a.用量筒量取水时,仰视读数
b.将量筒中的水倒入烧杯中时,有少量的水溅出
(3)一周后,化学兴趣小组整理实验室时,发现上周实验时取用氢氧化钠固体后忘记盖上瓶盖,老师告知,此瓶氢氧化钠固体已经变质,但未知变质程度,为此,该化学兴趣小组在老师的指导下进行有关实验探究.
【查阅资料】CaCl2溶液和BaCl2溶液都呈中性
【提出问题】
①氢氧化钠固体变质的原因?用化学方程式表示2NaOH+CO2=Na2CO3+H2O;
②氢氧化钠固体变质程度如何?
【实验设计】
化学兴趣小组分成甲、乙两组进行实验探究.
甲组方案:取少量固体样品于烧杯中,加蒸馏水完全溶解,然后滴入Ca(OH)2溶液,直到不再产生沉淀为止,静置,滴入无色酚酞试液,溶液变红,说明氢氧化钠固体部分变质.
乙组不同意甲组的观点,请说明理由:溶液变红,有可能是因为氢氧化钙与碳酸钠反应生成氢氧化钠导致的.
乙组方案:根据如下提供的药品设计实验方案,请你完成下表.
提供的药品:酚酞试液,CaCl2溶液,Ca(OH)2溶液,稀盐酸,BaCl2溶液,蒸馏水.
| 实验操作步骤 | 实验现象 | 结论 |
| a.取少量氢氧化钠固体样品于试管中 b.加蒸馏水完全溶解 c.先加入过量的CaCl2溶液(或BaCl2溶液)溶液然后滴加酚酞试液 | 有白色沉淀生成(或溶液变浑浊) 溶液变为红色 | 氢氧化钠固体部分变质 |
16.某同学为了测定NaCl和MgCl2固体混合物中MgCl2的质量分数,进行如下实验:将80g固体混合物溶于水配成溶液,平均分成四份,分别加入相同质量分数的NaOH溶液,获得如下实验数据:
问:
(1)表中m的值为5.8g;
(2)原固体混合物中MgCl2的质量分数是多少?(要求写出计算过程)
0 145755 145763 145769 145773 145779 145781 145785 145791 145793 145799 145805 145809 145811 145815 145821 145823 145829 145833 145835 145839 145841 145845 145847 145849 145850 145851 145853 145854 145855 145857 145859 145863 145865 145869 145871 145875 145881 145883 145889 145893 145895 145899 145905 145911 145913 145919 145923 145925 145931 145935 145941 145949 211419
| 实验次数 | 一 | 二 | 三 | 四 |
| 固体混合物的质量(g) | 20 | 20 | 20 | 20 |
| 加入NaOH溶液的质量(g) | 20 | 40 | 60 | 80 |
| 生成沉淀的质量(g) | 2.9 | m | 8.7 | 8.7 |
(1)表中m的值为5.8g;
(2)原固体混合物中MgCl2的质量分数是多少?(要求写出计算过程)
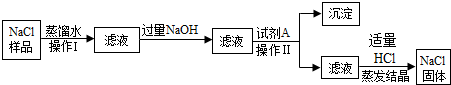
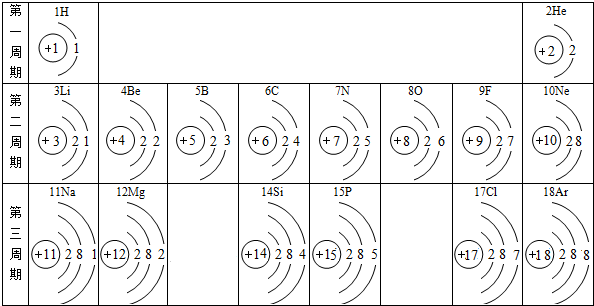
 化学反应中该原子比较容易得到(填“得到”或“失去”)电子变成离子;
化学反应中该原子比较容易得到(填“得到”或“失去”)电子变成离子;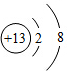 表示的是Al3+(填离子符号);
表示的是Al3+(填离子符号);