2.为提高实验探究能力,某化学兴趣小组的同学在老师的指导下,对一瓶久置出现变质硬化的氢氧化钙固体进行如下探究活动.
【探究活动一】试验硬化的氢氧化钙样品是否完全变质
(1)用化学方程式表示氢氧化钙变质的原因:CO2+Ca(OH)2═CaCO3↓+H2O.
(2)检验氢氧化钙样品是否完全变质,进行如下实验:
【探究活动二】测定样品中含有的变质固体(以下用R表示)的质量分数
取3克部分变质的氢氧化钙样品与足量的稀盐酸反应,测量生成气体的体积(气体不溶于植物油),从而计算出样品中R的质量,便可求出样品中R的质量分数.实验装置(气密性良好)如图1所示.

(3)将稀盐酸滴入样品中,产生气体的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,反应一段时间后,当观察到无气泡产生(填实验现象),才停止滴加稀盐酸.
(4)实验中量筒的作用是根据进入量筒内水的体积,测量生成的CO2的体积.
(5)实验结束后,量筒内进入水的体积如图2所示,其读数为165mL.已知在该实验条件下,生成气体的密度为2g•L-1,通过计算,样品中R的质量分数为25%.
(6)上述图1所示实验装置和相关试剂,用来实验测定样品中R的质量分数是比较粗略的,请简要说明测定数据存在误差的原因:无法考虑盐酸加入后烧瓶内物质所占体积的变化对测定数据产生的影响(写一个).
【探究活动一】试验硬化的氢氧化钙样品是否完全变质
(1)用化学方程式表示氢氧化钙变质的原因:CO2+Ca(OH)2═CaCO3↓+H2O.
(2)检验氢氧化钙样品是否完全变质,进行如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取氢氧化钙样品少量,研细后加适量蒸馏水 充分混合后静置,取少量上层清液,滴加1~2滴无色酚酞试液 | 溶液变成红色 | 该样品还含有氢氧化钙 |
取3克部分变质的氢氧化钙样品与足量的稀盐酸反应,测量生成气体的体积(气体不溶于植物油),从而计算出样品中R的质量,便可求出样品中R的质量分数.实验装置(气密性良好)如图1所示.

(3)将稀盐酸滴入样品中,产生气体的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,反应一段时间后,当观察到无气泡产生(填实验现象),才停止滴加稀盐酸.
(4)实验中量筒的作用是根据进入量筒内水的体积,测量生成的CO2的体积.
(5)实验结束后,量筒内进入水的体积如图2所示,其读数为165mL.已知在该实验条件下,生成气体的密度为2g•L-1,通过计算,样品中R的质量分数为25%.
(6)上述图1所示实验装置和相关试剂,用来实验测定样品中R的质量分数是比较粗略的,请简要说明测定数据存在误差的原因:无法考虑盐酸加入后烧瓶内物质所占体积的变化对测定数据产生的影响(写一个).
17.用158g高锰酸钾制取氧气的实验里,反应一段时间后测得前后固体物质中锰元素的质量分数之比为75:79,则生成氧气的质量是( )
| A. | 8g | B. | 16g | C. | 32g | D. | 4g |
16.下列有关资源能源的说法正确的是( )
| A. | 空气中氧气的质量分数为21% | |
| B. | 大气水、生物水、海洋水、河流水、湖泊水等都属于水资源 | |
| C. | 可燃冰是一种燃烧值大的正在广泛开发利用的新能源 | |
| D. | 金属资源都存在于地壳和海洋中 |
15.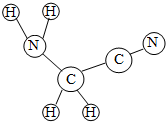 氨基乙腈广泛应用于药品的一种原料.如图是氨基乙腈的分子结构模型,下列说法正确的是( )
氨基乙腈广泛应用于药品的一种原料.如图是氨基乙腈的分子结构模型,下列说法正确的是( )
 氨基乙腈广泛应用于药品的一种原料.如图是氨基乙腈的分子结构模型,下列说法正确的是( )
氨基乙腈广泛应用于药品的一种原料.如图是氨基乙腈的分子结构模型,下列说法正确的是( )| A. | 氨基乙腈是由碳、氢、氮三种原子构成的 | |
| B. | 氨基乙腈中碳、氢、氮原子的个数比为1:2:1 | |
| C. | 一个氨基乙腈分子有8个原子,56个质子 | |
| D. | 氨基乙腈是一种有机高分子化合物 |
14.下列变化主要发生化学变化的是( )
0 145693 145701 145707 145711 145717 145719 145723 145729 145731 145737 145743 145747 145749 145753 145759 145761 145767 145771 145773 145777 145779 145783 145785 145787 145788 145789 145791 145792 145793 145795 145797 145801 145803 145807 145809 145813 145819 145821 145827 145831 145833 145837 145843 145849 145851 145857 145861 145863 145869 145873 145879 145887 211419
| A. |  浓硫酸在纸上写字 | B. |  检查装置气密性 | ||
| C. | 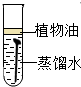 铁生锈实验探究 | D. | 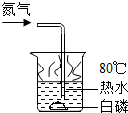 燃烧条件的探究 |

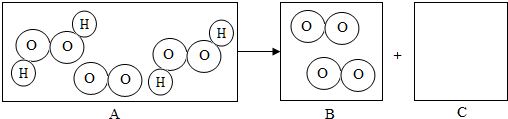
 表示氢原子,用
表示氢原子,用 表示氧原子);
表示氧原子); 电动独轮车是新一代的节能、环保、便携的代步工具.它体形小巧、携带方便,最轻的一款只有10Kg,可以直接放进汽车后备箱,提到家里或是办公室.
电动独轮车是新一代的节能、环保、便携的代步工具.它体形小巧、携带方便,最轻的一款只有10Kg,可以直接放进汽车后备箱,提到家里或是办公室. 在紧张的学习生活中,一份美味的营养午餐不仅能为我们补充能量,也能带来好心情.右图是一份营养餐,包含了排骨、胡萝卜、玉米、西兰花、鸡蛋、米饭等食物.其中排骨和鸡蛋主要为人体提供的营养素是(1)蛋白质胡萝卜、西兰花富含的营养素对人体的作用是(2)调节新陈代谢、预防疾病、维持身体健康,玉米富含的营养素在人体内经(3)酶的催化作用,与(4)水发生一系列反应,最终变成(5)C6H12O6(填化学式).为了促进玉米的生长有时需要施加适量钾肥,请写出一种钾肥的化学式(6)KCl.该化肥 作用是保证(7)各种代谢过程的顺利进行,增强植物的(8)抗病虫害、抗倒伏能力.
在紧张的学习生活中,一份美味的营养午餐不仅能为我们补充能量,也能带来好心情.右图是一份营养餐,包含了排骨、胡萝卜、玉米、西兰花、鸡蛋、米饭等食物.其中排骨和鸡蛋主要为人体提供的营养素是(1)蛋白质胡萝卜、西兰花富含的营养素对人体的作用是(2)调节新陈代谢、预防疾病、维持身体健康,玉米富含的营养素在人体内经(3)酶的催化作用,与(4)水发生一系列反应,最终变成(5)C6H12O6(填化学式).为了促进玉米的生长有时需要施加适量钾肥,请写出一种钾肥的化学式(6)KCl.该化肥 作用是保证(7)各种代谢过程的顺利进行,增强植物的(8)抗病虫害、抗倒伏能力.