6.(1)镁将成为2 1世纪重要的轻型环保材料,我国含有非常丰富的镁资源.老师每次做有关镁的实验时都会强调:镁是一种银白色有金属光泽的金属.但拿出的镁条总是有一层灰黑色的“外衣“,这层灰黑色的外衣是什么物质呢?
猜想:小明认为可能是MgO;
小赵认为可能是Mg2(OH)2C03;
小花认为可能是Mg(OH)2.
小赵认为小明的猜想是错误的,其理由是是氧化镁为白色固体与水缓慢反应生成氢氧化镁,而信息中为灰黑色物质.
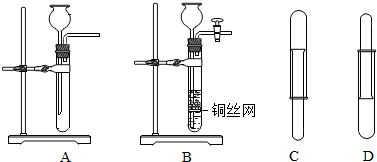
实验探究:小赵按图3所示装置进行实验,发现试管口有液滴出现,澄清石灰水变浑浊,同时试管内生成白色固体.
实验分析:实验后,小赵认为小花的猜测也是错误的,其理由是样品分解生成的二氧化碳使澄清石灰水变浑浊,而氢氧化镁不会生成二氧化碳.
查阅资料得出结论:Mg(OH)2和Mg2(OH)2CO3都可以加热分解,产物均为氧化物,据此请你写出Mg2(OH)2C03加热分解的化学方程式Mg2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+CO2↑+H2O
(2)已知某金属粉末中除含有Al外还含有一定量的Fe和Cu,为证明Al、Fe和Cu的存在并测定其中Al的质量分数,某化学兴趣小组的同学展开了如下的实验探究.
资料在线:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.
①化学兴趣小组的同学讨论了证明金属粉末中存在Al、Fe和Cu的实验设计,下列他们的说法正确的是AB.
A.先加氢氧化钠溶液后加稀盐酸 B.加入的溶液都要过量
C.反应过程中溶液始终是无色 D.充分反应到最后,无固体残留
②为探究该金属粉末中Al的质量分数,取20g该金属粉末,把100g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据与图象如图4:
Ⅰ.分析以上数据可知,上表中n的值为14.6g;
Ⅱ.该金属粉末中Al的质量分数为70%
Ⅲ.列式计算:第一次参加反应氢氧化钠的质量?
0 145630 145638 145644 145648 145654 145656 145660 145666 145668 145674 145680 145684 145686 145690 145696 145698 145704 145708 145710 145714 145716 145720 145722 145724 145725 145726 145728 145729 145730 145732 145734 145738 145740 145744 145746 145750 145756 145758 145764 145768 145770 145774 145780 145786 145788 145794 145798 145800 145806 145810 145816 145824 211419
猜想:小明认为可能是MgO;
小赵认为可能是Mg2(OH)2C03;
小花认为可能是Mg(OH)2.
小赵认为小明的猜想是错误的,其理由是是氧化镁为白色固体与水缓慢反应生成氢氧化镁,而信息中为灰黑色物质.
实验探究:小赵按图3所示装置进行实验,发现试管口有液滴出现,澄清石灰水变浑浊,同时试管内生成白色固体.
实验分析:实验后,小赵认为小花的猜测也是错误的,其理由是样品分解生成的二氧化碳使澄清石灰水变浑浊,而氢氧化镁不会生成二氧化碳.
查阅资料得出结论:Mg(OH)2和Mg2(OH)2CO3都可以加热分解,产物均为氧化物,据此请你写出Mg2(OH)2C03加热分解的化学方程式Mg2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+CO2↑+H2O
(2)已知某金属粉末中除含有Al外还含有一定量的Fe和Cu,为证明Al、Fe和Cu的存在并测定其中Al的质量分数,某化学兴趣小组的同学展开了如下的实验探究.
资料在线:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.
①化学兴趣小组的同学讨论了证明金属粉末中存在Al、Fe和Cu的实验设计,下列他们的说法正确的是AB.
A.先加氢氧化钠溶液后加稀盐酸 B.加入的溶液都要过量
C.反应过程中溶液始终是无色 D.充分反应到最后,无固体残留
| 加NaOH溶液的次数 | 第一次 | 第二次 | 第三次 | … |
| 剩余固体的质量/g | 17.3 | n | 11.9 | … |
Ⅰ.分析以上数据可知,上表中n的值为14.6g;
Ⅱ.该金属粉末中Al的质量分数为70%

Ⅲ.列式计算:第一次参加反应氢氧化钠的质量?