5.物质的性质决定其保存方法.氢氧化钠固体必须密封保存的主要原因是( )
| A. | 白色固体 | B. | 有腐蚀性 | ||
| C. | 易吸收水分 | D. | 能与空气中的二氧化碳反应 |
4.乙醇俗称酒精,可用作医用消毒,也常作燃料.其完全燃烧的化学方程式可表示为:C2H6O+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+
3H2O
(1)根据化学方程式计算:46g乙醇完全燃烧需消耗多少克氧气?
(2)乙醇不完全燃烧会产生CO,某实验测得反应前后各物质的质量如下表,回答下列问题
①表中a的值为1.4
②请完成该反应的化学方程式:4C2H6O+11O2$\frac{\underline{\;点燃\;}}{\;}$6CO2+12H2O+2CO.
3H2O
(1)根据化学方程式计算:46g乙醇完全燃烧需消耗多少克氧气?
(2)乙醇不完全燃烧会产生CO,某实验测得反应前后各物质的质量如下表,回答下列问题
| 物质 | 乙醇 | 氧气 | CO2 | 水 | CO |
| 反应前质量(g) | 4.6 | 8.8 | 0 | 0 | 0 |
| 反应后质量(g) | 0 | 0 | 6.6 | 5.4 | a |
②请完成该反应的化学方程式:4C2H6O+11O2$\frac{\underline{\;点燃\;}}{\;}$6CO2+12H2O+2CO.
2.生活中常遇见铜制品生锈的情况.活动课上,同学们设计实验对铜锈进行了如下探究活动.

探究活动一:验证铜锈的组成
【査阅资料】①铜锈为绿色,其主要成分是Cu2(OH)2CO3.②白色的硫酸铜粉末遇水能变为蓝色.③碳不与稀硫酸反应.④氧化铜为黑色固体,能与稀硫酸反应生成硫酸铜溶液.
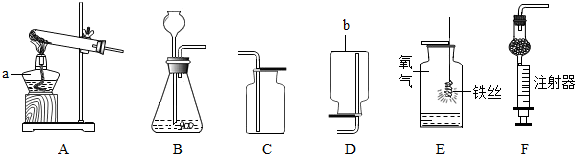
【进行实验1】同学们设计了如图所示装置并进行实验.
【进行实验2】同学们进行了下面的4个实验,每天观察一次现象,一段时间后,发现只有实验4中的铜丝生锈了,且与水接触的部分生锈更明显.
0 145578 145586 145592 145596 145602 145604 145608 145614 145616 145622 145628 145632 145634 145638 145644 145646 145652 145656 145658 145662 145664 145668 145670 145672 145673 145674 145676 145677 145678 145680 145682 145686 145688 145692 145694 145698 145704 145706 145712 145716 145718 145722 145728 145734 145736 145742 145746 145748 145754 145758 145764 145772 211419

探究活动一:验证铜锈的组成
【査阅资料】①铜锈为绿色,其主要成分是Cu2(OH)2CO3.②白色的硫酸铜粉末遇水能变为蓝色.③碳不与稀硫酸反应.④氧化铜为黑色固体,能与稀硫酸反应生成硫酸铜溶液.
【进行实验1】同学们设计了如图所示装置并进行实验.
| 实验橾作 | 实验现象 | 实验结论 |
| ①按如图组装仪器,装入药品. ②加热铜锈,直至不再有气体产生,停止加热. | 绿色固体变为黑色;硫酸铜粉末变为蓝色;烧杯中液体变浑浊. | 加热铜锈生成的物质有 CO2、H2O、CuO;铜绣由Cu、C、H、O元素组成;烧杯中发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O. |
| ③冷却后,向试管中固体 加入适量稀硫酸,稍加热. | 黑色固体溶解,溶液变 为蓝色. |
| 序号 | 实验内容 | 实验结论 | 实验反思 |
| 实验1 | 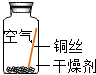 | 在干燥环境中,铜不易生锈 | (1)实验2和3中使用的是经煮沸后迅速冷却的蒸馏水,其原因是 除去蒸馏水中溶解的O2和CO2. (2)如果要证明铜生锈的快慢是否与二氧化碳的浓度有关,还需要补充的一个实验内容是 按实验4内容重复操作后,再通入一定量的CO2排出部分空气,塞紧胶塞. |
| 实验2 | 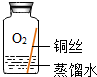 | 在有O2和H2O、无CO2的环境中,铜不易生锈 | |
| 实验3 | 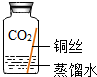 | 在有CO2和H2O、无O2的环境中,铜不易生锈 | |
| 实验4 | 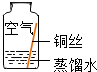 | 铜生锈的条件是 与O2、CO2和H2O同时接触 |
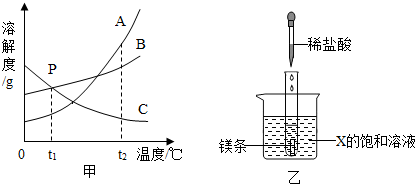
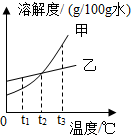 甲、乙两种物质的溶解度曲线如图所示.
甲、乙两种物质的溶解度曲线如图所示. 请根据所学知识回答下列问题.
请根据所学知识回答下列问题.