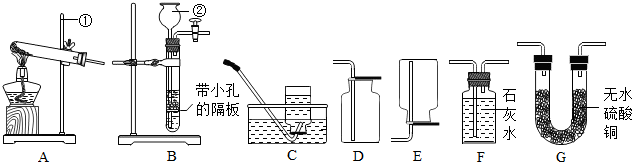
2.学习化学后,我们学会了从微观角度认识物质,已知碳原子和氧原子的结构示意图分别为: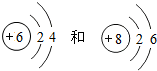 两种原子中相等的是( )
两种原子中相等的是( )
 两种原子中相等的是( )
两种原子中相等的是( )| A. | 质子数 | B. | 电子数 | C. | 第一层电子数 | D. | 第二层电子数 |
1.钢铁是使用最多的金属材料,下列说法中不正确的是( )
| A. | 生铁和钢属于含碳量不同的两种铁合金 | |
| B. | 地壳中含量最高的金属元素是铁 | |
| C. | 生铁比纯铁硬 | |
| D. | 不锈钢抗腐蚀性能也比纯铁好得多 |
20.在一定条件下,将二氧化碳气体压缩成干冰,这是因为( )
| A. | 分子之间有间隔 | B. | 分子可以再分 | ||
| C. | 分子在不断运动 | D. | 分子体积可以变小 |
19.下列变化中属于化学变化的是( )
| A. | 钢铁生锈 | B. | 轮胎爆裂 | C. | 海水晒盐 | D. | 风力发电 |
18.乙醇俗称酒精,常用作酒精灯、火锅等的燃料,下列有关性质中属于化学性质的是( )
| A. | 无色液体 | B. | 挥发性 | C. | 可燃性 | D. | 与水能互溶 |
17.今后五年,河北加快推进美丽乡村建设,下列措施中,我们不应采取的是( )
| A. | 做好房前屋后绿化 | B. | 推广清洁燃料炉具 | ||
| C. | 积极推进污水处理 | D. | 将垃圾集中焚烧 |
16.下列图片中利用了物质的物理性质的是( )
| A. |  燃烧 | B. |  放烟花 | C. |  用铜丝作导线 | D. |  酿酒 |
15.同学们对制作糕点常用膨松剂Na2CO3或NaHCO3进行了下列探究.
【查阅资料】
【探究一】NaHCO3和Na2CO3性质差异的探究
(1)现有20℃时溶质质量分数为8%的Na2CO3和NaHCO3溶液
酸碱性:取样于试管中,分别滴加紫色石蕊试液,均显蓝色;
酸碱度:NaHCO3溶液<Na2CO3溶液(填“>”或”“<”).
(2)稳定性:按图1,实验中可观察乙烧杯中的石灰水变浑浊,对应试管中发生反应的化学方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
结论:在受热条件下,碳酸钠比碳酸氢钠稳定性强(填“强”或“弱”).
(3)利用溶解度鉴别NaHCO3和Na2CO3:分别取Xg两种固体粉末加入20℃,10g水中充分溶解,通过观察溶解现象来区分,X可以是下列的A.(选填A、B或C)
A.2g B.0.96g C.0.5g
【问题讨论】
(4)实验结束时,应先B(选填A或B).
A.熄灭酒精灯 B.将甲、乙烧杯移开
(5)甲认为探究稳定性实验中,由于受热时两物质温度不同,不能得到(2)中的结论,经对装置设计讨论后一致认为可以得到上述结论,理由是加热时碳酸钠的温度比碳酸氢钠温度高.
【探究二】测定NaHCO3和Na2CO3混合物10.0g中NaHCO3的质量分数(图2,夹持装置略)
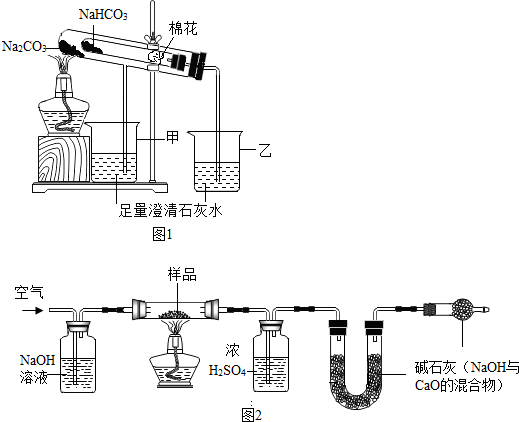
【问题讨论】
(6)实验前先通一段时间的空气的目的是排尽装置内的空气(或二氧化碳);
(7)A的作用是吸收鼓入空气中的二氧化碳,若没有装置E,NaHCO3的质量分数测定结果会偏大(填“偏大”、“不变”或“偏小”).
(8)停止加热后,仍继续通入空气一段时间,目的是使反应生成的二氧化碳全部被D吸收.
【含量测定】
(9)测得装置D的质量实验前为122.2g,实验后为124.4g,计算该样品中NaHCO3的质量分数.(要有计算过程)
【知识拓展】
(10)向Na2CO3溶液中通入CO2气体可以生成NaHCO3,该反应的化学反应方程式为:Na2CO3+CO2+H2O═2NaHCO3.
0 145456 145464 145470 145474 145480 145482 145486 145492 145494 145500 145506 145510 145512 145516 145522 145524 145530 145534 145536 145540 145542 145546 145548 145550 145551 145552 145554 145555 145556 145558 145560 145564 145566 145570 145572 145576 145582 145584 145590 145594 145596 145600 145606 145612 145614 145620 145624 145626 145632 145636 145642 145650 211419
【查阅资料】
| 20℃ | 8%Na2CO3溶液 | 8%NaHCO3溶液 |
| pH | 10.6 | 8.0 |
| 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
(1)现有20℃时溶质质量分数为8%的Na2CO3和NaHCO3溶液
酸碱性:取样于试管中,分别滴加紫色石蕊试液,均显蓝色;
酸碱度:NaHCO3溶液<Na2CO3溶液(填“>”或”“<”).
(2)稳定性:按图1,实验中可观察乙烧杯中的石灰水变浑浊,对应试管中发生反应的化学方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
结论:在受热条件下,碳酸钠比碳酸氢钠稳定性强(填“强”或“弱”).
(3)利用溶解度鉴别NaHCO3和Na2CO3:分别取Xg两种固体粉末加入20℃,10g水中充分溶解,通过观察溶解现象来区分,X可以是下列的A.(选填A、B或C)
A.2g B.0.96g C.0.5g
【问题讨论】
(4)实验结束时,应先B(选填A或B).
A.熄灭酒精灯 B.将甲、乙烧杯移开
(5)甲认为探究稳定性实验中,由于受热时两物质温度不同,不能得到(2)中的结论,经对装置设计讨论后一致认为可以得到上述结论,理由是加热时碳酸钠的温度比碳酸氢钠温度高.
【探究二】测定NaHCO3和Na2CO3混合物10.0g中NaHCO3的质量分数(图2,夹持装置略)

【问题讨论】
(6)实验前先通一段时间的空气的目的是排尽装置内的空气(或二氧化碳);
(7)A的作用是吸收鼓入空气中的二氧化碳,若没有装置E,NaHCO3的质量分数测定结果会偏大(填“偏大”、“不变”或“偏小”).
(8)停止加热后,仍继续通入空气一段时间,目的是使反应生成的二氧化碳全部被D吸收.
【含量测定】
(9)测得装置D的质量实验前为122.2g,实验后为124.4g,计算该样品中NaHCO3的质量分数.(要有计算过程)
【知识拓展】
(10)向Na2CO3溶液中通入CO2气体可以生成NaHCO3,该反应的化学反应方程式为:Na2CO3+CO2+H2O═2NaHCO3.