5. 在元素周期表中,硫元素的信息如图所示,下列从图中获得的信息错误的是( )
在元素周期表中,硫元素的信息如图所示,下列从图中获得的信息错误的是( )
 在元素周期表中,硫元素的信息如图所示,下列从图中获得的信息错误的是( )
在元素周期表中,硫元素的信息如图所示,下列从图中获得的信息错误的是( )| A. | 在硫元素的核外电子排布中a=2,b=8 | |
| B. | 硫原子在化学反应中易获得2个电子变成S2+ | |
| C. | 硫原子里,质子数=中子数=电子数=16 | |
| D. | 一个硫原子的相对原子质量是32.06克 |
3.我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如下),崔进了世界制碱技术的发展.下列有关说法:①沉淀池中的反应物共含有六种元素②过滤得到的“母液”中一定只含有两种溶质③图中X可能是氨气④通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀,正确的是( )


| A. | ①②④ | B. | ①③④ | C. | ①④ | D. | ②③ |
2.为探究影响双氧水分解速度的某种因素,记录了如下实验数据:
【数据处理及结论】
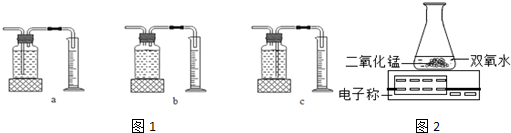
(1)本实验中,测量O2体积的装置是C(选填图1中的装置编号).
(2)实验结论:在相同条件下,双氧水浓度越大,双氧水分解速率越快.
(3)C小组用如图2装置进行实验,通过比较相同时间天平读数差值大小也能达到实验目的.
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2的体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |
(1)本实验中,测量O2体积的装置是C(选填图1中的装置编号).
(2)实验结论:在相同条件下,双氧水浓度越大,双氧水分解速率越快.
(3)C小组用如图2装置进行实验,通过比较相同时间天平读数差值大小也能达到实验目的.

1.实验盒中有7种没有标签的溶液,老师让化学实验小组同学鉴别这些溶液.
(1)调查研究
①实验盒中记录单上登记的7种溶液是:KMnO4、Na2CO3、CuSO4、NaCl、Ca(OH)2、NaOH和稀盐酸,其中有颜色的是KMnO4、CuSO4溶液.
②查阅资料:无色有刺激性气味的氯化氢气体溶于水得到盐酸.
③研究方式:从5种无色溶液中任意取出4种为一组进行鉴别.这样的组合共有四组.
(2)提出假设:同学们从5种无色溶液中取出4种,贴上A、B、C、D标签,并且假设这一组溶液可能是Na2CO3、NaCl、Ca(OH)2和稀盐酸.
(3)实验探究:同学们按以下步骤进行鉴别.
第一步:取4支试管,分别加入少量的A、B、C、D溶液,然后依次加入少稀盐酸,实验现象记录如下:
实验结论:C是Na2CO3溶液.
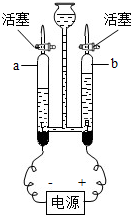
第二步:依据如图1装置进行实验,其中夹持固定装置已略去.从长颈漏斗加入稀盐酸,可以观察到C溶液中有气泡产生,A溶液中有白色沉淀生成,B、D溶液均无明显变化.

实验解释:A溶液中发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O.
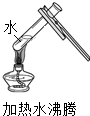
第三步:依据如图2装置进行2个实验.取少量B溶液倒入蒸发皿,加热,闻到有刺激性气味,停止加热.再取少量D溶液倒入另一蒸发皿,加热,有白色固体析出,停止加热.
实验结论:B是稀盐酸,D是NaCl溶液.
经过上述三步实验,同学们认为第5种无色溶液是NaOH溶液.
(4)实验反思:老师引导同学们讨论了上述实验探究过程,进行了全面反思.老师指出:实验结论仍有不确定性.不能确定的是NaCl和NaOH溶液;其鉴别方法是取溶液加入酚酞试液,变红的是氢氧化钠溶液,不变色的是氯化钠溶液.
(1)调查研究
①实验盒中记录单上登记的7种溶液是:KMnO4、Na2CO3、CuSO4、NaCl、Ca(OH)2、NaOH和稀盐酸,其中有颜色的是KMnO4、CuSO4溶液.
②查阅资料:无色有刺激性气味的氯化氢气体溶于水得到盐酸.
③研究方式:从5种无色溶液中任意取出4种为一组进行鉴别.这样的组合共有四组.
(2)提出假设:同学们从5种无色溶液中取出4种,贴上A、B、C、D标签,并且假设这一组溶液可能是Na2CO3、NaCl、Ca(OH)2和稀盐酸.
(3)实验探究:同学们按以下步骤进行鉴别.
第一步:取4支试管,分别加入少量的A、B、C、D溶液,然后依次加入少稀盐酸,实验现象记录如下:
| 溶液 | A | B | C | D |
| 加入盐酸后的现象 | 无明显变化 | 无明显变化 | 有气泡产生 | 无明显变化 |
第二步:依据如图1装置进行实验,其中夹持固定装置已略去.从长颈漏斗加入稀盐酸,可以观察到C溶液中有气泡产生,A溶液中有白色沉淀生成,B、D溶液均无明显变化.

实验解释:A溶液中发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O.
第三步:依据如图2装置进行2个实验.取少量B溶液倒入蒸发皿,加热,闻到有刺激性气味,停止加热.再取少量D溶液倒入另一蒸发皿,加热,有白色固体析出,停止加热.
实验结论:B是稀盐酸,D是NaCl溶液.
经过上述三步实验,同学们认为第5种无色溶液是NaOH溶液.
(4)实验反思:老师引导同学们讨论了上述实验探究过程,进行了全面反思.老师指出:实验结论仍有不确定性.不能确定的是NaCl和NaOH溶液;其鉴别方法是取溶液加入酚酞试液,变红的是氢氧化钠溶液,不变色的是氯化钠溶液.
20.下列4个图象分别表示4个实验过程中某些物质量的变化,其中正确的是( )
| A. | 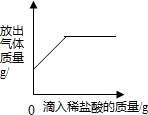 向一定量的石灰石中滴加稀盐酸 | |
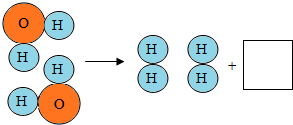
| B. |  向一定量过氧化氢溶液中加入少量二氧化锰 | |
| C. | 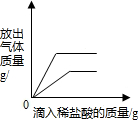 向相同质量的铁粉和锌粉中分别加入足量稀盐酸 | |
| D. |  向一定量硫酸铜溶液中不断加入铁粉 |
19.每年中招体育加试期间同学爱喝含有牛磺酸(C2H7NO3S)饮料以缓解肌肉和神经疲劳,下列关于牛磺酸的说法正确的( )
| A. | 牛磺酸中共有5种元素 | B. | 化合物中O、S元素的质量比为3:1 | ||
| C. | 牛磺酸分子中含有7个氢原子 | D. | 牛磺酸中含有臭氧(O3)分子 |
18.写出除去下列各物质中的杂质所用的试剂及相应的化学方程式(括号内为杂质)
0 145364 145372 145378 145382 145388 145390 145394 145400 145402 145408 145414 145418 145420 145424 145430 145432 145438 145442 145444 145448 145450 145454 145456 145458 145459 145460 145462 145463 145464 145466 145468 145472 145474 145478 145480 145484 145490 145492 145498 145502 145504 145508 145514 145520 145522 145528 145532 145534 145540 145544 145550 145558 211419
| 混合物 | 所用试剂 | 化学方程式 |
| FeSO4溶液(CuSO4) | 铁粉 | Fe+CuSO4═FeSO4+Cu |
| NaCl(Na2CO3) | 稀盐酸 | Na2CO3+2HCl═2NaCl+H2O+CO2↑ |


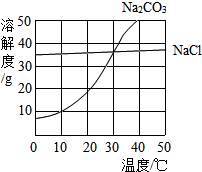 如图为氯化钠、碳酸钠在水中的溶解度曲线,请回答下列问题:
如图为氯化钠、碳酸钠在水中的溶解度曲线,请回答下列问题: