15.由硫酸钠和硫酸钙组成的混合物中,测知氧元素的质量分数为46%.若再计算混合物中的下列各项:①硫元素的质量分数 ②钠元素的质量分数 ③硫酸钙的质量分数 ④硫酸钠的质量 ⑤硫酸钠和硫酸钙的质量比 ⑥钙元素和钠元素的总质量;以下判断正确的是( )
| A. | 都能确定 | B. | 都不能确定 | ||
| C. | 除④和⑥外都能确定 | D. | 只有①和⑤能确定 |
14. 如图是某化学反应的微观模拟图,其中
如图是某化学反应的微观模拟图,其中
“ ”和“
”和“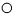 ”分别表示两种质子数不同的原子,a、b分别表示反应前和反应后的物质.下列判断正确的是( )
”分别表示两种质子数不同的原子,a、b分别表示反应前和反应后的物质.下列判断正确的是( )
 如图是某化学反应的微观模拟图,其中
如图是某化学反应的微观模拟图,其中“
 ”和“
”和“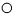 ”分别表示两种质子数不同的原子,a、b分别表示反应前和反应后的物质.下列判断正确的是( )
”分别表示两种质子数不同的原子,a、b分别表示反应前和反应后的物质.下列判断正确的是( )| A. | 该反应既不是分解反应也不是化合反应 | |
| B. | 该反应中白球表示的元素化合价不一定改变 | |
| C. | 该反应可能是表示的水的电解 | |
| D. | 该反应中反应物的分子个数比为2:3 |
13.A、B、C三种物质各15g,它们化合时只能生成30g新物质D;若增加10gA,则反应停止后,原反应物中只剩下C.下列说法正确的是( )
| A. | 第一次反应停止后,B剩余9g | B. | 第二次反应后,C的质量为10g | ||
| C. | 反应中A和B的质量比为3:2 | D. | 第二次反应消耗的C的质量为4g |
12.下列有关说法正确的是( )
| A. | 经过静止沉淀、过滤、活性炭吸附可以大大降低水的硬度 | |
| B. | 离子变成原子后,最外层电子数和电子层数一定会改变 | |
| C. | 由不同种元素组成的物质是化合物 | |
| D. | 物质发生还原反应时,一定有元素的化合价发生改变 |
11.果糖大量存在于水果中,其分子的化学式为C6H12O6,下列说法不正确的是( )
| A. | 果糖是一种氧化物 | |
| B. | 果糖中氧元素的质量分数最大 | |
| C. | 果糖中碳、氢、氧元素质量比6:1:8 | |
| D. | 1个果糖分子由6个碳原子、12个氢原子、6个氧原子构成 |
10. 研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行研究,以下是他们探究的主要过程:
研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行研究,以下是他们探究的主要过程:
【假设】H2O2生成O2的快慢与催化剂种类有关
【实验方案】常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量MnO2和红砖粉,测量各生成一瓶(相同体积)O2所需要的时间.
【进行实验】如图是他们进行实验的装置图,气体发生装置中A仪器名称是:锥形瓶,此实验中B处宜采用的气体收集方法是:排水法.
【实验记录】
【结论】该探究过程得出的结论是相同条件下,H2O2生成O2的快慢与催化剂的种类有关.
【反思】H2O2在常温下分解缓慢,加入MnO2或红砖粉后反应明显加快,若要证明MnO2或红砖粉是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的质量和化学性质是否改变.
H2O2生成O2的快慢还与哪些因素有关?请你帮助他们继续探究.(只要求提出假设和实验方案)
【假设】H2O2生成O2的快慢与H2O2的质量分数有关.
【实验方案】同温下取2份质量相等,质量分数不同的H2O2溶液,分别加入质量相等的同种催化剂,测量收集一试管气体所需的时间.结果质量分数大的过氧化氢溶液生成的氧气快,先收集满.
你若还能提出新的合理的假设和实验方案
【假设】H2O2生成O2的快慢与温度有关.
【实验方案】取二份质量相等的同浓度的H2O2溶液,分别加入质量相等的同种催化剂,测量在不同温度下各收集一瓶气体所需的时间.
 研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行研究,以下是他们探究的主要过程:
研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行研究,以下是他们探究的主要过程:【假设】H2O2生成O2的快慢与催化剂种类有关
【实验方案】常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量MnO2和红砖粉,测量各生成一瓶(相同体积)O2所需要的时间.
【进行实验】如图是他们进行实验的装置图,气体发生装置中A仪器名称是:锥形瓶,此实验中B处宜采用的气体收集方法是:排水法.
【实验记录】
| 实验编号 | 1 | 2 |
| 反应物 | 6% H2O2 | 6% H2O2 |
| 催化剂 | 1g红砖粉 | 1g MnO2 |
| 时间 | 152s | 35s |
【反思】H2O2在常温下分解缓慢,加入MnO2或红砖粉后反应明显加快,若要证明MnO2或红砖粉是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的质量和化学性质是否改变.
H2O2生成O2的快慢还与哪些因素有关?请你帮助他们继续探究.(只要求提出假设和实验方案)
【假设】H2O2生成O2的快慢与H2O2的质量分数有关.
【实验方案】同温下取2份质量相等,质量分数不同的H2O2溶液,分别加入质量相等的同种催化剂,测量收集一试管气体所需的时间.结果质量分数大的过氧化氢溶液生成的氧气快,先收集满.
你若还能提出新的合理的假设和实验方案
【假设】H2O2生成O2的快慢与温度有关.
【实验方案】取二份质量相等的同浓度的H2O2溶液,分别加入质量相等的同种催化剂,测量在不同温度下各收集一瓶气体所需的时间.
9.小明参观某养鱼池时,好奇的发现农民向养鱼池中撒一种叫做过氧化钙的淡黄色固体,用来增加鱼池中的含氧量.小明刚学完氧气的实验室制法,于是他想可否用过氧化钙来制取氧气呢?
【提出问题】过氧化钙可否用于制取氧气?
【查阅资料】过氧化钙(CaO2)室温下稳定,在300℃时分解成氧气,可做增氧剂、杀菌剂等.
【猜想与论证】(1)小明依据化学反应前后元素的种类不变,提出猜想Ⅰ:加热过氧化钙可制取氧气.
实验结论:加热过氧化钙可制取氧气.
(2)小明联想到农民用过氧化钙增加鱼池中的含氧量,提出猜想Ⅱ.
猜想Ⅱ:过氧化钙与水反应可制取氧气.
实验结论:不能用过氧化钙与水反应制取氧气.
分析与反思:
①虽然没有快速收集到大量氧气,但由此实验现象,小明认为农民用过氧化钙做增氧剂的主要原因是过氧化钙在水中持续、缓慢放出氧气,所以可以作为增氧剂.
②小明希望对此实验进行改进,使该反应加快,你能帮他提出建议吗?
你的合理建议:加热过氧化钙和水的混合物(或向过氧化钙和水的混合物中加入催化剂).以上建议是否可行,还需进一步通过实验验证.
0 145324 145332 145338 145342 145348 145350 145354 145360 145362 145368 145374 145378 145380 145384 145390 145392 145398 145402 145404 145408 145410 145414 145416 145418 145419 145420 145422 145423 145424 145426 145428 145432 145434 145438 145440 145444 145450 145452 145458 145462 145464 145468 145474 145480 145482 145488 145492 145494 145500 145504 145510 145518 211419
【提出问题】过氧化钙可否用于制取氧气?
【查阅资料】过氧化钙(CaO2)室温下稳定,在300℃时分解成氧气,可做增氧剂、杀菌剂等.
【猜想与论证】(1)小明依据化学反应前后元素的种类不变,提出猜想Ⅰ:加热过氧化钙可制取氧气.
| 实验装置 | 实验主要过程 |
 | ①检验装置气密性.操作如下:想将导管伸入液面下,用手紧握试管,观察到导管口有气泡冒出,松开后,有液体进入导管. ②加入过氧化钙,加热,导管口有大量气泡冒出.加热时应先均匀预热,然后集中在药品处加热 ③收集一瓶气体.生成的气体可用排水法收集,原因是氧气不易溶于水, ④停止加热.熄灭酒精灯前,应将导管从水槽中取出. ⑤检验气体.方法是将带火星的木条放在瓶口,若木条复燃,则是氧气. |
(2)小明联想到农民用过氧化钙增加鱼池中的含氧量,提出猜想Ⅱ.
猜想Ⅱ:过氧化钙与水反应可制取氧气.
| 实验装置 | 实验主要过程 |
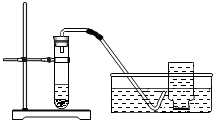 | ①检验装置气密性. ②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎看不到气体.该装置放置到第二天,集气瓶中只收集到极少量气体,震荡试管后仍有少量细小气泡缓慢放出,经检验该气体为氧气,该反应同时还生成氢氧化钙,写出该反应的符号表达式:2CaO2+2H2O=2Ca(OH)2+O2↑. |
分析与反思:
①虽然没有快速收集到大量氧气,但由此实验现象,小明认为农民用过氧化钙做增氧剂的主要原因是过氧化钙在水中持续、缓慢放出氧气,所以可以作为增氧剂.
②小明希望对此实验进行改进,使该反应加快,你能帮他提出建议吗?
你的合理建议:加热过氧化钙和水的混合物(或向过氧化钙和水的混合物中加入催化剂).以上建议是否可行,还需进一步通过实验验证.
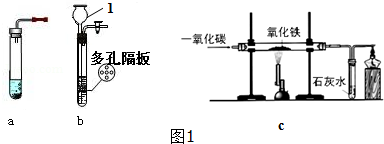 如图1所示装置制取氢气,试回答下列问题:
如图1所示装置制取氢气,试回答下列问题: