9.某石灰石厂实验室用5.55g石灰石样品高温煅烧对样品进行分析,实验数据记录如表(杂质不参与反应):
(1)完全反应后生成的CO2质量是2.2g.
(2)石灰石样品中碳酸钙的质量分数是多少?(写出计算过程,结果保留1%)
| 操作序号 | 1 | 2 | 3 | 4 |
| 剩余固体质量/(g) | 4.25 | 3.95 | 3.35 | 3.35 |
(2)石灰石样品中碳酸钙的质量分数是多少?(写出计算过程,结果保留1%)
8.精还原铁粉是一种重要的化工原料,某兴趣小组对其进行下列研究:
【物质制备】利用绿矾制备精还原铁粉的工艺流程如下:

粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式为:
FexOy+yH2$\frac{\underline{\;高温\;}}{\;}$3Fe+yH2O
Fe3C+2H2$\frac{\underline{\;高温\;}}{\;}$3Fe+CH4
(1)焙烧中加焦炭的作用:①制取CO;②提供热量.
(2)写出焙烧中氧化铁与CO反应的化学方程式:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
【含量测定】为得到精还原铁粉并测定粗还原铁粉中铁的氧化物组成及Fe3C的质量分数,取粗还原铁粉16g,并将其分为2等分,一份与足量的稀盐酸反应,得到氢气0.2g,另一份按如下装置进行实验.(假设每步反应都完全且不考虑装置内原有空气对测定结果的影响).
【资料卡】①3CH4+4Fe2O3 $\frac{\underline{\;高温\;}}{\;}$3CO2+6H2O+8Fe
②铁的氧化物及Fe3C均不能与稀盐酸反应产生H2
③浓硫酸的作用吸水,碱石灰吸水和二氧化碳

(3)写出装置中所指定仪器的名称:①硬质粗玻璃管;②铁架台.
(4)写出铁与稀盐酸反应的化学方程式:Fe+2HCl=FeCl2+H2↑.
(5)主要实验步骤如下:
①按顺序组装仪器,检查装置的气密性,精确称量样品和B、D、E装置的质量;②点燃A处酒精灯;③缓缓通入纯净干燥的H2;④点燃C处酒精灯;⑤分别熄灭A、C处酒精灯;⑥再缓缓通入少量H2;⑦再次精确称量样品及B、D、E装置的质量.
正确操作的先后顺序是①→③→④→②→⑤→⑥→⑦(填序号),否则,测定的Fe3C质量分数偏小(填“偏大”、“偏小”或“不变”).步骤③的目的是将装置中的空气排尽,防止点燃时发生爆炸,验证该步骤目的达到的实验方法是收集尾气验纯;步骤⑥的目的是防止生成的精还原铁粉在高温下又被氧化.
(6)经精确称量,实验样品及B、D、E装置反应前后质量的变化如表:
计算样品中Fe3C质量分数,应选用上表中的E组数据(填“D”或“E”),其理由是H2与Fe2O3反应也生成H2O,则Fe3C质量分数为11.25%(精确到0.01%).
(7)样品中铁的氧化物中,铁、氧元素的质量比是多少?(精确到0.01)(写出计算过程)
【物质制备】利用绿矾制备精还原铁粉的工艺流程如下:

粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式为:
FexOy+yH2$\frac{\underline{\;高温\;}}{\;}$3Fe+yH2O
Fe3C+2H2$\frac{\underline{\;高温\;}}{\;}$3Fe+CH4
(1)焙烧中加焦炭的作用:①制取CO;②提供热量.
(2)写出焙烧中氧化铁与CO反应的化学方程式:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
【含量测定】为得到精还原铁粉并测定粗还原铁粉中铁的氧化物组成及Fe3C的质量分数,取粗还原铁粉16g,并将其分为2等分,一份与足量的稀盐酸反应,得到氢气0.2g,另一份按如下装置进行实验.(假设每步反应都完全且不考虑装置内原有空气对测定结果的影响).
【资料卡】①3CH4+4Fe2O3 $\frac{\underline{\;高温\;}}{\;}$3CO2+6H2O+8Fe
②铁的氧化物及Fe3C均不能与稀盐酸反应产生H2
③浓硫酸的作用吸水,碱石灰吸水和二氧化碳

(3)写出装置中所指定仪器的名称:①硬质粗玻璃管;②铁架台.
(4)写出铁与稀盐酸反应的化学方程式:Fe+2HCl=FeCl2+H2↑.
(5)主要实验步骤如下:
①按顺序组装仪器,检查装置的气密性,精确称量样品和B、D、E装置的质量;②点燃A处酒精灯;③缓缓通入纯净干燥的H2;④点燃C处酒精灯;⑤分别熄灭A、C处酒精灯;⑥再缓缓通入少量H2;⑦再次精确称量样品及B、D、E装置的质量.
正确操作的先后顺序是①→③→④→②→⑤→⑥→⑦(填序号),否则,测定的Fe3C质量分数偏小(填“偏大”、“偏小”或“不变”).步骤③的目的是将装置中的空气排尽,防止点燃时发生爆炸,验证该步骤目的达到的实验方法是收集尾气验纯;步骤⑥的目的是防止生成的精还原铁粉在高温下又被氧化.
(6)经精确称量,实验样品及B、D、E装置反应前后质量的变化如表:
| 样品 | B | D | E | |
| 反应前 | 8g | 350g | 350g | 220g |
| 反应后 | 7.553g | 350.435g | 351.98g | 220.22g |
(7)样品中铁的氧化物中,铁、氧元素的质量比是多少?(精确到0.01)(写出计算过程)
6.镁将成为21世纪重要的轻型环保材料,我国含有非常丰富的镁资源.
(1)占地球表面积7O%的海洋是天然的镁元素宝库,从海水中提取镁的流程如下:
海水中的MgCl2$→_{过滤、洗涤}^{熟石灰}$Mg(OH)2$→_{蒸发、浓缩、结晶}^{盐酸}$MgCl2•6H2O$\stackrel{脱水}{→}$MgCl2$\stackrel{通电}{→}$Mg
其中在进行过滤操作时除用到玻璃棒,还用到的玻璃仪器有烧杯、漏斗.
(2)燃烧不一定需要氧气参加.金属镁是一种较活泼金属,在氮气中燃烧生成一种淡黄色固体--氮化镁,其中氮元素的化合价为-3,氮化镁的化学式为Mg3N2.
金属镁在二氧化碳气体中燃烧生成一种白色固体和一种黑色固体.该黑色固体不溶于水和盐酸,但能在氧气中燃烧而成为气体,该黑色固体的化学式为C.金属镁在二氧化碳气体中燃烧的反应类型属于.
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
若白色固体为纯净物,其成分有两种可能,你的猜想是:①MgO,②MgCO3.
请你设计一种证明白色固体成分的最简单易行的得实验方法:
(1)占地球表面积7O%的海洋是天然的镁元素宝库,从海水中提取镁的流程如下:
海水中的MgCl2$→_{过滤、洗涤}^{熟石灰}$Mg(OH)2$→_{蒸发、浓缩、结晶}^{盐酸}$MgCl2•6H2O$\stackrel{脱水}{→}$MgCl2$\stackrel{通电}{→}$Mg
其中在进行过滤操作时除用到玻璃棒,还用到的玻璃仪器有烧杯、漏斗.
(2)燃烧不一定需要氧气参加.金属镁是一种较活泼金属,在氮气中燃烧生成一种淡黄色固体--氮化镁,其中氮元素的化合价为-3,氮化镁的化学式为Mg3N2.
金属镁在二氧化碳气体中燃烧生成一种白色固体和一种黑色固体.该黑色固体不溶于水和盐酸,但能在氧气中燃烧而成为气体,该黑色固体的化学式为C.金属镁在二氧化碳气体中燃烧的反应类型属于.
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
若白色固体为纯净物,其成分有两种可能,你的猜想是:①MgO,②MgCO3.
请你设计一种证明白色固体成分的最简单易行的得实验方法:
| 实验操作 | 实验现象 | 结论 |
| 取少许白色固体于试管中, 滴加少量稀盐酸. | 若有气泡冒出 若无气泡冒出 | 则白色固体为MgCO3 则白色固体为MgO |
4.马鞍山市今年进行“四城同创”,其中与我们化学密切相关的是( )
| A. | 提高市民的交通法规意识 | |
| B. | 垃圾分类回收,提高资源利用率 | |
| C. | 实现均衡教育,保护儿童受教育的权利 | |
| D. | 拥军爱民,提高国防意识 |
3.进行化学实验必须注意安全,下列做法符合实际的是( )
| A. | 不慎将浓硫酸沾到皮肤上,应立即用水冲洗,再涂上硼酸溶液 | |
| B. | 药品和仪器的存放应符合一定的规范,氢氧化钠溶液如图存放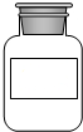 | |
| C. | 在实验室里可用品尝的办法区别食盐和蔗糖晶体 | |
| D. | 配制稀硫酸时,可先在烧杯中加入一定量的水,再慢慢注入浓硫酸并不断搅拌 |
2.下面是小强同学设计测定金属铁、铜、锌和银的活动性的探究实验过程和实验记录.
【实验目的】测定金属铁、铜、锌和镁的活动性强弱
【所用试剂】稀硫酸、硝酸锌溶液、硝酸银溶液、光亮的薄铁片、薄铜片、薄镁片
【实验过程】
步骤Ⅰ:将铁片、铜片、锌片分别放入三只盛有溶质质量分数相同、体积相同的稀硫酸的试管中;
步骤Ⅱ:将铁片、铜片、锌片分别放入三只盛有溶质质量分数相同、体积相同的硝酸锌溶液的试管中;
步骤Ⅲ:将铁片、铜片、锌片分别放入三只盛有溶质质量分数相同、体积相同的硝酸银溶液的试管中.
【实验记录】用“√”表示能观察到实验现象,用“-”表示观察不到实验现象(见如表).
(1)在上述步骤中,除了控制溶液的溶质质量分数和体积相同外,还应该控制的变量有金属的质量、形状.
(2)铁和稀硫酸反应的实验现象是有气泡产生,溶液由无色变成浅绿色,反应的化学方程式为Fe+H2SO4=FeSO4+H2↑,反应后溶液的质量变大(填“大”或“小”).实验室常用稀硫酸和锌粒反应制取氢气,不能用稀盐酸代替稀硫酸,原因是稀盐酸具有挥发性,制取的氢气不纯.请写出铜和硝酸银溶液反应的化学方程式Cu+2AgNO3=Cu(NO3)2+2Ag.
(3)四种金属的活动性顺序是锌、铁、铜、银,科学实验证明,大多数金属的化学性质比较活泼,原因是大多数都会与氧气反应.
(4)在金属活动性顺序中位置靠前的金属易失电子,给位于其后的金属阳离子.金属原子失去电子,具有还原性,失电子能力越强还原性越强;金属阳离子得到电子,具有氧化性,得电子能力越强氧化性越强.请写出Zn2+、Cu2+、Fe2+的氧化性强弱顺序Cu2+、Fe2+、Zn2+.
(5)钢铁的锈蚀主要是铁与空气中的氧气、水等物质发生化学反应的结果.铝的活动性比铁强,但生活中很少见到铝被腐蚀,原因是铝和空气中的氧气反应会生成致密的氧化铝薄膜.
【实验目的】测定金属铁、铜、锌和镁的活动性强弱
【所用试剂】稀硫酸、硝酸锌溶液、硝酸银溶液、光亮的薄铁片、薄铜片、薄镁片
【实验过程】
步骤Ⅰ:将铁片、铜片、锌片分别放入三只盛有溶质质量分数相同、体积相同的稀硫酸的试管中;
步骤Ⅱ:将铁片、铜片、锌片分别放入三只盛有溶质质量分数相同、体积相同的硝酸锌溶液的试管中;
步骤Ⅲ:将铁片、铜片、锌片分别放入三只盛有溶质质量分数相同、体积相同的硝酸银溶液的试管中.
【实验记录】用“√”表示能观察到实验现象,用“-”表示观察不到实验现象(见如表).
| 金属 | 空气 | 稀硫酸 | 硝酸银溶液 |
| 铁 | √ | - | √ |
| 铜 | - | - | √ |
| 镁 | √ | - | √ |
(2)铁和稀硫酸反应的实验现象是有气泡产生,溶液由无色变成浅绿色,反应的化学方程式为Fe+H2SO4=FeSO4+H2↑,反应后溶液的质量变大(填“大”或“小”).实验室常用稀硫酸和锌粒反应制取氢气,不能用稀盐酸代替稀硫酸,原因是稀盐酸具有挥发性,制取的氢气不纯.请写出铜和硝酸银溶液反应的化学方程式Cu+2AgNO3=Cu(NO3)2+2Ag.
(3)四种金属的活动性顺序是锌、铁、铜、银,科学实验证明,大多数金属的化学性质比较活泼,原因是大多数都会与氧气反应.
(4)在金属活动性顺序中位置靠前的金属易失电子,给位于其后的金属阳离子.金属原子失去电子,具有还原性,失电子能力越强还原性越强;金属阳离子得到电子,具有氧化性,得电子能力越强氧化性越强.请写出Zn2+、Cu2+、Fe2+的氧化性强弱顺序Cu2+、Fe2+、Zn2+.
(5)钢铁的锈蚀主要是铁与空气中的氧气、水等物质发生化学反应的结果.铝的活动性比铁强,但生活中很少见到铝被腐蚀,原因是铝和空气中的氧气反应会生成致密的氧化铝薄膜.
1.化学就在我们身边:
(1)现有下列四种物质;a石油、b干冰、c熟石灰、d合成橡胶、e汞、f尿素
请选择相应的物质用序号填空:
①可做汽车轮胎的材料是合成橡胶 ②温度计中填充的液态金属是汞
③可作氮肥的是尿素 ④被称为“工业的血液”的化石燃料是石油
⑤可用作人工降雨的是干冰⑥可用作改良酸性土壤的是熟石灰
(2)优质方便面的品质不仅仅是口感问题,还包括较高的营养指标.下表是某一方便面的营养成分表.试回答问题.
①方便面所含的营养素主要有蛋白质、糖类、油脂、无机盐和水.
②表中可知方便面内不含维生素C,为了补充 维生素C,平时应该多吃水果和蔬菜.
(3)H7N9禽流感病毒在4℃水中可存活1个月,在pH=4的条件下具有一定的存活能力.在100℃水中一分钟可被消灭.2013年4月5日抗流感新药帕拉米韦(化学式:C15H28 N4O4)氯化钠注射液临床试验效果较好.
①帕拉米韦属于(填字母,下同):有机物; A.氧化物 B.混合物 C.有机物
②下列能测出溶液pH=4的是C. A.酚酞试液 B.石蕊试液 C.PH试纸
(4)A物质常用于焊接或切割金属.把一定质量的纯净物A和40g的纯净物B在-定条件下按下图所示充分反应,当B物质反应完时,可生成44g C物质和9g D物质.
①参加反应的A物质的质量是13g. ②A物质中各元素的质量比为12:1.

0 145259 145267 145273 145277 145283 145285 145289 145295 145297 145303 145309 145313 145315 145319 145325 145327 145333 145337 145339 145343 145345 145349 145351 145353 145354 145355 145357 145358 145359 145361 145363 145367 145369 145373 145375 145379 145385 145387 145393 145397 145399 145403 145409 145415 145417 145423 145427 145429 145435 145439 145445 145453 211419
(1)现有下列四种物质;a石油、b干冰、c熟石灰、d合成橡胶、e汞、f尿素
请选择相应的物质用序号填空:
①可做汽车轮胎的材料是合成橡胶 ②温度计中填充的液态金属是汞
③可作氮肥的是尿素 ④被称为“工业的血液”的化石燃料是石油
⑤可用作人工降雨的是干冰⑥可用作改良酸性土壤的是熟石灰
(2)优质方便面的品质不仅仅是口感问题,还包括较高的营养指标.下表是某一方便面的营养成分表.试回答问题.
| 方便面营养成分表(每100g中含量) | |||||||||
| 糖类(g) | 脂肪(g) | 蛋白质(g) | 水分(g) | 钠(mg) | 钾(mg) | 磷(mg) | 钙(mg) | 维生素C(mg) | 其他 |
| 61.6 | 21.1 | 9.5 | 3.6 | 1144 | 134 | 80 | 25 | 0 | … |
②表中可知方便面内不含维生素C,为了补充 维生素C,平时应该多吃水果和蔬菜.
(3)H7N9禽流感病毒在4℃水中可存活1个月,在pH=4的条件下具有一定的存活能力.在100℃水中一分钟可被消灭.2013年4月5日抗流感新药帕拉米韦(化学式:C15H28 N4O4)氯化钠注射液临床试验效果较好.
①帕拉米韦属于(填字母,下同):有机物; A.氧化物 B.混合物 C.有机物
②下列能测出溶液pH=4的是C. A.酚酞试液 B.石蕊试液 C.PH试纸
(4)A物质常用于焊接或切割金属.把一定质量的纯净物A和40g的纯净物B在-定条件下按下图所示充分反应,当B物质反应完时,可生成44g C物质和9g D物质.
①参加反应的A物质的质量是13g. ②A物质中各元素的质量比为12:1.

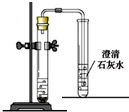 小明在实验操作考试中的考题是:二氧化碳的制取与性质.
小明在实验操作考试中的考题是:二氧化碳的制取与性质.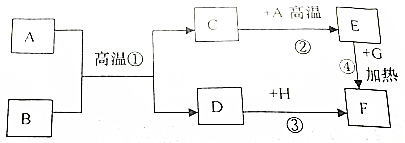 A一H是初中化学常见的物质,已知A为黑色固体单质,B为红棕色粉末,C和E的组成元素相同,G为黑色的固体化合物,F为红色固体单质,它们的转化关系如图所示,请回答:
A一H是初中化学常见的物质,已知A为黑色固体单质,B为红棕色粉末,C和E的组成元素相同,G为黑色的固体化合物,F为红色固体单质,它们的转化关系如图所示,请回答: