7.下列有关对质量守恒定律的理解,正确的是( )
| A. | 将100g冰加热变成100g的水,遵循质量守恒定律 | |
| B. | 5g硫和5g氧气完全反应后,生成物质量为10g | |
| C. | 化学反应前后分子的总数一定不会发生变化 | |
| D. | 镁条燃烧后质量增加,不遵循质量守恒定律 |
6.下列实验操作及现象结论正确的是( )
| A. | 将水慢慢注入盛有浓硫酸的量筒中进行稀释 | |
| B. | 浓硫酸能使纸张碳化变黑,说明浓硫酸具有脱水性 | |
| C. | 氢气还原氧化铜实验结束时,先停止通氢气再熄灭酒精灯 | |
| D. | 往溶液中加BaCl2溶液生成不溶于稀硝酸的白色沉淀,说明溶液中一定含SO42- |
5.有三种溶液:Ⅰ-FeCl2、Ⅱ-CuSO4、Ⅲ-Ca(NO3)2,拟用甲(银质容器);乙(铁质容器);丙(锌质容器)分别盛装三种溶液,则下列组合中最合适的是( )
| 组合编号 | 甲 | 乙 | 丙 |
| A | Ⅱ | Ⅰ | Ⅲ |
| B | Ⅰ | Ⅲ | Ⅱ |
| C | Ⅲ | Ⅱ | Ⅰ |
| D | Ⅱ | Ⅲ | Ⅰ |
| A. | A | B. | B | C. | C | D. | D |
2.探究金属镁、锌的活动性强弱
(1)请利用金属能与酸反应的性质,自选仪器和药品,探究金属镁、锌的活动性强弱,完成下列实验报告:
(2)写出上述反应中镁与酸反应的化学反应方程式Mg+2HCl═MgCl2+H2↑,该反应属于基本反应类型中的置换反应,反应的实质是镁原子失去电子变成镁离子,氢离子得到电子变成氢原子,氢原子结合成为氢分子.
(3)从原子结构的角度分析,金属原子在化学反应变化中都容易失去电子是因为最外层电子数小于4,容易失去电子,但是不同原子失去电子的能力不同,因此金属的活动性不同.
(1)请利用金属能与酸反应的性质,自选仪器和药品,探究金属镁、锌的活动性强弱,完成下列实验报告:
| 实验步骤 | 实验现象 | 实验结论 |
| 镁比锌活泼 |
(3)从原子结构的角度分析,金属原子在化学反应变化中都容易失去电子是因为最外层电子数小于4,容易失去电子,但是不同原子失去电子的能力不同,因此金属的活动性不同.
4.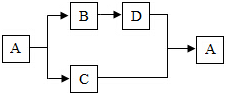 A~D都是初中科学中的常见物质,且有如图所示转化关系.若A在常温下是一种无色液体,B转化为D发生的是化合反应,则符合上述要求的D可能是( )
A~D都是初中科学中的常见物质,且有如图所示转化关系.若A在常温下是一种无色液体,B转化为D发生的是化合反应,则符合上述要求的D可能是( )
 A~D都是初中科学中的常见物质,且有如图所示转化关系.若A在常温下是一种无色液体,B转化为D发生的是化合反应,则符合上述要求的D可能是( )
A~D都是初中科学中的常见物质,且有如图所示转化关系.若A在常温下是一种无色液体,B转化为D发生的是化合反应,则符合上述要求的D可能是( )| A. | SO3 | B. | Fe(OH)3 | C. | MgO | D. | CuO |
2.下列物质转化不能一步实现的是 ( )
0 145232 145240 145246 145250 145256 145258 145262 145268 145270 145276 145282 145286 145288 145292 145298 145300 145306 145310 145312 145316 145318 145322 145324 145326 145327 145328 145330 145331 145332 145334 145336 145340 145342 145346 145348 145352 145358 145360 145366 145370 145372 145376 145382 145388 145390 145396 145400 145402 145408 145412 145418 145426 211419
| A. | Ca(OH)2→NaOH | B. | CO2→Na2CO3 | C. | FeCl3→Fe(OH)3 | D. | CaCO3→Ca(OH)2 |

