17.某化学兴趣小组对课本介绍的三种金属Mg、Ti(钛)、Cu的金属活动性进行探究.
[提出假设]a:Ti金属活动性比镁强,b:Mg金属活动性比Cu强
[查阅资料]在相同条件下,金属与酸反应,产生气泡的速度越快,则该金属活动性越强.
[实验设计]同温下,取质量相同的这三种金属薄片,分别投入等体积等浓度的足量的稀盐酸中反应,观察现象.
[回答问题](1)三种金属加入盐酸前都先用砂布将表片擦亮,其目的是A.
A.除去氧化膜,利于直接反应 B.使表面不平整,易反应
C.使表面光亮,易观察现象 D.使反应温度相同,易反应
(2)填写下表中的有关现象和结论:
(3)探究结束后,小涛同学说我还有其它办法也能得出三种金属在金属活动顺序中的相对位置关系,他选用了三种药品进行实验,则他选用的三种药品可能是Mg、TiSO4 、Cu.
[总结与归纳]由上述试验得出比较金属活动性强弱的方法有:
①通过金属与酸反应比较;②通过金属与盐溶液反应比较.
[提出假设]a:Ti金属活动性比镁强,b:Mg金属活动性比Cu强
[查阅资料]在相同条件下,金属与酸反应,产生气泡的速度越快,则该金属活动性越强.
[实验设计]同温下,取质量相同的这三种金属薄片,分别投入等体积等浓度的足量的稀盐酸中反应,观察现象.
[回答问题](1)三种金属加入盐酸前都先用砂布将表片擦亮,其目的是A.
A.除去氧化膜,利于直接反应 B.使表面不平整,易反应
C.使表面光亮,易观察现象 D.使反应温度相同,易反应
(2)填写下表中的有关现象和结论:
| Ti | Mg | Cu | |
| 与盐酸反应现象 | 放出气泡速度缓慢 | 放出气泡速度快 | 无现象 |
| 结论 | 原假设中a不正确(填“a”、“b”、“a b”)理由是钛与盐酸反应放出气泡速度缓慢,镁与盐酸反应放出气泡速度快;三种金属的活动性顺序为Mg>Ti>Cu. | ||
[总结与归纳]由上述试验得出比较金属活动性强弱的方法有:
①通过金属与酸反应比较;②通过金属与盐溶液反应比较.
16.某化学兴趣小组用火柴、蜡烛、烧杯三种实验材料探究物质燃烧的条件.
[提出问题]物质燃烧需要什么条件?
[猜想与假设]1.有可燃物 2.温度要达到着火点 3.与氧气(或空气)接触
[设计与实验]
[得出结论]猜想正确,燃烧必须同时满足上述3个条件,只要破坏1个燃烧的条件,就能达到灭火的目的.
[反思质疑门氢气在氯气中能燃烧.燃烧是否一定要有氧气参加?
[查阅资料1]镁条能在空气中剧烈燃烧,也能在二氧化碳中剧烈燃烧,发出耀眼的白光、放出大量的热;细铁丝可以在氯气中剧烈燃烧,放出大量的热,产生大量棕黄色的烟;磷能在氯气中剧烈燃烧,放出大量的热,产生大量的白色烟雾.
[表达与交流]根据上述内容和课本中对“燃烧”的描述,你认为发光、放热的剧烈的化学反应叫做燃烧.
[反思质疑2]根据“细铁丝在氧气中燃烧”的实验现象,细铁丝在氧气中燃烧为什么会“火星四射”?
[查阅资料2]含碳细铁丝燃烧时,其中的炭粒生成的CO2气体在熔融液态物质中形成气泡,熔融液态物质因气泡炸裂引起“火星四射”的现象.
[设计实验]为了验证细铁丝在纯氧中燃烧产生“火星四射”现象的原因,你设计的实验方案是取长短相等、粗细相同的含碳细铁丝和不含碳细铁丝,分别在足量的氧气中燃烧,观察实验现象.
[提出问题]物质燃烧需要什么条件?
[猜想与假设]1.有可燃物 2.温度要达到着火点 3.与氧气(或空气)接触
[设计与实验]
| 验证 | 对比实验 | |
| 假设1 | 示例:加热烧杯,烧杯不可燃 | (仿照示例填写)点燃蜡烛,蜡烛可燃 |
| 假设2 | 常温放置蜡烛,蜡烛不燃烧 | (仿照示例填写)点燃蜡烛,蜡烛燃烧 |
| 假设3 | 点燃蜡烛,蜡烛在空气中持续燃烧 | (仿照示例填写)将燃着的蜡烛扣入一只烧杯内,蜡烛逐渐熄灭 |
[反思质疑门氢气在氯气中能燃烧.燃烧是否一定要有氧气参加?
[查阅资料1]镁条能在空气中剧烈燃烧,也能在二氧化碳中剧烈燃烧,发出耀眼的白光、放出大量的热;细铁丝可以在氯气中剧烈燃烧,放出大量的热,产生大量棕黄色的烟;磷能在氯气中剧烈燃烧,放出大量的热,产生大量的白色烟雾.
[表达与交流]根据上述内容和课本中对“燃烧”的描述,你认为发光、放热的剧烈的化学反应叫做燃烧.
[反思质疑2]根据“细铁丝在氧气中燃烧”的实验现象,细铁丝在氧气中燃烧为什么会“火星四射”?
[查阅资料2]含碳细铁丝燃烧时,其中的炭粒生成的CO2气体在熔融液态物质中形成气泡,熔融液态物质因气泡炸裂引起“火星四射”的现象.
[设计实验]为了验证细铁丝在纯氧中燃烧产生“火星四射”现象的原因,你设计的实验方案是取长短相等、粗细相同的含碳细铁丝和不含碳细铁丝,分别在足量的氧气中燃烧,观察实验现象.
15.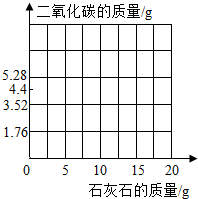 石灰石是我省的主要矿产之一.学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g,平均分成4份,进行实验,结果如下:
石灰石是我省的主要矿产之一.学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g,平均分成4份,进行实验,结果如下:
(1)上表中m的数值是4.4.
(2)所用盐酸溶液的溶质质量分数?
(3)在图中画出石灰石与生成二氧化碳的关系图
(4)某同学计算碳酸钙的质量分数过程如下:
设15克石灰石中碳酸钙的质量为x
根据化学方程式列关系式为:$\frac{100}{x}$=$\frac{44}{4.4g}$ 求得:x=10g,碳酸钙的质量分数为10g/15g×100%=66.7%,你认为正确么?如正确本题可不答,如不正确,请说明理由15g石灰石样品没有完全反应.
 石灰石是我省的主要矿产之一.学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g,平均分成4份,进行实验,结果如下:
石灰石是我省的主要矿产之一.学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g,平均分成4份,进行实验,结果如下:| 实验 | 1 | 2 | 3 | 4 |
| 加入样品的质量/g | 5 | 10 | 15 | 20 |
| 生成CO2的质量/g | 1.76 | 3.52 | 4.4 | m |
(2)所用盐酸溶液的溶质质量分数?
(3)在图中画出石灰石与生成二氧化碳的关系图
(4)某同学计算碳酸钙的质量分数过程如下:
设15克石灰石中碳酸钙的质量为x
根据化学方程式列关系式为:$\frac{100}{x}$=$\frac{44}{4.4g}$ 求得:x=10g,碳酸钙的质量分数为10g/15g×100%=66.7%,你认为正确么?如正确本题可不答,如不正确,请说明理由15g石灰石样品没有完全反应.
12.取一定质量的CaCO3高温加热一段时间后,冷却,测得剩余固体的质量为10.6g,剩余固体中碳元素的质量为0.6g,下列判断正确的是( )
| A. | 生成了2.2g CO2 | B. | 剩余CaCO3的质量为10.0g | ||
| C. | 生成了10.6g CaO | D. | 原来CaCO3的质量为15.0g |
11.为证明“二氧化锰是过氧化氢分解的催化剂”,小明同学设计了一下实验方案:
实验1:准确称取少量二氧化锰装入试管,把带火星的木条伸入试管内,观察现象.
实验2:在上述试管中加入6mL10%过氧化氢溶液,把带火星的木条伸入试管内,观察现象.
实验3:待“实验2”的试管中没有现象发生时,重新加入6mL10%过氧化氢溶液,观察现象.
实验4:把“实验3”中的二氧化锰过滤出来,洗涤、烘干、称量.
请回答:
(1)“实验2”中观察到的现象是溶液中有大量气泡冒出,带火星木条复燃.
(2)“实验3”的实验目的是证明二氧化锰反应前后化学性质不变.
(3)小红同学认为以上实验方案不完整,还需要补充实验.请你把需要补充的实验的有关
内容填在下面实验报告的空格内.
0 145074 145082 145088 145092 145098 145100 145104 145110 145112 145118 145124 145128 145130 145134 145140 145142 145148 145152 145154 145158 145160 145164 145166 145168 145169 145170 145172 145173 145174 145176 145178 145182 145184 145188 145190 145194 145200 145202 145208 145212 145214 145218 145224 145230 145232 145238 145242 145244 145250 145254 145260 145268 211419
实验1:准确称取少量二氧化锰装入试管,把带火星的木条伸入试管内,观察现象.
实验2:在上述试管中加入6mL10%过氧化氢溶液,把带火星的木条伸入试管内,观察现象.
实验3:待“实验2”的试管中没有现象发生时,重新加入6mL10%过氧化氢溶液,观察现象.
实验4:把“实验3”中的二氧化锰过滤出来,洗涤、烘干、称量.
请回答:
(1)“实验2”中观察到的现象是溶液中有大量气泡冒出,带火星木条复燃.
(2)“实验3”的实验目的是证明二氧化锰反应前后化学性质不变.
(3)小红同学认为以上实验方案不完整,还需要补充实验.请你把需要补充的实验的有关
内容填在下面实验报告的空格内.
| 实验操作 | 实验现象 | 解释 |
| 取一支试管加入6mL10%的过氧化亲溶液,把带火星的木条伸入试管内,观察现象 | 带火星木条不复燃 | 常温下,过氧化氢溶液分解速率很慢,放出氧气很少,不足以使带火星的木条复燃 |

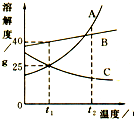 小明同学绘制了A、B、C三种固体物质的溶解度曲线如图.
小明同学绘制了A、B、C三种固体物质的溶解度曲线如图.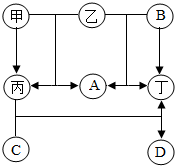 如右图A、B、C、D、甲、乙、丙、丁都是我们已学过的物质.(图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,部分反应物、生成物及反应条件已略去.)甲、乙、丙、丁均是氧化物,且乙是黑色固体.A、B是单质,D是石灰石的主要成分,且D和C的组成元素中有两种是相同的.
如右图A、B、C、D、甲、乙、丙、丁都是我们已学过的物质.(图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,部分反应物、生成物及反应条件已略去.)甲、乙、丙、丁均是氧化物,且乙是黑色固体.A、B是单质,D是石灰石的主要成分,且D和C的组成元素中有两种是相同的.