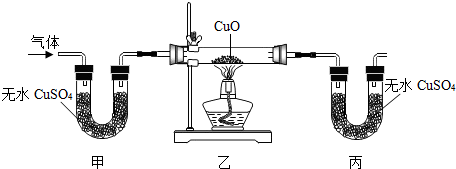
10.现有锻烧一段时间后的石灰石的样品,其质量是100g,将其充分锻烧后,得固体90g,将90g固体加入到足量的稀盐酸中,充分反应后过滤,得滤渣6g,则100g原固体中钙元素的质量分数是( )(杂质不和盐酸反应也不分解和溶解)
| A. | 60% | B. | 50% | C. | 48% | D. | 40% |
5.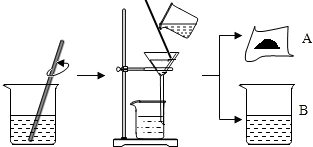 据有关资料介绍:将贝壳(主要成分是碳酸钙)灼烧后与草木灰(主要成分是碳酸钾)在水中作用,可以得到氢氧化钾.某科学课外小组的同学们为了制取氢氧化钾,将少量碳酸钙充分灼烧后的固体放入烧杯中,再向其中加入一定量10%的碳酸钾溶液,充分反应冷却后过滤、洗涤得到固体A和溶液B,操作步骤如图所示.请你与小组同学共同完成以下探究:
据有关资料介绍:将贝壳(主要成分是碳酸钙)灼烧后与草木灰(主要成分是碳酸钾)在水中作用,可以得到氢氧化钾.某科学课外小组的同学们为了制取氢氧化钾,将少量碳酸钙充分灼烧后的固体放入烧杯中,再向其中加入一定量10%的碳酸钾溶液,充分反应冷却后过滤、洗涤得到固体A和溶液B,操作步骤如图所示.请你与小组同学共同完成以下探究:
【提出问题1】固体A中的成分是什么?
【猜想与假设】甲同学:只有CaCO3;乙同学:CaCO3、Ca(OH)2
【实验与探究】甲、乙同学为了验证各自的猜想,分别进行了实验:
【反思与评价】小组同学讨论后认为,甲同学的实验不能证明他的猜想,理由是加入稀盐酸有气泡只能证明有碳酸钙,不能证明有无氢氧化钙;而乙同学的实验能证明他的猜想,因此小组同学确定了固体A的成分.
【提出问题2】溶液B中溶质的成分是什么?加入稀盐酸有气泡只能证明有碳酸钙,不能证明有无氢氧化钙
【猜想与假设】丙同学:KOH、K2CO3 丁同学:KOH、Ca(OH)2
【表达与交流】结合对固体成分的探究,同学们经过讨论确定了丁同学猜想正确,理由固体中含有氢氧化钙,说明溶液中的碳酸钾已完全反应.为了得到纯净的氢氧化钾,需要向溶液B中滴加适量的一种溶液,发生反应的化学方程式为K2CO3+Ca(OH)2═CaCO3↓+2KOH,小组同学通过相应的实验操作最终制得了氢氧化钾.
 据有关资料介绍:将贝壳(主要成分是碳酸钙)灼烧后与草木灰(主要成分是碳酸钾)在水中作用,可以得到氢氧化钾.某科学课外小组的同学们为了制取氢氧化钾,将少量碳酸钙充分灼烧后的固体放入烧杯中,再向其中加入一定量10%的碳酸钾溶液,充分反应冷却后过滤、洗涤得到固体A和溶液B,操作步骤如图所示.请你与小组同学共同完成以下探究:
据有关资料介绍:将贝壳(主要成分是碳酸钙)灼烧后与草木灰(主要成分是碳酸钾)在水中作用,可以得到氢氧化钾.某科学课外小组的同学们为了制取氢氧化钾,将少量碳酸钙充分灼烧后的固体放入烧杯中,再向其中加入一定量10%的碳酸钾溶液,充分反应冷却后过滤、洗涤得到固体A和溶液B,操作步骤如图所示.请你与小组同学共同完成以下探究:【提出问题1】固体A中的成分是什么?
【猜想与假设】甲同学:只有CaCO3;乙同学:CaCO3、Ca(OH)2
【实验与探究】甲、乙同学为了验证各自的猜想,分别进行了实验:
| 实验内容 | 实验现象 | 实验结论 |
| 甲同学:取少量固体于试管中,向其中加入稀盐酸. | 有气泡产生 | 自己的猜 想正确 |
| 乙同学:取少量固体于试管中,加水充分溶解、过滤,向滤液中滴加酚酞试液. | 溶液由无色 变为红色 | 自己的猜 想正确 |
【提出问题2】溶液B中溶质的成分是什么?加入稀盐酸有气泡只能证明有碳酸钙,不能证明有无氢氧化钙
【猜想与假设】丙同学:KOH、K2CO3 丁同学:KOH、Ca(OH)2
【表达与交流】结合对固体成分的探究,同学们经过讨论确定了丁同学猜想正确,理由固体中含有氢氧化钙,说明溶液中的碳酸钾已完全反应.为了得到纯净的氢氧化钾,需要向溶液B中滴加适量的一种溶液,发生反应的化学方程式为K2CO3+Ca(OH)2═CaCO3↓+2KOH,小组同学通过相应的实验操作最终制得了氢氧化钾.
4.某探究小组的同学用H2SO4、Na2CO3、NaOH、BaCl2四种溶液进行“复分解反应发生条件及应用”的实验探究.
(1)将四种溶液两两混合,若用H2SO4与另三种溶液分别混合:
①实验中,能直接观察到说明H2SO4与Na2CO3溶液发生化学反应的证据是:有气体产生.
②实验中的H2SO4与NaOH混合“无明显现象”,但实际上发生了化学反应,其反应的实质是H+和OH-结合生成H2O.同理,H2SO4与BaCl2发生了化学反应,其反应的实质是Ba2+和${SO}_{4}^{2-}$生成硫酸钡沉淀.由此同学们总结得出:复分解反应发生的条件是有沉淀或气体或水生成.
(2)若将原四种溶液混合反应后过滤,滤液经检验呈碱性且不含Ba2+、SO42-,取滤液少量,加入BaCl2溶液,无沉淀产生,再滴入几滴酚酞试液,溶液变红色,则滤液中存在的离子有Na+、OH-、Cl-.
0 145072 145080 145086 145090 145096 145098 145102 145108 145110 145116 145122 145126 145128 145132 145138 145140 145146 145150 145152 145156 145158 145162 145164 145166 145167 145168 145170 145171 145172 145174 145176 145180 145182 145186 145188 145192 145198 145200 145206 145210 145212 145216 145222 145228 145230 145236 145240 145242 145248 145252 145258 145266 211419
(1)将四种溶液两两混合,若用H2SO4与另三种溶液分别混合:
| Na2CO3 | NaOH | BaCl2 | |
| H2SO4 |
②实验中的H2SO4与NaOH混合“无明显现象”,但实际上发生了化学反应,其反应的实质是H+和OH-结合生成H2O.同理,H2SO4与BaCl2发生了化学反应,其反应的实质是Ba2+和${SO}_{4}^{2-}$生成硫酸钡沉淀.由此同学们总结得出:复分解反应发生的条件是有沉淀或气体或水生成.
(2)若将原四种溶液混合反应后过滤,滤液经检验呈碱性且不含Ba2+、SO42-,取滤液少量,加入BaCl2溶液,无沉淀产生,再滴入几滴酚酞试液,溶液变红色,则滤液中存在的离子有Na+、OH-、Cl-.