1. 如右图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响).则滴管和烧瓶中所用试剂可能是B
如右图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响).则滴管和烧瓶中所用试剂可能是B
 如右图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响).则滴管和烧瓶中所用试剂可能是B
如右图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响).则滴管和烧瓶中所用试剂可能是B| 甲 | 乙 | |
| A | 稀硫酸和铜片 | 水和二氧化碳 |
| B | 双氧水和二氧化锰 | Ca(OH)2溶液和二氧化碳 |
| C | 水和氨气 | Mg和稀硫酸 |
| D | 碳酸钠溶液和稀盐酸 | 氢氧化钠溶液和二氧化碳 |
19.金属A和非金属B可直接合成化合物AB,甲、乙、丙三人分别作A和B化合反应的实验,充分反应时各人所用A和B的质量不同,但总质量都是9g.甲、乙所用A和B的质量及三人得到化合物AB的质量如表,请填写表中的空格.
| A的质量 | B的质量 | 得到AB的质量 | |
| 甲 | 7g | 2g | 6g |
| 乙 | 4g | 5g | 6g |
| 丙 | 5g | 4g | 7.5 |
18. 利用如图进行活性炭还原氧化铜的实验.
利用如图进行活性炭还原氧化铜的实验.
(1)请用化学方程式表示图中发生的反应.
①C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑
②CO2+Ca(OH)2═CaCO3↓+H2O
(2)请将下述实验步骤补充完整.
①检查装置的气密性.
②平放试管,用药匙将反应物送至试管底端.
③先预热试管,然后集中加热试管底部,观察记录.
④结束反应时,先将导管移离液面,再撤走酒精灯.
(3)为探究活性炭还原氧化铜的最佳条件,有研究小组进行了三组对照试验.各组实验结果如下.
表1:活性炭和氧化铜不同质量比对照实验
表2:反应物是否分别烘干对照实验
表3:反应混合物不同研磨时间对照实验
①上述记录中的下列现象,说明有铜生成的是BD(填编号).
A.固体红热 B.细小红色金属光泽固体 C.黑色固体 D.球状金属光泽固体
②归纳以上实验结果可知,活性炭还原氧化铜实验的最佳条件是:反应物质量比(C:CuO)
为1:8,反应物要先分别烘干研磨,然后再混合起来10分钟.
 利用如图进行活性炭还原氧化铜的实验.
利用如图进行活性炭还原氧化铜的实验.(1)请用化学方程式表示图中发生的反应.
①C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑
②CO2+Ca(OH)2═CaCO3↓+H2O
(2)请将下述实验步骤补充完整.
①检查装置的气密性.
②平放试管,用药匙将反应物送至试管底端.
③先预热试管,然后集中加热试管底部,观察记录.
④结束反应时,先将导管移离液面,再撤走酒精灯.
(3)为探究活性炭还原氧化铜的最佳条件,有研究小组进行了三组对照试验.各组实验结果如下.
表1:活性炭和氧化铜不同质量比对照实验
| 反应物质量比(C:CuO) | 1:6 | 1:8 | 1:10 | 1:12 | |
| 固体变化 | 实验中 | 轻微红热 | 红热 | 红热 | 红热 |
| 实验后 | 砖红色粉末中有少量黑色固体 | 多量球状金属光泽固体 | 砖红色粉末中有细小光亮金属光泽球状固体 | 砖红色粉末中有部分黑色固体 | |
| 是否烘干 | 否 | 是 | |
| 固体变化 | 实验中 | 无明显现象 | 红热 |
| 实验后 | 大量黑色固体中有少量砖红色粉末 | 红色金属光泽球状固体小颗粒 | |
| 研磨时间(分钟) | 0 | 5 | 10 | |
| 固体变化 | 实验中 | 无明显现象 | 轻微红热 | 红热 |
| 实验后 | 砖红色粉末中有少量黑色固体 | 砖红色粉末中有多量细小红色金属光泽固体 | 有多量金属光泽红色球状固体 | |
A.固体红热 B.细小红色金属光泽固体 C.黑色固体 D.球状金属光泽固体
②归纳以上实验结果可知,活性炭还原氧化铜实验的最佳条件是:反应物质量比(C:CuO)
为1:8,反应物要先分别烘干研磨,然后再混合起来10分钟.
16.下列四个图象分别表示对应的四种操作过程,其中正确的是( )
| A. | 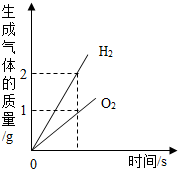 水的电解 | |
| B. |  用等质量、等浓度的过氧化氢溶液分别在加和没加MnO2条件下制取氧气 | |
| C. |  等质量的锌、铁与足量的稀硫酸反应,产生氢气的质量与反应时间的关系 | |
| D. |  某温度下,向不饱和氯化钠溶液中加入氯化钠 |
15. 在实验室、医院经常使用的多功能瓶如图所示,下列叙述错误的是( )
在实验室、医院经常使用的多功能瓶如图所示,下列叙述错误的是( )
 在实验室、医院经常使用的多功能瓶如图所示,下列叙述错误的是( )
在实验室、医院经常使用的多功能瓶如图所示,下列叙述错误的是( )| A. | 瓶内充满空气时,如果收集二氧化碳,a是进气管 | |
| B. | 瓶内盛满水时,如果收集氢气,a是进气管 | |
| C. | 瓶内盛有适量的浓硫酸用于干燥氧气时,a是进气管 | |
| D. | 瓶内盛放半瓶水,病人吸氧时,a管连接氧气罐 |
13.下列化学方程式书写正确的是( )
| A. | 氢气在一定浓度的氧气中能燃烧:H2+O2$\frac{\underline{\;点燃\;}}{\;}$H2O | |
| B. | 铝制品有较好抗腐蚀性的原因是:4Al+3O2$\frac{\underline{\;点燃\;}}{\;}$2Al2O3 | |
| C. | 将打磨过的铝丝放到硫酸溶液中:Al+H2SO4═Al2SO4+H2↑ | |
| D. | 燃烧红磷测定空气中氧气的含量:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 |
12.某同学为了测定实验室中氯酸钾样品的纯度,取2.5g该样品与0.5g二氧化锰混合,加热该混合物t1时间后(假设样品中杂质不参加反应),冷却,称量剩余固体质量,重复以上操作,依次称得加热t2、t3、t4时间后剩余固体的质量,记录数据如下表:
(1)写出发生反应的方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(2)加热t3时间后氯酸钾是否完全反应?是(填“是”或“否”)
(3)求完全反应后产生的氧气的质量.
(4)求该样品中氯酸钾的纯度.
0 145037 145045 145051 145055 145061 145063 145067 145073 145075 145081 145087 145091 145093 145097 145103 145105 145111 145115 145117 145121 145123 145127 145129 145131 145132 145133 145135 145136 145137 145139 145141 145145 145147 145151 145153 145157 145163 145165 145171 145175 145177 145181 145187 145193 145195 145201 145205 145207 145213 145217 145223 145231 211419
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量(g) | 2.12 | 2.08 | 2.04 | 2.04 |
(2)加热t3时间后氯酸钾是否完全反应?是(填“是”或“否”)
(3)求完全反应后产生的氧气的质量.
(4)求该样品中氯酸钾的纯度.
 相同质量的M、N两种活泼金属,分别与足量的稀盐酸反应(M、N在生成物中均为+2价),生成H2质量和反应时间的关系如图.下列叙述正确的是A
相同质量的M、N两种活泼金属,分别与足量的稀盐酸反应(M、N在生成物中均为+2价),生成H2质量和反应时间的关系如图.下列叙述正确的是A 根据下列实验装置图回答问题.
根据下列实验装置图回答问题.
