9.下列化学方程式书写正确的是( )
| A. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | B. | 2NaOH+CuSO4═Na2SO4+Cu(OH)2↓ | ||
| C. | 2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2↑+O2↑ | D. | Fe2O3+2H2SO4═2FeSO4+2H2O |
8.为纪念化学对社会进步和人类文明的贡献,联合国将2011年定为“国际化学年”.下列说法不正确的是( )
| A. | 合成药品的研发和使用,保障了人体健康 | |
| B. | 新材料的研制和应用,提高了人们的生活品质 | |
| C. | 大量燃烧煤、石油和天然气,促进了低碳经济的发展 | |
| D. | 化肥的合理使用提高了农作物产量,缓解了人类粮食危机 |
5.实验室氧气的制取及性质等探究考查.

(1)写出图A中有标号仪器的名称:a酒精灯、b铁架台、c锥形瓶;
(2)用A装置作为发生装置制取氧气时,发生反应的文字表达式为氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气.
可选用的发生装置是(填序号)A;可选用的收集装置是(填序号)C或E.实验室还有一种反应可用此装置制取氧气,但需在试管口放一团棉花,其反应的文字表达式为:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.
(3)实验室常用氯化铵固体与碱石灰固体混和加热来制取氨气.常温下氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水.制取并收集氨气时,应该从图1中选择的发生装置是A(填序号),收集装置是D.(填序号)
(4)用E装置收集氧气时,检验氧气是否集满的方法是把带火星的木条放在瓶口来验满,如果带火星的木条在瓶口能复燃,则证明该瓶氧气已经收集满了.
(5)若直接使用图2所示装置收集O2,则O2由a口进入;若将装置中充满水,则O2由b口进入.
(6)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是B(填序号),该反应的文字表达式为过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.若想控制该反应的反应速率,B装置的改进方法是注射器代替B装置中的长颈漏斗.要想收集一瓶较纯净的氧气,应选用的收集装置为C.
对此实验,让我们继续思考并研究几个问题:
问题一:催化剂二氧化锰(MnO2)的用量对反应速率有没有影响?
实验方案是:每次均用30mL10%的过氧化氢(H2O2)溶液,采用不同量二氧化锰(MnO2)粉末作催化剂,测定各次收集到500mL氧气时所用的时间,结果如下:(其他条件均相同)
请分析表中数据分析写出你的实验结论:答:有,MnO2的用量越多,反应速率越来越快.
问题二:H2O2溶液的溶质质量分数(浓度)对反应速率有没有影响呢?他又做了一组实验:每次均取5mL 30%的H2O2溶液,然后稀释成不同溶质质量分数的溶浠讲行章聆.记录数据如下:(实验均在20℃室温下进行,其他实验条件也均相同)
请分析表中数据回答:
H2O2溶液的溶质质量分数对反应速率的影响是H2O2溶液的质量分数越大反应速率越快.
由表中数据还可看出,该反应是个放热反应.(填“放热”或“吸热”)
问题三:下面是收集相同体积的氧气所需的时间,将其探究过程与前面的相结合,除了可以完成过氧化氢溶液的浓度对反应速率的影响的探究之外,还可以完成的探究问题是:催化剂的种类.
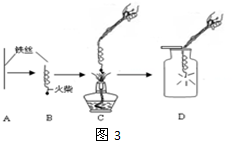
(7)某同学用收集到的氧气作图3所示实验,在细铁丝前端系一火柴的目的是引燃铁丝,将细铁丝绕成螺旋状的目的是为了增大铁丝与氧气的接触面积和增大铁丝的受热面积,此实验在在的问题是集气瓶内没有预先装少量水或铺一层细沙,造成的后果是燃烧产生的熔融物溅落瓶底使瓶底炸裂,改正后再次收集,完成实验,你看到的燃烧现象是剧烈燃烧,放出大量的热,火星四射,产生黑色固体,反应的文字表达式为铁+氧气$\stackrel{点燃}{→}$四氧化三铁,反应类型为化合反应.

(1)写出图A中有标号仪器的名称:a酒精灯、b铁架台、c锥形瓶;
(2)用A装置作为发生装置制取氧气时,发生反应的文字表达式为氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气.
可选用的发生装置是(填序号)A;可选用的收集装置是(填序号)C或E.实验室还有一种反应可用此装置制取氧气,但需在试管口放一团棉花,其反应的文字表达式为:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.
(3)实验室常用氯化铵固体与碱石灰固体混和加热来制取氨气.常温下氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水.制取并收集氨气时,应该从图1中选择的发生装置是A(填序号),收集装置是D.(填序号)
(4)用E装置收集氧气时,检验氧气是否集满的方法是把带火星的木条放在瓶口来验满,如果带火星的木条在瓶口能复燃,则证明该瓶氧气已经收集满了.
(5)若直接使用图2所示装置收集O2,则O2由a口进入;若将装置中充满水,则O2由b口进入.
(6)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是B(填序号),该反应的文字表达式为过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.若想控制该反应的反应速率,B装置的改进方法是注射器代替B装置中的长颈漏斗.要想收集一瓶较纯净的氧气,应选用的收集装置为C.
对此实验,让我们继续思考并研究几个问题:
问题一:催化剂二氧化锰(MnO2)的用量对反应速率有没有影响?
实验方案是:每次均用30mL10%的过氧化氢(H2O2)溶液,采用不同量二氧化锰(MnO2)粉末作催化剂,测定各次收集到500mL氧气时所用的时间,结果如下:(其他条件均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| MnO2粉末用量(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 所用时间(t) | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 | 2 | 2 |
问题二:H2O2溶液的溶质质量分数(浓度)对反应速率有没有影响呢?他又做了一组实验:每次均取5mL 30%的H2O2溶液,然后稀释成不同溶质质量分数的溶浠讲行章聆.记录数据如下:(实验均在20℃室温下进行,其他实验条件也均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| H2O2溶液溶质质量分数 | 1% | 3% | 5% | 10% | 15% | 20% | 25% | 30% |
| MnO2粉末用量(g) | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 |
| 收集540mL气体所用的时间(t) | 660 | 220 | 205 | 80 | 25 | 9 | 4 | 3 |
| 反应后液体温度(℃) | 24 | 34 | 39 | 56 | 65 | 67 | 69 | 70 |
H2O2溶液的溶质质量分数对反应速率的影响是H2O2溶液的质量分数越大反应速率越快.
由表中数据还可看出,该反应是个放热反应.(填“放热”或“吸热”)
问题三:下面是收集相同体积的氧气所需的时间,将其探究过程与前面的相结合,除了可以完成过氧化氢溶液的浓度对反应速率的影响的探究之外,还可以完成的探究问题是:催化剂的种类.
| 浓度 时间(min) 条件 | 等体积的30% H2O2溶液 | 等体积的15% H2O2溶液 | 等体积的5% H2O2溶液 |
| 加入a g MnO2 | 0.2 | 0.8 | 2.0 |
| 加入a g Fe 2O3 | 7.0 | 9.0 | 16.0 |

3.下列物质中存在氧分子的是( )
| A. | 水 | B. | 臭氧 | C. | 空气和液氧 | D. | 二氧化碳 |
1.下列有关H2O的说法中,正确的是( )
0 144811 144819 144825 144829 144835 144837 144841 144847 144849 144855 144861 144865 144867 144871 144877 144879 144885 144889 144891 144895 144897 144901 144903 144905 144906 144907 144909 144910 144911 144913 144915 144919 144921 144925 144927 144931 144937 144939 144945 144949 144951 144955 144961 144967 144969 144975 144979 144981 144987 144991 144997 145005 211419
| A. | 水是由两个氢元素和一个氧元素组成的 | |
| B. | 水是由氢氧两种原子组成的 | |
| C. | 一个水分是由两个氢原子和一个氧原子构成的 | |
| D. | 水是由两个氢原子和一个氧原子构成的 |
 ;③2个碳酸根离子2${{CO}_{3}}^{2-}$.
;③2个碳酸根离子2${{CO}_{3}}^{2-}$.