4.稀盐酸可用于除铁锈,发生的反应可用如下化学方程式表示:X+6HCl═2FeCl3+3H2O,则X 的化学式为( )
| A. | FeO | B. | Fe3O4 | C. | Fe2O3 | D. | Fe2O |
3.下列说法中正确的是( )
| A. | 氢原子和氧原子保持水的化学性质 | |
| B. | 氯化钠晶体由氯化钠分子构成 | |
| C. | 化学反应的微观实质是原子的重新组合 | |
| D. | 原子不显电性,是因为原子中不存在带电的粒子 |
2.下列物质属于纯净物的是( )
| A. | 冰水混合物 | B. | 清澈的湖水 | C. | 浑浊的河水 | D. | 自来水 |
1.下列实验操作中,正确的是( )
| A. |  点燃酒精灯 | B. |  滴加液体 | C. |  取用固体粉末 | D. | 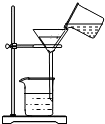 过滤 |
20.下列关于空气的说法不正确的是( )
| A. | 空气是人类宝贵的资源 | B. | 空气中氧气约占总质量的1/5 | ||
| C. | 空气中含量最多的是氮气 | D. | 空气是混合物 |
19.下列物质的性质与所对应的用途没有直接关系的是( )
| A. | 二氧化碳不支持燃烧--用于灭火 | |
| B. | 稀有气体的性质稳定--作保护气 | |
| C. | 酒精具有可燃性--医疗上用作消毒剂 | |
| D. | 干冰升华吸热--用于人工降雨 |
18.下列说法中正确的是( )
| A. | 经常用水冲洗自行车可以防锈 | B. | 用活性炭可以降低水的硬度 | ||
| C. | 空气主要由氮气和氧气组成 | D. | 铁合金是一种纯净物 |
16.小明家的新房装修,瓦工师傅用石灰浆(主要成分是氢氧化钙)抹墙.收工时瓦工师傅把未用完的石灰浆用沙土盖上,以备第二天再用,这样做的目的是防止石灰浆因变质而失效.
(1)请你根据所学知识写出石灰浆变质的化学方程式:Ca(OH)2+CO2=CaCO3↓+H2O.
(2)小明想通过实验验证石灰浆的变质情况,请你帮助小明完成以下实验.
(3)由此小明联想到实验室里的一些药品必须密封保存.实验室中必须密封保存的药品可分为以下几类:①药品能与空气中的成分发生反应,如澄清的石灰水;
②药品具有挥发性,如浓盐酸;
③药品具有吸水性,如浓硫酸.
0 144752 144760 144766 144770 144776 144778 144782 144788 144790 144796 144802 144806 144808 144812 144818 144820 144826 144830 144832 144836 144838 144842 144844 144846 144847 144848 144850 144851 144852 144854 144856 144860 144862 144866 144868 144872 144878 144880 144886 144890 144892 144896 144902 144908 144910 144916 144920 144922 144928 144932 144938 144946 211419
(1)请你根据所学知识写出石灰浆变质的化学方程式:Ca(OH)2+CO2=CaCO3↓+H2O.
(2)小明想通过实验验证石灰浆的变质情况,请你帮助小明完成以下实验.
| 实验步骤 | 实验现象 | 实验结论 |
| 取样,加一定量水充分溶解后,过滤 | 该石灰浆部分变质 | |
| 取少量滤渣于试管中,加入足量稀盐酸 | 有气泡产生 | |
| 取少量滤液于试管中,滴入无色酚酞试液 | 无色变红色 |
②药品具有挥发性,如浓盐酸;
③药品具有吸水性,如浓硫酸.

