3.学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了以下探究.
【猜想】Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、CuO参与反应产生O2,反应前后质量好化学性质发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后质量和化学性质不变.
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
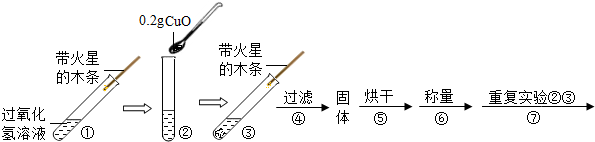
(1)填写下表:
(2)步骤①的目的是与步骤③对比,检验加入氧化铜后双氧水的分解速率是否发生了变化.
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒.
(4)过氧化氢能被CuO催化分解放出O2的符号表达式为2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑.
【拓展】影响过氧化氢溶液分解产生氧气的快慢的因素还有度升高,过氧化氢溶液分解的速率加快.(一种即可)
【猜想】Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、CuO参与反应产生O2,反应前后质量好化学性质发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后质量和化学性质不变.
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦目的 | 结论 |
剧烈反应,产生大量气泡 | 0.2g | 带火星木条复燃 | 猜想Ⅰ、Ⅱ不成立;猜想Ⅲ成立. |
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒.
(4)过氧化氢能被CuO催化分解放出O2的符号表达式为2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑.
【拓展】影响过氧化氢溶液分解产生氧气的快慢的因素还有度升高,过氧化氢溶液分解的速率加快.(一种即可)
20.20°C时100g某硝酸钾溶液,经过以下变化,恢复到20°C,最终析出晶体的质量是( )


| A. | 小于3克 | B. | 等于3克 | C. | 大于3克 | D. | 大于等于3克 |
19.一氧化碳还原氧化铜的实验装置如图所示,有关说法错误的是( )


| A. | 实验时通入CO后再点燃A处酒精灯,可以防止爆炸 | |
| B. | 通过观察黑色固体颜色的变化判断反应是否发生 | |
| C. | 通入0.1mol一氧化碳可以生成0.1mol铜 | |
| D. | 实验结束时应先熄灭A处酒精灯 |
14.为了探究影响大理石与稀盐酸反应剧烈程度的因素,某学习小组将稀盐酸分成四等份,分别加入四支试管中进行下列对比实验.

下列对比实验的设计不合理的是
( )
0 144511 144519 144525 144529 144535 144537 144541 144547 144549 144555 144561 144565 144567 144571 144577 144579 144585 144589 144591 144595 144597 144601 144603 144605 144606 144607 144609 144610 144611 144613 144615 144619 144621 144625 144627 144631 144637 144639 144645 144649 144651 144655 144661 144667 144669 144675 144679 144681 144687 144691 144697 144705 211419

下列对比实验的设计不合理的是
| 选项 | 对比实验 | 探究影响因素 |
| A | ①和② | 反应物的接触面积 |
| B | ②和③ | 温度 |
| C | ②和④ | 温度 |
| D | ③和④ | 反应物的接触面积 |
| A. | A | B. | B | C. | C | D. | D |


 海水淡化可解决淡水资源缺乏的问题.如图是海水淡化的一种装置.
海水淡化可解决淡水资源缺乏的问题.如图是海水淡化的一种装置.