15.奠定近代化学基础的是( )
| A. | 原子论和分子学说 | B. | 火的发现和利用 | ||
| C. | 门捷列夫发现元素周期律 | D. | 制得了人类有实用价值的产品 |
10.小宇和同学们在学习化学之后再次走进科技馆.下面的连环画记录了他们的参观过程.
请据图和叙述回答21-25题.
(1)今天天气晴朗,空气质量优良.
①下列属于空气污染物的是C(填字母序号).
A.N2 B.CO2 C.PM2.5
②保护人类赖以生存的空气,是每个公民的责任.小宇能做些什么呢?请你给她的出行提出一条建议:乘公交车出行.
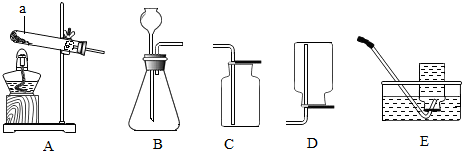
(2)来到“与门捷列夫对话”展台.看到熟悉的元素周期表,依据图②中显示的信息回答.
①氯的相对原子质量为35.45.
②镁元素是核电荷数为12的一类原子的总称.镁原子原子的结构示意图为: ,在化学反应中易失(填“得”或“失”)电子.
,在化学反应中易失(填“得”或“失”)电子.
③写出图②中一种元素的单质与氧气反应的化学方程式2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
(3)“身边的元素”展台摆放了一些家居用品,告诉大家身边的物质都是由元素组成的.依据化学式计算出Na2SiO3的相对分子质量为122,计算式为23×2+28+16×3.
(4)来到“新型材料”展台,小宇对记忆合金特别感兴趣.常见的双向记忆合金是钛镍合金,它属于金属(填“金属”或“非金属”)材料.
(5)太空探索”展台周围吸引了很多观众.
①航天员出舱所穿的宇航服能为其提供氧气,吸收二氧化碳.用于吸收二氧化碳的物质是氢氧化锂,已知其中锂(Li)的化合价为+1,其化学式为LiOH.
②钛合金具有很多优良的性能,可用于制造飞船和火箭发动机的壳体.下列有关说法正确的是ABC(填字母序号).
A.钛合金密度小,可以减轻飞船重量
B.钛合金的机械性能好、易于加工
C.钛合金耐高温,可以有效防止飞船高速飞行时被烧损.
 |  |
 |  |
(1)今天天气晴朗,空气质量优良.
①下列属于空气污染物的是C(填字母序号).
A.N2 B.CO2 C.PM2.5
②保护人类赖以生存的空气,是每个公民的责任.小宇能做些什么呢?请你给她的出行提出一条建议:乘公交车出行.
(2)来到“与门捷列夫对话”展台.看到熟悉的元素周期表,依据图②中显示的信息回答.
①氯的相对原子质量为35.45.
②镁元素是核电荷数为12的一类原子的总称.镁原子原子的结构示意图为:
 ,在化学反应中易失(填“得”或“失”)电子.
,在化学反应中易失(填“得”或“失”)电子.③写出图②中一种元素的单质与氧气反应的化学方程式2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
(3)“身边的元素”展台摆放了一些家居用品,告诉大家身边的物质都是由元素组成的.依据化学式计算出Na2SiO3的相对分子质量为122,计算式为23×2+28+16×3.
(4)来到“新型材料”展台,小宇对记忆合金特别感兴趣.常见的双向记忆合金是钛镍合金,它属于金属(填“金属”或“非金属”)材料.
(5)太空探索”展台周围吸引了很多观众.
①航天员出舱所穿的宇航服能为其提供氧气,吸收二氧化碳.用于吸收二氧化碳的物质是氢氧化锂,已知其中锂(Li)的化合价为+1,其化学式为LiOH.
②钛合金具有很多优良的性能,可用于制造飞船和火箭发动机的壳体.下列有关说法正确的是ABC(填字母序号).
A.钛合金密度小,可以减轻飞船重量
B.钛合金的机械性能好、易于加工
C.钛合金耐高温,可以有效防止飞船高速飞行时被烧损.
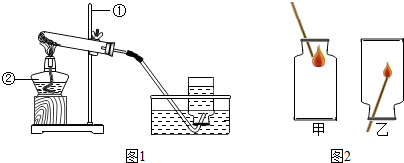
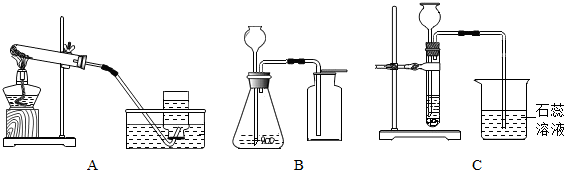
8.根据如图回答问题:

(1)装置图中标号仪器的名称:①试管,②集气瓶.
(2)实验室若用A装置制取氧气,反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(3)实验室制取二氧化碳的化学方程式是CaCO3+2HCl═CaCl2+CO2↑+H2O.若用G收集二氧化碳,二氧化碳应从a(选“a”或“b”)进,装置C与装置B相比,其主要优点是可以控制反应的发生或停止.
(4)工业上用碳酸钙在高温下分解来制取氧化钙和二氧化碳.
①若要制取5.6t氧化钙,需碳酸钙的质量是多少?(请写出计算过程)
②小华为测定某石灰石样品中碳酸钙的质量分数,取一定量的石灰石样品,将20g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余成分不与盐酸反应,也不溶于水),充分反应后经过过滤、干燥等操作,最后称量,数据如下表:
这种石灰石样品中碳酸钙的质量分数为80%.若要制取5.6t氧化钙,理论上需要这种石灰石的质量是12.5t.
0 144426 144434 144440 144444 144450 144452 144456 144462 144464 144470 144476 144480 144482 144486 144492 144494 144500 144504 144506 144510 144512 144516 144518 144520 144521 144522 144524 144525 144526 144528 144530 144534 144536 144540 144542 144546 144552 144554 144560 144564 144566 144570 144576 144582 144584 144590 144594 144596 144602 144606 144612 144620 211419

(1)装置图中标号仪器的名称:①试管,②集气瓶.
(2)实验室若用A装置制取氧气,反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(3)实验室制取二氧化碳的化学方程式是CaCO3+2HCl═CaCl2+CO2↑+H2O.若用G收集二氧化碳,二氧化碳应从a(选“a”或“b”)进,装置C与装置B相比,其主要优点是可以控制反应的发生或停止.
(4)工业上用碳酸钙在高温下分解来制取氧化钙和二氧化碳.
①若要制取5.6t氧化钙,需碳酸钙的质量是多少?(请写出计算过程)
②小华为测定某石灰石样品中碳酸钙的质量分数,取一定量的石灰石样品,将20g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余成分不与盐酸反应,也不溶于水),充分反应后经过过滤、干燥等操作,最后称量,数据如下表:
| 稀盐酸的用量 | 剩余固体的质量 |
| 第一次加入5g | 1.5g |
| 第二次加入5g | 1.0g |
| 第三次加入5g | 0.5g |
| 第四次加入5g | 0.4g |

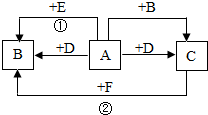 如图,A、B、C、D、E、F均是初中化学的常见物质,A、B、C均含有同一种元素.变化①的现象是颜色由黑变红,变化②的现象是颜色由红变黑,相应变化的生成物没有全部列出,各变化的条件也未标出.回答下列问题:
如图,A、B、C、D、E、F均是初中化学的常见物质,A、B、C均含有同一种元素.变化①的现象是颜色由黑变红,变化②的现象是颜色由红变黑,相应变化的生成物没有全部列出,各变化的条件也未标出.回答下列问题: