10.如图4个坐标图分别表示4个实验过程中某些质量的变化,其中不正确的是( )
| A. |  向一定量过氧化氢溶液中加入少量二氧化锰 | |
| B. |  将等质量的镁片和铁片投入到足量稀硫酸中 | |
| C. | 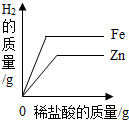 向相同质量的铁粉和锌粉中分别加入足量稀盐酸 | |
| D. |  一氧化碳与一定量氧化铁在高温条件下完全反应 |
6.下列图象能正确反映其对应操作中各量变化关系的是( )
| A. |  红磷燃烧 | |
| B. |  加热一定量的高锰酸钾固体 | |
| C. |  在少量二氧化锰中加入双氧水 | |
| D. |  加热一定量的氯酸钾和二氧化锰的混合物 |
5.除去下列物质中的少量杂质,所选试剂及操作都正确的是( )
| 序号 | 物 质 | 杂 质 | 试 剂 | 主要操作 |
| A | CO2 | CO | 氧气 | 点燃 |
| B | CuSO4 | FeSO4 | 铁 | 过滤 |
| C | NaCl | 泥沙 | 水 | 溶解、过滤、蒸发 |
| D | 镁粉 | 铁粉 | 盐酸 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
4.实验室制取氧气时,下列操作错误的是( )
| A. | 固定试管,试管口稍向下倾斜 | |
| B. | 加热时,先预热,再对试管中药品部位集中加热 | |
| C. | 导管口刚有泡泡冒出口,立即收集 | |
| D. | 固定试管,铁夹夹在离试管口$\frac{1}{3}$处 |
3.化学兴趣小组的同学对某炼铁厂生产的生铁(杂质不与酸反应)进行组成分析.其实验数据如下表.
实验后测得加入的生铁与盐酸恰好完全反应,根据表中数据,计算
(1)生成氢气质量.
(2)生铁中铁的质量分数.
(3)反应后所得溶液中溶质质量分数.
0 143875 143883 143889 143893 143899 143901 143905 143911 143913 143919 143925 143929 143931 143935 143941 143943 143949 143953 143955 143959 143961 143965 143967 143969 143970 143971 143973 143974 143975 143977 143979 143983 143985 143989 143991 143995 144001 144003 144009 144013 144015 144019 144025 144031 144033 144039 144043 144045 144051 144055 144061 144069 211419
| 实验步骤 | 相关数据 |
| 1称取生铁样品放入烧杯中 | 16g |
| 2加入适量14.6%的盐酸 | 200.0g |
| 3称取反应后烧杯中物质总质量 | 215.8g |
(1)生成氢气质量.
(2)生铁中铁的质量分数.
(3)反应后所得溶液中溶质质量分数.



