20.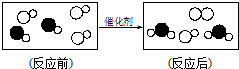 如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法错误的是( )
如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法错误的是( )
 如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法错误的是( )
如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法错误的是( )| A. | 此反应有单质生成 | |
| B. | 图中生成物全部是化合物 | |
| C. | 原子在化学变化中没有分裂 | |
| D. | 参加反应的两种分子的个数比为1:1 |
16.请根据下列实验装置图回答问题:
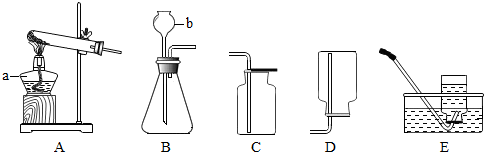
(1)写出仪器a、b的名称.a是酒精灯; b是长颈漏斗.
(2)选用B、D装置组合制取收集某气体的条件是:制取反应物为固体与液体,且反应不需加热、收集气体的密度比空气的密度小.
(3)若要收集较纯净的氧气进行实验,应选用装置E收集氧气(填序号).这种操作注意的要点是集气瓶内要装满水,等气泡连续、均匀冒出时再收集气体.收集满氧气的集气瓶用毛玻璃片盖好后瓶口应向上(填“向上”或“向下”)放在桌面上.
(4)用装置BC组合制备氧气.并用该瓶氧气做铁丝燃烧实验时,未看到“火星四射”现象,下列解释合理的是Ⅰ、Ⅱ、Ⅳ (填序号).
Ⅰ.收集到的氧气太少,纯度太低
Ⅱ.所用铁丝表面有油漆
Ⅲ.集气瓶底部没有预先铺一薄层细沙
Ⅳ.铁丝的温度未达到燃烧温度
(5)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),通过以下四步实验操作可回收二氧化锰.正确操作的先后顺序是b-c-d-a(填写选项序号).
a.烘干 b.溶解 c.过滤 d.洗涤(6)在二氧化锰的催化作用下,过氧化氢、氯酸钾能迅速分解生成氧气.课外活动小组进行了更深入的探究.
【探究实验一】:温度对化学反应速率是否有影响?
实验用品:试管、烧杯、热水、冷水、5%过氧化氢溶液
【探究实验二】:氧化铜是否也能作氯酸钾分解的催化剂?
设计实验:小刚设计了下列二组实验(其它可能影响实验的因素均忽略).
上述实验应测量的“待测数据”是生成等体积的氧气所需的时间.
若实验②比实验①的“待测数据”更小 (填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率.
【讨论交流】小刚同学认为,根据上述实验的结论就能判断氧化铜是该反应的催化剂,你是否支持他的观点?并简述理由.不支持;未验证氧化铜反应前后的质量和化学性质是否改变
【实验拓展】回顾整个工作过程,你认为在准备工作阶段除考虑制氧气反应的难易、反应所需的温度等因素外.还应考虑的因素是制氧气过程的安全性(或有没有污染环境的物质放出、或考虑药品的价格等)(合理即可).(写一条即可)
(7)实验时小刚加热6克氯酸钾和二氧化锰的混合物一段时间,冷却至室温,称得剩余固体物质的质量为4.08克,则生成氧气的物质的量是多少?同时消耗氯酸钾的物质的量是多少?(写出计算过程)
0 143874 143882 143888 143892 143898 143900 143904 143910 143912 143918 143924 143928 143930 143934 143940 143942 143948 143952 143954 143958 143960 143964 143966 143968 143969 143970 143972 143973 143974 143976 143978 143982 143984 143988 143990 143994 144000 144002 144008 144012 144014 144018 144024 144030 144032 144038 144042 144044 144050 144054 144060 144068 211419

(1)写出仪器a、b的名称.a是酒精灯; b是长颈漏斗.
(2)选用B、D装置组合制取收集某气体的条件是:制取反应物为固体与液体,且反应不需加热、收集气体的密度比空气的密度小.
(3)若要收集较纯净的氧气进行实验,应选用装置E收集氧气(填序号).这种操作注意的要点是集气瓶内要装满水,等气泡连续、均匀冒出时再收集气体.收集满氧气的集气瓶用毛玻璃片盖好后瓶口应向上(填“向上”或“向下”)放在桌面上.
(4)用装置BC组合制备氧气.并用该瓶氧气做铁丝燃烧实验时,未看到“火星四射”现象,下列解释合理的是Ⅰ、Ⅱ、Ⅳ (填序号).
Ⅰ.收集到的氧气太少,纯度太低
Ⅱ.所用铁丝表面有油漆
Ⅲ.集气瓶底部没有预先铺一薄层细沙
Ⅳ.铁丝的温度未达到燃烧温度
(5)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),通过以下四步实验操作可回收二氧化锰.正确操作的先后顺序是b-c-d-a(填写选项序号).
a.烘干 b.溶解 c.过滤 d.洗涤(6)在二氧化锰的催化作用下,过氧化氢、氯酸钾能迅速分解生成氧气.课外活动小组进行了更深入的探究.
【探究实验一】:温度对化学反应速率是否有影响?
实验用品:试管、烧杯、热水、冷水、5%过氧化氢溶液
| 实验步骤 | 现 象 | 结 论 |
| 取一支试管加入3~5mL5%的过氧化氢溶液,然后把试管放入盛有冷水的烧杯中 | 缓慢有少量气泡冒出 | 温度越高,过氧化氢分解的速率越大 |
| 取一支试管加入3~5mL5%的过氧化氢溶液,然后把试管放入盛有热水的烧杯中 | 迅速有大量气泡冒出 |
设计实验:小刚设计了下列二组实验(其它可能影响实验的因素均忽略).
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | / | |
| ② | 1.2g | CuO 0.5g |
若实验②比实验①的“待测数据”更小 (填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率.
【讨论交流】小刚同学认为,根据上述实验的结论就能判断氧化铜是该反应的催化剂,你是否支持他的观点?并简述理由.不支持;未验证氧化铜反应前后的质量和化学性质是否改变
【实验拓展】回顾整个工作过程,你认为在准备工作阶段除考虑制氧气反应的难易、反应所需的温度等因素外.还应考虑的因素是制氧气过程的安全性(或有没有污染环境的物质放出、或考虑药品的价格等)(合理即可).(写一条即可)
(7)实验时小刚加热6克氯酸钾和二氧化锰的混合物一段时间,冷却至室温,称得剩余固体物质的质量为4.08克,则生成氧气的物质的量是多少?同时消耗氯酸钾的物质的量是多少?(写出计算过程)


 ,表现为易失去(填“得到”或“失去”)电子;氯元素的相对原子质量为35.5.
,表现为易失去(填“得到”或“失去”)电子;氯元素的相对原子质量为35.5.



 某化学小组欲测定洪泽湖大堤上某石灰石块中碳酸钙的质量分数,进行了如下实验研究.
某化学小组欲测定洪泽湖大堤上某石灰石块中碳酸钙的质量分数,进行了如下实验研究.