仓库中有一包氮肥的包装标签模糊不清,有同学进行了以下探究:
(1)操作③用玻棒搅拌的目的是 .
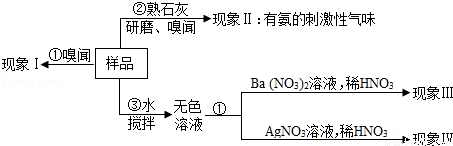
(2)请完成下表(已知AgCl和BaSO4是难溶于水和酸的白色固体):
假设和现象 | 判断和化学方程式 | |
a | 若现象I为无氨味. | 则样品中不含 (填名称). |
b | 由操作②现象判断. | 该样品一定含有 离子. |
c | 若现象Ⅲ为白色沉淀,现象Ⅳ为无沉淀. | 则样品中含有 (写名称),该反应的化学方程式为 . |
d | 若现象Ⅲ为“无沉淀”,现象Ⅳ为白色沉淀. | 则样品中含有 (写化学式),该反应的化学方程式为 . |
(3)若现象Ⅲ、Ⅳ都无现象,则该氮肥可能是 (写化学式);若操作②现象为无气味、现象Ⅲ、Ⅳ无现象,则该氮肥可能是 (只写一种).
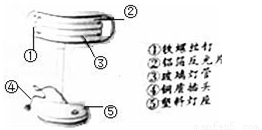
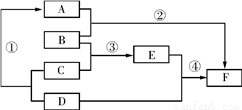
如下图是实验室制取气体的常用仪器。请根据要求填空:

(1)图中仪器名称是②____________,⑧____________。
(2)小宝同学用氯酸钾和二氧化锰制取并收集一瓶氧气,应选择上图中的仪器____________(填序号,下同),其化学方程式为:________________________;验证瓶中氧气已集满的方法是________________________________。
(3)小茹同学用锌和稀硫酸制取H2,同时生成硫酸锌,则应选择上图中____________装置,其化学方程式为:________________________________。
(4)小佳同学查阅资料得到制取硫化氢气体的如下信息,请回答下列问题:
气体 | 实验药品 | 反应条件 | 气体物理性质 |
H2S | 硫化亚铁固体与稀硫酸 | 不需加热 | 无色,密度比空气大,可溶于水 |
①制取硫化氢____________(填“可以”或“不可以”)采用装置①,理由是________________________________________________。
②制取硫化氢____________(填“可以”或“不可以”)采用装置②和③,理由是____________________________________________________。
糕点疏松剂的主要成分中含有碳酸氢钠,某化学兴趣小组对碳酸氢钠的化学性质进行探究。
【探究实验一】碳酸氢钠溶液的酸碱性:用玻璃棒蘸取碳酸氢钠溶液滴在pH试纸上并与__________对比,读出其pH值约为10,由此得出结论是:碳酸氢钠溶液呈碱性。
【探究实验二】碳酸氢钠能否与酸反应:取少量固体放入试管中,滴加足量的稀盐酸,现象为__________,结论:碳酸氢钠能与酸反应。
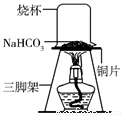
【探究实验三】碳酸氢钠的热稳定性:取一定量的碳酸氢钠放在铜片上加热,如图所示。
(1)加热一段时间后,观察到烧杯内壁有水珠。
(2)充分加热后,将烧杯迅速倒转过来,加入适量的澄清石灰水,振荡,观察到石灰水变浑浊。
(3)通过进一步实验来确定充分加热后的固体产物的成分,限选试剂及仪器:稀盐酸、氯化钙溶液、澄清石灰水、酚酞溶液、蒸馏水、试管、胶头滴管。
序号 | 实验操作 | 预期现象 | 结论 |
① | 取少量加热后的固体产物放入试管A中,加入适量蒸馏水,充分振荡溶解,滴加足量氯化钙溶液,振荡,静置 | 产生白色沉淀 | 产物含__________ |
② | 取操作①后的上层清液于试管B中,滴加____________ | ____________ | 产物不含NaOH |
请分析上述操作①中不能用澄清石灰水替代氯化钙溶液的理由_______________________________________________________。
(4)根据上述实验结论,写出碳酸氢钠受热分解的化学方程式_______________________。
为分析某由氧化铜和铜组成的混合物中氧化铜的质量分数,现取3份该混合物各20 g,分别缓慢加入到50 g、100 g、150 g某稀硫酸中,测得三组实验数据如表:
组别 | 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 |
稀硫酸的质量/g | 50 | 100 | 150 |
溶解固体的质量/g | 10.0 | 16.0 | 16.0 |
根据实验及有关数据进行分析与计算:
(1)第Ⅰ组实验中反应物______________(填“氧化铜”“稀硫酸”或“氧化铜与稀硫酸”)反应完。
(2)20 g样品中含氧化铜的质量为________g。
(3)根据第Ⅰ组数据计算所用的稀硫酸溶质的质量分数(写出计算过程)。
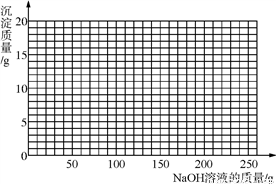
(4)将第Ⅱ组混合物过滤,在滤液中滴加10%的NaOH溶液,画出在该混合溶液中加入10% NaOH溶液的质量与生成沉淀质量变化关系的曲线图。