为除去下列物质中的杂质,下列操作方法能达到目的的是
选项 | 物质(杂质) | 操作方法 |
A | CO2(H2O) | 将气体通过盛有火碱的干燥管 |
B | CuO(CuSO4) | 加入过量硫酸并加热 |
C | Na2SO4(Na2CO3) | 加盐酸至恰好不再产生气泡为止 |
D | FeCl2(CuCl2) | 加入足量铁屑,充搅拌应后过滤 |
A. A B. B C. C D. D
学习化学就是要研究物质的组成、结构、性质、变化、用途、制法等知识。
⑴判断下列物质的类别,并用相应的序号填空
①单质②氧化物③酸④碱⑤盐
物质化学式 | HNO3 | CuSO4 |
物质类别 | ________ | ________ |
⑵按要求写化学符号:铝离子________;两个甲烷分子________。
⑶在下列横线上填写“>”、“<”、“=”。
①热稳定性:氯化钠________碳酸氢铵
②耐酸、耐碱性:棉纱线________腈纶。
⑷现有以下四种物质:A.硝酸钾B.熟石灰C.碘酒D.尼龙,根据下列要求用字母填空:
①能用作配制波尔多液的是________;②可用作钓鱼线的是________;
⑸按要求写出方程式:
①实验室制氢气__________;②自然界中制取氧气的主要方法__________。
吴老师为了鼓励同学们研究蛋白质的相关性质,请同学们将鸡蛋带到实验室,并设计了甲乙两组实验。
甲实验:
实验步骤 | 实验内容 | 实验现象 |
① | 在盛有鸡蛋清的试管中滴加饱和硫酸铵溶液; | 有白色絮状沉淀出现; |
② | 再向上述试管中加入少量蒸馏水,振荡; | ____________ |
乙实验:
实验步骤 | 实验内容 | 实验现象 |
① | 在盛有鸡蛋清的试管中滴加乙酸铅溶液; | 有沉淀出现 |
② | 再向上述试管中加入少量蒸馏水,振荡; | ____________ |
分析与思考:
⑴ 甲实验研究的是蛋白质的________(填“盐析”或“变性”);
⑵ 通过甲、乙实验对比说明:乙实验是________(填“物理变化”或“化学变化”);
⑶ 为进一步研究乙实验中蛋白质发生的变化是乙酸铅溶液中铅离子作用还是乙酸根离子作用,以下可以与乙酸铅溶液做对照实验的试剂有________。
A.乙酸铵溶液 B.硫酸铜溶液 C.硫酸铅溶液 D.福尔马林溶液
据统计,我国每年报废的手机超过1亿部,若不进行有效回收利用,会造成巨大的浪费和污染。同学们对废旧手机中的金属回收产生兴趣。
【提出问题】从废旧手机中可以回收到哪些有价值的金属?如何回收?
【查阅资料】
Ⅰ.手机电路板中的金属及其价格如下表所示:
种类 | Fe | Cu | Al | Ni | Au | Ag | Pd(钯) |
市场价格/($/t) | 365 | 7175.5 | 1710.5 | 14235 | 4.7×107 | 7.6×105 | 2.7×107 |
矿石中含量 | 72.4 | 0.87 | 29.1 | 1.02 | 4 | 120 | 0.4 |
手机电路板中含量 | 5 | 13 | 1 | 0.1 | 350 | 1380 | 210 |
说明:Fe、Cu、Al、Ni的含量用质量分数(%)表示,Au、Ag、Pd的含量的单位为“g/t”。
Ⅱ.Ni的金属活动性位于氢前;Pd的金属活动性位于氢后;NiCl2溶液为绿色。
Ⅲ.2Cu + O2 + 2H2SO4 2CuSO4 + 2H2O
【实验方案】
第一步:选择值得回收的金属。
依据资料Ⅰ中的数据,废旧手机中有回收价值的金属有Au、Ag、Cu、Pd,原因是:①它们的市场价格较高;②________________。
第二步:设计实验分离、回收部分金属。
序号 | 实验步骤 | 实验现象 |
I | 取一废旧手机电路板,用电吹风机靠近电路焊接点的焊锡吹热风,一段时间后,用镊子将金属电路从塑料板中拽出 | 焊锡熔化 |
II | 将金属电路放入烧杯中,加入过量稀盐酸浸泡 | …… |
III | 取II中未溶解的金属电路,用蒸馏水洗净后,放入如图所示装置中,进行实验。
| 溶液逐渐变成蓝色,仍有微量金属固体未溶解 |
IV | 过滤III中烧杯中的物质,洗涤滤纸上的物质 | 滤纸上仍有微量金属固体 |
V | …… | …… |
【问题讨论】
⑴ 由步骤I中的现象,可推知的焊锡的物理性质是________;
⑵ 步骤II对应的实验现象是________________;
⑶ 步骤II所得溶液中,至少含有溶质有______种;
⑷ 步骤V的操作是:“向步骤Ⅳ获得滤液中加入一定量铁粉”,若该实验过程加入铁粉前后溶液中主要离子变化示意图如图所示。

① 图中“ ”所代表微粒的符号为________;
”所代表微粒的符号为________;
② 充分反应后过滤,滤纸上固体物质是________(写化学式)。
小苏打(碳酸氢钠)在日常生活中有广泛的用途,工业上制取小苏打有多种方法,其中有一种是气相固碳法,其利用的原理是:Na2CO3 + H2O + CO2 =2NaHCO3
资料: 碳酸钠和碳酸氢钠的溶解度表(一个标准大气压下)(部分)
温度/℃ | 0 | 15 | 20 | 30 | 40 | 50 | 60 |
碳酸氢钠溶解度/g | 6.9 | 8.72 | 9.6 | 11.1 | 12.7 | 14.45 | 16.4 |
碳酸钠溶解度/g | 7.1 | 13.25 | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 |
学校实验小组验证反应原理,在室温为15℃时,同学们将10g氢氧化钠固体完全溶解溶于80g水中,而后匀速的通入二氧化碳气体。同时用传感器测定溶液的pH变化,同时用数据采集器记录并绘制图像如图2所示。
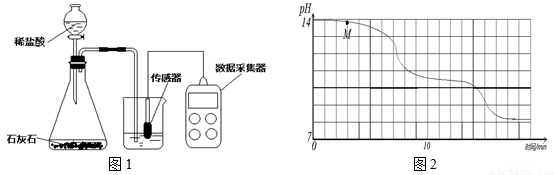
⑴ 图1所示实验中,用“分液漏斗”而不用“长颈漏斗”其原因是______________;
⑵ 通过图像分析,小苏打溶液是显________(填“酸性”、“中性”或“碱性”),图像中M点处发生的主要化学反应方程式为________________;
⑶ 为了确定M处溶液的成分,同学们进行如下实验:
实验步骤 | 加入试剂 | 实验现象 | 初步实验结论 |
① | 滴入________ | 溶液变红 | 有________物质 |
② | 加入________ | ______________ |
⑷ 实验过程中,同学们发现18min后溶液的pH基本不再变化,则此时烧杯中就可观察到的现象有________。
 4NO+6H2O
4NO+6H2O 


