同学们对实验“煅烧石灰石”展开深入探究.
资料:石灰石中的杂质高温不分解.
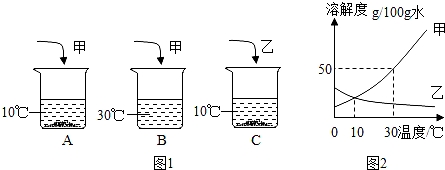
①为证明石灰石已分解,三位同学设计方案如图:
Ⅰ.甲同学按图一进行实验(煤气灯亦能达到石灰石分解的温 度),观察到烧杯内壁石灰水变浑浊,写出石灰水发生反应的化学方程式 .
度),观察到烧杯内壁石灰水变浑浊,写出石灰水发生反应的化学方程式 .
II.乙同学按图二进行试验,观察到B中液体变 色,A实验的作用 .
III.大家认为甲同学的方案不合理,请分析原因.
IV.丙同学取一块质量为12.5g的石灰石煅烧,并记录有关数据如下表
| 时间(秒) | 0 | 60 | 120 | 180 | 240 | 300 |
| 固体质量(克) | 12.5 | 12.3 | 11.2 | 9.2 | 8.1 | 8.1 |
根据上述数据判断, 秒时,已经可以证明石灰石开始分解了.240秒时,石灰石已经完全分解了,理由是 .
②根据丙同学记录的数据,该石灰石分解共生成 克CO2,物质的量为 mol.根据化学方程式列式计算:这块石灰石中含碳酸钙的质量是 克.

同学想研究不同的氧化物能否在氯酸钾制取氧气实验中起催化作用,进行了以下实验:
| 实验编号 | KClO3/g | 氧化物 | 产生气体的体积(mL) | 耗时(s) |
| 1 | 0.6 | / | 9.8 | 4 |
| 2 | 0.6 | 0.2g二氧化锰 | 67 | 36.5 |
| 3 | 0.6 | 0.2g氧化铜 | 67 | 89.5 |
①写出实验2反应的化学方程式 ;
②为证明氧化铜是该反应的催化剂,同学们又完成了以下的实验:
Ⅰ.在实验3反应后的混合物中加足量的水溶解,过滤,将滤渣洗涤并干燥,用电子天平称量,质量为0.2g.
Ⅱ.将过量的CO通入滤出的固体,
按如图进行实验:仪器a的名称 .
③甲同学的实验报告如下:
| 装置 | 现象 | 实验结论 |
| A | 黑色固体全部变红 | 生成了铜,反应方程式 CO+CuO |
| B | 石灰水变浑浊 | 产生了二氧化碳 |
Ⅲ.该实验装置存在的缺陷是 ;当出现 现象时,证明反应已经开始.
④以上实验证明氧化铜在反应前后质量和化学性质都没改变,能作为氯酸钾受热分解的催化剂.两种氧化物相比, 的催化效果更好.
的催化效果更好.

 Cu+CO2
Cu+CO2 
 ”表示氧原子,“
”表示氧原子,“ ”表示氢原子):
”表示氢原子):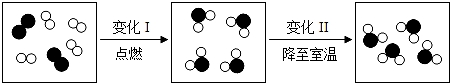
 ”的 m 倍.则参加反应的
”的 m 倍.则参加反应的  和
和  的质量比为 .
的质量比为 .



 断加入蔗糖固体
断加入蔗糖固体