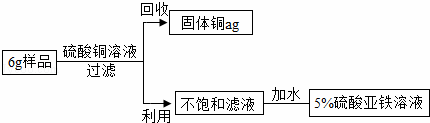
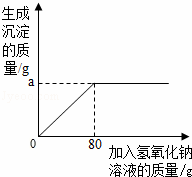
某学校化学兴趣小组的同学对我市南部山区的大理石矿区进行调查并取样。样品的主要成分是碳酸钙(其中含有二氧化硅等杂质)。下面是同学们的实验探究过程,请你参与并回答有关。
【实验目的】测定大理石样品中碳酸钙的质量分数。
【查阅资料】二氧化硅等杂质不溶于水,也不与盐酸反应。
【实验过程】准确称量5.0g大理石样品于烧杯中,向其中加入40mL质量分数为20%的盐酸,立即将烧杯放在电子秤上称量。每分钟记录一次数据(提示:反应结束后盐酸有剩余)。
相关的实验数据如下表:
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 质量/g | 102.0 | 101.0 | 100.5 | 100.2 | 100.1 | 100.4 | 100.1 | 100.1 | 100.1 |
【数据处理】
⑴表中有一个称量数据是不合理的,该数据的测定时间是_分钟。
⑵计算样品中碳酸钙的质量分数。(写出计算过程,计算结果保留一位小数)
【反思交流】实验结束后,部分同学认为测得的碳酸钙质量分数偏大,请你分析出现此情况的原因可能是_ _。
为了测定某纯碱样品(含少量氯化钠杂质)中碳酸钠的质量分数,取该样品与足量稀盐酸在烧杯中反应,有关实验数据如下表。
| 反应前 | 反应后 | ||
| 实验 数据 | 烧杯和稀盐酸的质量/g | 纯碱样品的质量/g | 烧杯和其中混合物的质量/g |
| 120 | 12 | 127.6 |
请计算:(1)反应生成二氧化碳的质量为 g。
(2)该纯碱样品中碳酸钠的质量分数是多少。(请写出计算过程)
某化学探究小组的同学在学校仓库里找到一块废弃的生铁暖气片,其表面有银粉漆(铝粉)涂层.该组同学取一小块生铁暖气片,用砂纸打磨除净涂层,制成生铁样品,为测定此样品中铁质量分数,他们将样品放入烧杯中,再加入足量的稀盐酸,至不再有气泡产生为止.
各步称量数据见下表:(稀盐酸的挥发可忽略不计)
| 除净涂层后的生铁样品质量/g | 11.5 |
| 烧杯的质量/g | 32.5 |
| 所加稀盐酸的质量/g | 200.0 |
| 反应后烧杯及所盛物质的总质量/g | 243.6 |
请回答下列问题:
(1)反应中产生气体的质量是 g.
(2)计算该生铁样品中铁的质量分数(写出计算步骤,计算结果精确到0.1%).
(3)以下操作中,对该样品中铁的质量分数的测定结果,没有影响的是 (填写序号).
A、加入的稀盐酸不足量
B、将打磨干净涂层的生铁样品磨成粉末
C、假设涂层中的铝粉已完全转化为氧化铝,且样品表面涂层未打磨干净.

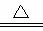 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑