一瓶未贴标签的粉末状常见金属R,为了测定R的相对原子质量,准确称取一定量金属粉末,在坩埚内加强热使其完全氧化,冷却后再称重,重复试验,获得如表数据.请回答:
| 试验次数 | 金属质量(g) | 金属氧化物质量(g) |
| 1 | 45.0 | 84.9 |
| 2 | 45.0 | 85.1 |
| 3 | 45.0 | 85.0 |
| 平均值 | 45.0 | m |
(1)表格中m=
(2)该金属氧化物中,R元素和氧元素的质量比为
(3)已知R的化合价为+3价,则R的相对原子质量为 .
将红色的铜丝放在酒精灯火焰的外焰上加热,铜丝表面变为黑色,下列说法错误的是( )
|
| A. | 红色铜丝表面变黑,是因为生成了氧化铜 |
|
| B. | 红色铜丝表面变黑,是因为铜发生了还原反应 |
|
| C. | 立即把变黑的铜丝插入稀硫酸中,溶液会出现蓝色 |
|
| D. | 立即把变黑的铜丝插入酒精中,铜丝变回红色 |
将一定质量金属M的粉末放入盛有Cu(NO3)2溶液的烧杯中,充分反应后溶液呈无色;继续向烧杯中加入一定量的AgNO3溶液,待充分反应后过滤,得蓝色滤液和滤渣.根据实验分析,以下结论错误的是( )
|
| A. | 金属活动性顺序:M>Cu>Ag |
|
| B. | 滤液中一定含有M的阳离子和Cu2+ |
|
| C. | 滤渣中一定含有Ag和Cu |
|
| D. | 向滤液中滴加稀盐酸,可能产生白色沉淀 |
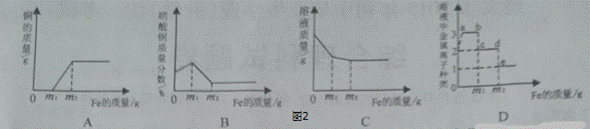
用廉价金属回收贵重金属是工业生产中的一道重要程序.某化学兴趣小组的同学在实验室中进行了模拟实验.向含有硝酸铜和硝酸银的废液中加入一定量的铁粉,充分反应后过滤,得到滤液和滤渣.下列说法正确的是( )
|
| A. | 滤液中最多含有三种溶质 |
|
| B. | 滤液质量比反应前原溶液质量大 |
|
| C. | 滤液中一定含有硝酸亚铁,滤渣中一定含有银 |
|
| D. | 若反应后所得滤液呈浅绿色,则滤渣中一定含有铁、铜、银 |
在AgNO3、Zn(NO3)2和Cu(NO3)2的混合溶液中加人一定量的铁粉,充分反应后过滤.向滤渣中加入稀盐酸,有气泡产生.根据上述现象,下列结论正确的是( )
|
| A. | 滤渣中一定有Zn | B. | 滤渣中可能有Ag、Cu |
|
| C. | 滤液中﹣定有Fe(NO3)2、Zn(NO3)2 | D. | 滤液中可能有AgNO3、Cu(NO3)2 |
金属M与AgNO3溶液发生反应:M+2AgNO3=M(NO3)2+2Ag,下列说法正确的是( )
|
| A. | M可能是铝 |
|
| B. | Ag的金属活动性比M强 |
|
| C. | 反应前后M的化合价发生了改变 |
|
| D. | 在金属活动性顺序里,M一定排在氢前 |
将一定量的锌粉加入到硫酸亚铁、硫酸铜和硫酸镁的混合溶液中,过一段时间后过滤,向滤渣中加入稀盐酸有气泡产生,则下列叙述正确的是( )
①滤渣中一定含有锌
②滤渣中一定含有铜,可能含有锌
③向滤渣中加入稀盐酸,最后溶液一定变成浅绿色
④滤液中溶质一定含有硫酸锌和硫酸镁
⑤滤液的颜色不可能为浅绿色.
|
| A. | ①④⑤ | B. | ②③④⑤ | C. | ②③④ | D. | ②④ |