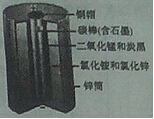
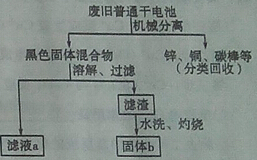
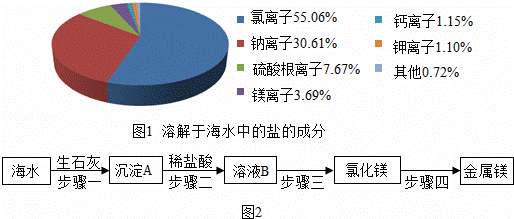
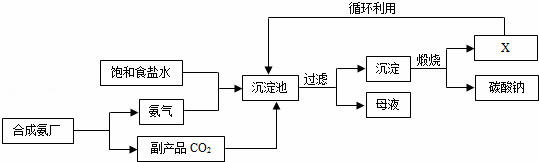
我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),促进了世界制碱技术的发展.下列有关说法正确的是()
|
| A. | 沉淀池中的反应物共含有六种元素 |
|
| B. | 过滤得到的“母液”中一定只含有两种溶质 |
|
| C. | 图中X可能是氨气 |
|
| D. | 通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀 |
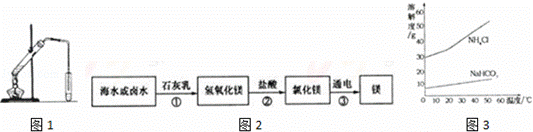
燃煤产生的烟气中含有二氧化硫,直接排放会污染空气,它与水反应形成酸雨污染环境,某科研小组利用海水除去二氧化硫,其工艺流程见下图:
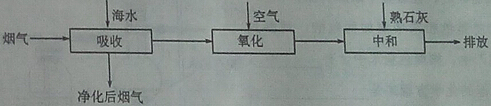
请回答下列问题:
(1)二氧化硫中硫的化合价是 。
(2)用熟石灰中和稀硫酸的化学方程式是 。
(3)亚硫酸(H2SO3)被空气中氧气氧化为硫酸,写出反应的化学方程式 。
(4)为了研究脱硫率(脱硫率是已除去的二氧化硫的量占总二氧化硫量的百分比——与温度、烟气中SO2浓度的关系,他们进行了探究实验。实验结果如下:
| 实验序号 | 温度/℃ | 烟气中SO2浓度/10-2g·L-1 | 脱硫率/% |
| I | 23 | 2.5% | 99.5 |
| II | 23 | 3.2% | 97.1 |
| III | 40 | 2.5% | 94.3 |
由表中实验数据可得出的结论是 。
(5)目前,科学家正在研究在一定条件下将乙烯(C2H4)和烟气混合除去二氧化硫,其反应的过程可分为如下三步:
第一步:O2与Cu+反应生成Cu+(O2)
第二步:Cu+(O2)与SO2反应生成Cu+(SO3)2
第三步:Cu+(SO3)2与C2H4反应生成S、CO2、H2O和Cu+。
①反应中Cu+的作用是 。
②除去二氧化硫的总反应的化学方程式是 。