某化学小组初步探究“氢氧化钠溶液与盐酸发生中和反应时溶液温度的变化情况”。
实验用品:37%的浓盐酸(密度为1.18g/mL)、10%的氢氧化钠溶液、蒸 馏水、量筒、温
馏水、量筒、温 度计
度计
实验一:配制100mL10%的盐酸(密度为1.05g/mL)
实验步骤
(1)计算:需要37%的浓盐酸的体积为 mL(精确到0.01mL,下同);需要蒸馏水的体积为 mL(水的密度为1.0g/mL)
(2)量取浓盐酸和蒸馏水。
(3)混合配制。
实验二:在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸(室温下),反应中溶液温度的变化如下:
| 加入盐酸的体积(V)/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
| 溶液温度变化(△t)/℃ | △t1 | 5.2 | 9.6 | 12.0 | 16.0 | 18.2 | 16.7 | 15.7 | 14.7 | 13.7 | 12.9 |
(1)表中△t1的值为 。
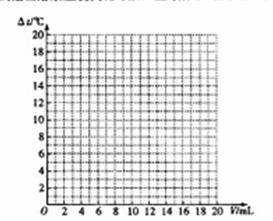 (2)试绘出溶液温度变化与加入盐酸体积之间的关系图。
(2)试绘出溶液温度变化与加入盐酸体积之间的关系图。
(3)根据所绘曲线分析,加入盐酸的体积在0~10mL时,溶液温度变化的趋势及其原因是
。
(4)其他条件不变,若改用20%的盐酸进行滴加,结合对上述曲线的分析,大胆猜想新曲线最高点的位置(不考虑溶液密度和比热容的变化及热量散失等影响因素)。
横坐标及猜想理由: ;
纵坐标及猜想理由: 。
从硅的氧化物可以制取硅单质,主要化学反应如下:
粗硅的制取:SiO2 + 2C Si + 2CO↑

 石英砂 焦炭 粗硅
石英砂 焦炭 粗硅
由粗硅制纯硅(常用方法):Si(粗) + 2Cl2 SiCl4 SiCl4 + 2H2 Si(纯) + 4HCl
 四氯化硅
四氯化硅
(1)根据上述信息,请补全制取纯硅的简易流程图:

(2)根据已有知识和上述信息,进行总结归纳:
① 完成置换反应的通式:单质(I) + 化合物(I)= 单质(II) +  。
。
② 填写下表:
| 单质(I) | 化合物(I) | 相应的置换反应的化学方程式(各一例) | |
| A | 金属 | 非金属 | Fe + 2HCl = FeCl2 + H2↑[来源:学_科_网Z_X_X_K] |
| B | 金属 | 金属 | [单质(I)为铜] |
| C |
|
|
|
| D |
| 金属 | H2 + CuO Cu + H2O |
 D.铁锅
D.铁锅
 Na2CO3 + H2O + CO2↑)
Na2CO3 + H2O + CO2↑) 方案一:如图所示
方案一:如图所示 请写出该气体与炭粉发生反应的化学方程式: 。
请写出该气体与炭粉发生反应的化学方程式: 。




 钠在氯气中燃烧 氯化钠形成的示意图
钠在氯气中燃烧 氯化钠形成的示意图 (填微粒符号)。
(填微粒符号)。