实验室常用下列装置制取气体,请你根据所学知识回答下列问题。


① 写出所指仪器名称:a ⑴ ;b ⑵ 。
② 以上装置图中共有两处明显错误,请改正:
Ⅰ  ⑶ ;Ⅱ ⑷ 。
⑶ ;Ⅱ ⑷ 。
③ 写出实验室选用A和E装置制取氧气的化学方程式 ⑸ ,该反应类型 ⑹ 。
下列有关实验操作错误的是 ⑺ (填序号)。
Ⅰ.气密性检查:用手握紧试管,观察到水中导气管有气泡冒出,说明装置不漏气
Ⅱ.加热:直接用酒精灯的焰心对准药品所在位置加热
Ⅲ.收集气体:当导管口刚有气泡冒出时立即收集
Ⅳ.停止加热:先把导管移出水面,再熄灭酒精灯
④ 装置B中小试管的作用是 ⑻ ;若装置B中反应剧烈,从实验安全角度考虑,不宜采取的措施有 ⑼ (填序号)。
Ⅰ.用容积较小的锥形瓶 Ⅱ.减慢液体滴加速度
Ⅲ. 加热反应物 Ⅳ.降低液体反应物浓度
加热反应物 Ⅳ.降低液体反应物浓度
B装置还可以验证二氧化碳的化学性质,请完成下表中的内容:
| 仪器名称 | 长颈漏斗 | 小试管 | 锥形瓶 |
| 装置内的药品 | ⑽ | 大理石 | (11) |
| 用化学方程式表示相关性质 | (12) |
如图所示,某校化学兴趣小组用过氧化氢(H2O2)溶液(MnO2作催化剂)制取干燥的氧气,并用来侧定,10g某铜粉样品(含杂质碳)中铜的质量分数.回答下列问题:
(1)仪器a的名称是 .
(2)装置A中发生反应的化学方程式是 .装置B的作用是 .
(3)通过称量反应前后装置 的质量,进行计算便可求出样品 中铜的质量分数.
中铜的质量分数.
(4)实验完毕.小丽同学误将用剩的H202溶液和装置C玻璃管中的剩余固体一起倒入烧杯中,发现有大最的气泡产生,经检验确认产生的气体是氧气.小刚和小明两位同学对此颇感兴趣.进而展开了他们的探究之旅.
【提出问题】是哪种物质加快了H202的分解速率?
【大胆猜想】猜想Ⅰ:剩余固体中的氧化铜加快了H202溶液的分解.
猜想Ⅱ:剩余固体中的 加快了H2O2溶液的分解.
猜想Ⅲ:氧化铜能做H202分解的催化剂.
【实验验证】
| 实验方案 | 实验现象 | 分析及结论 |
| 实验一:将带火星的木条伸入盛有5mL 5%H2O2溶液的试管. | 带火星木条不复燃 | H202溶液常温下产生氧气的量很少,不足以使带火星的木条复燃 |
| 实验二:向盛有5mL5%H202溶液的试管中加入1g氧化铜固体,将一根带 |
称得固体质量为1g. | 猜想Ⅰ成立.反应前后 |
| 实验三:向盛有5mL5%H202溶液的试管中加入1g ,将一根带火星的木条伸入试管,观察现象. | 没有气泡产生,带火星 木条不复燃. | 猜想Ⅱ (填”成立“或“不成立”) |
【讨论交流】小刚同学认为,根据实验二得出的两个结论就能判断Ⅲ成立,你是否支持他的观点?并简述理由。
答: 。 .

实验室常用石灰石和稀盐酸制取二氧化碳。
探究一 气体发生装置的选择

(1)写出图中带标号仪器的名称:a ;b 。
(2)实验室制取二氧化碳气体,发生和收集装置分别选用 和 (填字母),检验集满的方法是 。
探究二 药品的选择
小明对三组药品进行了研究,实验记录如下:
| 组别 | 药 品 | 实验现象 |
| ① | 块状石灰石和稀盐酸 | 产生气泡速率适中 |
| ② | 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
| ③ | 粉末状石灰石和稀盐酸 | 产生气泡速率很快 |
对照实验①③,是探究 对产生二氧化碳速率的影响;
对照实验 ,是探究不同的酸对产生二氧化碳速率的影响;
小明选择第①组药品来制取二氧化碳,该组反应的化学方程式为 。
探究三 生成二氧化碳量的测定
实验室常通过下列两种途径测量生成二氧化碳的量
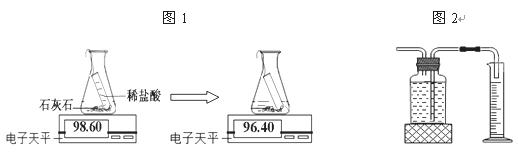
途径一(如图1):由图可知产生二氧化碳的质量为 g。
途径二(如图2):通过排水法测得生成二氧化碳的体积。
由上两种途径比较,你认为哪种途径实验结果更为准确,理由是 。

 (1) 。
(1) 。





 氧化铜的质量相等.
氧化铜的质量相等.