石灰石的主要成分为CaCO3,所含杂质不溶于水,也不参加反应。某化学兴趣小组为了测定石灰石中CaCO3的质量分数,进行了以下探究实验:称石灰石样品二份,分别放入大烧杯中,第一个烧杯中加入50克稀盐酸,第二个烧杯中放入100克同样的稀盐酸,充分反应至不再有气泡产生时称量残留物质量,有关数据如下表。
| 各物质的质量 | 第一个烧杯 | 第二个烧 |
| 石灰石样品质量 | 12g | 12 g |
| 稀盐酸质量 | 50g | 100g |
| 烧杯残留物质量 | 58.7 g | 107.6g |
| 产 |
|
|
求:(1)二个烧杯中产生CO2的质量(填入上表);
(2)石灰石样品中CaCO3的质量分数。(精确到0.1%)
现有下列三种物质,请根据要求回答有关内容。
| 物 质 | 化学方程式 | 简 述 |
| 生石灰 | 说明:可用作食品干燥剂 | |
| 酒精 | C2H5OH + 3O2点燃2CO2 + 3H2O | 用途: |
| 红磷 | 用途:测空气中氧气的含量 |
下图分别与相应的操作过程相对应,其中正确的是
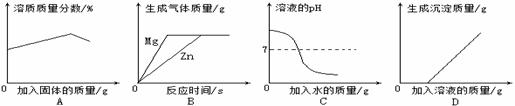 |
A.恒温下,向一接近饱和的硝酸钾溶液中不断加入硝酸钾晶体
B.向等质量、等溶质质量分数的稀硫酸中分别加入足量的镁片和锌片
C.向pH=10的氢氧化钙溶液中不断加水稀释
D.向含有硫酸的硫酸铜的混合溶液中加入过量的氢氧化钠溶液
 如图所示装置气密性良好、要使注射器中的活塞向右移动,使用的液体M和固体N可能是
如图所示装置气密性良好、要使注射器中的活塞向右移动,使用的液体M和固体N可能是
 杯
杯 下列装置常用于实验室制取气体。根据给出的装置回答下列问题:
下列装置常用于实验室制取气体。根据给出的装置回答下列问题: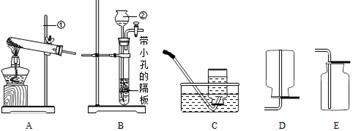
 示为____________________________,利用C装置收集氧气的最佳时刻是
示为____________________________,利用C装置收集氧气的最佳时刻是  。
。
 如右是A、B两物质(均不含结晶水)
如右是A、B两物质(均不含结晶水) 溶解度为______________g;
溶解度为______________g;