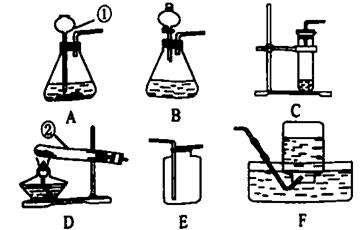
某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验,向烧杯中的氢氧化钙溶液滴加一定量的稀盐酸后,发现忘记滴加指示剂,此时,他们停止滴加稀盐酸,并对烧杯内溶液中溶质的成分进行探究。
(1)写出该中和反应的化学方程式_______________________。
(2)探究烧杯内溶液中溶质的成分:
【作出猜想】
(A)溶质可能是CaCl2与Ca(OH)2
(B)溶质可能是CaCl2
(C)溶质可能是CaCl2与HCl
【查阅资料】CaCl2溶液呈中性
【实验设计】
①取少量烧杯中的溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色。于是排除了猜想(A),你认为排除猜想(A)的理由是_____________。
②小华想用碳酸钠溶液来验证后两种猜想,请你帮他完成实验,填写以下表格:
| 实验步骤 | 预计现象 | 预计结论 |
| 取少量反应后的溶液于试管中, 逐滴加入碳酸钠溶液 | 猜想(B)正确 | |
| 猜想(C)正确 |
【交流反思】
为确定猜想(C)正确,下列几种实验方案不合理的是__________(填字母)。
A.取反应后的溶液于试管中,滴加紫色石蕊试液变红色
B.取反应后的溶液于试管中,加入锌粉冒气泡
C.用洁净的玻璃棒蘸取反应后的溶液,涂抹在pH试纸上,测溶液的pH <7
D.取反应后的溶液于试管中,加入硝酸银溶液,生成白色沉淀
有一种神奇的蜡烛,点燃后任你怎么吹也吹不灭,而且看上去和普通的蜡烛一样,那么到底是什么玄机能让蜡烛持续燃烧?请你一起参与探究。
查阅资料:普通蜡烛由石蜡和蜡烛芯制成,而吹不灭的蜡烛是在蜡烛芯上包裹一层打火石的粉末。打火石是由某种金属掺入少量稀土元素制成的合金,它的着火点只有150℃.当蜡烛燃烧时,金属并不燃烧;但当蜡烛吹灭后,未冷却的金属接触氧气就发生燃烧,从而使蜡烛复燃。
老师告诉同学们,蜡烛芯内打火石中的某种金属可能是镁、铁或铜中的一种,为确定该金属的成分,大家设计了以下实验方案,请你填空和回答有关问题(注:不考虑打火石中稀土元素对探究金属性质的影响)
| 实验 | 操作步骤 | 实验现象 | 实验结论 |
| 1 | 切开蜡烛,取出打火石,用砂纸打磨 | 打火石呈银白色 | 该金属一定不是铜。 |
| 2 | 取少量打磨后的打火石于试管中,滴加稀盐酸 | 有无色气体产生,溶液为无色。 | 该金属一定不是铁,而是镁。 |
反思交流:
(1)实验2中反应的化学方程式为 。
(2)这种蜡烛燃烧时,蜡烛芯里的金属为什么不燃烧? 。
(3)这种“吹不灭”的蜡烛实际上也可以熄灭,你采用的方法是 。
化学兴趣小组的同学发现,上个月做实验用的氢氧化钠溶液忘记了盖瓶盖。对于该溶液是否变质,小组内小明同学认为有两种可能:
猜想1:该溶液没有变质 猜想2:该溶液全部变质
(1)小组同学讨论后认为还有一种可能,请你补充出猜想3: 。
(2)为了验证猜想3,小红同学设计了如下实验方案,请你帮他完成实验报告的填写
| 实验步骤 | 实验现象 | 结论 |
| 1.取样, ,过滤 | 产生白色沉淀 | 猜想3成立 |
| 2.向上述滤液中滴加几滴无色酚酞溶液 | 酚酞溶液变红 |
(3)探究启示:氢氧化钠必须 保存。
某同学发现,上个月实验用过的氢氧化钠溶液的试剂瓶忘了盖瓶盖,对该溶液是否变质,同学们一起进行如下探究实验。
【猜想与假设】
猜想(1):该溶液没有变质;
猜想(2):该溶液全部变质;
猜想(3):该溶液部分变质;
【方案讨论】
为了验证猜想(2)或猜想(3),甲、乙、丙三同学分别提出如下方案。
甲:向溶液中滴加酚酞,若酚酞变红,则猜想(3)成立,否则猜想(2)成立。同学们认为此方案不行,原因是 。
乙:先向溶液中滴加足量的Ba(OH)2,再滴入酚酞,根据现象不同来判断猜想(2)或猜想(3)成立。
同学们认为此方案也不行,原因是 。
丙:先向溶液中滴加足量的BaCl2,再滴入酚酞,根据现象不同来判断猜想(2)或猜想(3)成立。同学们通过分析认为此方案可行。
【实验验证】
| 实验步骤 | 实验现象 | 结论及解释 |
| ①取少量待测液于试管中,向其中滴加足量 | 有气泡产生 | 猜想 不成立 |
| ②取少量待测液于试管中,向其中滴加足量的BaCl2溶液,静置,向上层清液中滴加酚酞 | 有 | 猜想 成立 |
【反思与交流】敞口放置的氢氧化钠溶液容易变质,所以要 保存。
实验室中的药品一般要密封保存,否则可能会与空气接触而变质。某研究性学习小组的同学对实验室里久置于空气中变质的过氧化钠(Na2O2)固体的成分进行探究。
[查阅资料](1)Na2O2的化学性质很活泼,能与水、二氧化碳反应,相关反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2↑ 2Na2O2+2CO2=2Na2CO3+O2↑
(2)CaCl2溶液为中性
[猜想]I:固体为Na2O2、NaOH、Na2CO3的混合物
II:固体为NaOH和Na2CO3的混合物
III:固体为NaOH
IV:固体为Na2CO3
[实验探究]
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量固体于试管中,加水振荡,直至完全溶解 |
| 猜想I不成立 |
| ②取少量①的溶液于试管中,滴加CaCl2溶液至过量 |
| 证明有Na2CO3存在 |
| ③
|
| 证明有NaOH存在 |
| 综合以上实验现象,说明猜想II是成立的。 |
[反思评价](1)实验操作②中反应的化学方程式为
(2)实验操作②中“滴加CaCl2溶液至过量”的目的是
小敏和小玉在实验室用盐酸和石灰石反应,分别用甲、乙装置(气密性均良好)进行二氧化碳的制取及性质实验,但均未发现澄清石灰水变浑浊。针对此现象,同学们提出了自已的想法。
小敏同学实验时澄清石灰水未变浑浊的原因是 。
[提出问題]小玉同学实验时澄清石灰水为什么没有变浑浊呢?
[作出猜想]猜想一:澄清石灰水已变质。猜想二:反应产生的气体中除了有二氧化碳外,还有氯化氢。
[查阅资料]氯化氢气体溶于水形成盐酸。
[实验探究]


| 实验 | 实验步骤 | 实验现象 | 实验结论 |
| 实验I | 将纯净的CO2通入到该实验所用的 澄清石灰水中 | 澄清的石灰水变浑浊 | 猜想一不成立 |
| 实验II | 将反应产生的气体通入到 |
| 猜想二成立 |
同学们经讨论发现,用丙装罝(如右图),在A、B中均加入实验II中所用试剂即可同时完成上述两个猜想的探究,其中B装置所起的作用是 。如果看到 现象,则两个猜想都成立。
[实验反思]由实验可知,小玉同学实验时可能错误使用了一种药品,她使用的药品是 。