某同学用氢氧化钙和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液中滴加稀盐酸一会儿后,发现忘记了滴加指示剂,因此,他停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行了如下探究。请你和他一起完成探究活动。
【提出问题】溶液中的溶质是什么物质?
【作出猜想】猜想一:溶液质只有氯化钙。
猜想二:溶质中有CaCl2和Ca(OH)2。
猜想三:溶液中有
【查阅资料】氯化钙溶液呈中性。
【方案设计】
| 方案 | 方法步骤 | 实验现象 | 实验结论 |
| 方案一 | 取少量烧杯内的溶液于试管中,滴入几滴无色酚酞溶液 | 酚酞不变色 | 猜想一正确 |
| 酚酞变红色 | 猜想二正确 | ||
| 方案二 | 取少量烧杯内的溶液于试管中,逐滴加入 溶液至过量 |
| 猜想三正确 |
【方案评价】该同学与同学们通过讨论后认为:(1)方案一能证明猜想二正确,但不能证明猜想一正确。(2)方案二可行,但该同学在记录时未记录完整,请你替他将方案二补充完整。
【方案反思】方案一不能证明猜想一正确的理由是 。
【拓展与应用】实验证明猜想三是正确的。要想使溶液中的溶质只有氯化钙,你认为应该进行的实验步骤是 。
【结论】在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑 。
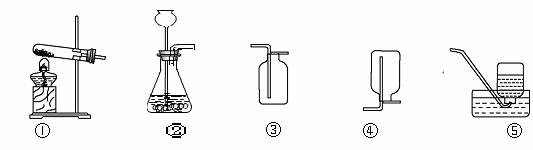
某校学习小组准备探究气体的测定和数据处理方法
【提出问题】
如何利用石灰石(主要成分为CaCO3)与稀盐酸反应来测定生成的CO2的质量和体积,并处理数据。
【实验设计】
通过下列两个实验分别测定CO2的质量和体积:

【分析与表达】
(1)上述两个实验中,反应的化学方程式是_______________________。
(2)实验Ⅰ中,将小烧杯中的所有稀盐酸分几次加入到大烧杯中,并不断搅拌,判断石灰石中CaCO3完全反应的实验现象是___________________________________________。
(3)实验Ⅱ中,先连接好装置,再_______(填操作名称),然后装好药品,最后将10 mL稀盐酸快速推入到烧瓶中,若稀盐酸是缓慢推入的,则可能造成的后果是______。
【记录与处理】
(4)已知实验Ⅰ反应前的总质量[m(大烧杯+石灰石粉末)+m(小烧杯+稀硫酸)],要计算生成的CO2的质量,至少还需要的数据是_______(填序号)
A.m(小烧杯) B.m(大烧杯) C.m(大烧杯+反应后的剩余物)
(5)实验Ⅱ的实验记录如下(表中数据在相同温度、相同压强条件下测定)
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 注射器读数/mL | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
①  根据以上实验过程和数据综合分析,最终生成CO2
根据以上实验过程和数据综合分析,最终生成CO2
的体积是______mL,理由是____________。
②根据你的认识,在坐标图中绘制出0~10min生成
CO2体积随时间变化的曲线。
【反思与评价】
(1)经过分析,你认为实验Ⅰ的优点是________,实验Ⅱ
的优点是________。
实验室有一瓶标签破损的无色溶液如图21,同学们对该溶液的成分进行了探究。
【提出问题】该溶液的成分是什么?
【猜想假设】①可能是CaCl2溶液;②你的猜想是 溶液;
【查阅资料】CaCl2的水溶液呈中性
【设计实验】同学们设计了如下实验方案并进行实验,请你完成实验报告.
| 实验操作 | 实验现象 | 实验结论 |
| 取该溶液少量于试管中, |
|
|
同学们在帮助老师整理实验室时,从1、2号橱窗中发现了两瓶失去标签的黑色粉末药品,并确定了这两瓶黑色粉末是木炭粉、铁粉、氧化铜、高锰酸钾中的两种。
他们继续进行了分析、试验和反思:
【查阅资料】 CuO、Fe2O3等金属氧化物与酸反应,生成盐和水
⑴ 分析:小燕同学认为一定不是高锰酸钾,原因是 ;
⑵ 实验一:
| 实验操作 | ||
| ①取一种黑色粉末少许,加入到稀硫酸中 | 黑色粉末溶解,溶液颜色变__ _ | 此粉末是氧化铜 |
| ②取另一种黑色粉末少许,加入到稀硫酸中 | 黑色粉末不溶解,没看到气体产生 | 此粉末一定不是铁粉 |
⑶ 反思:小华同学认为不做实验①,运用逻辑推理的方法也能得出其中之一是氧化铜的结论,原因是:_______________________________________________________________;
⑷ 实验二:他们又进行了如下实验:将两种黑色粉末混合加热(实验装置如下图),发现黑色粉末逐渐变_____,澄清石灰水变______。写出两种黑色粉末发生反应的化学方程式__ ___ _。

(1)实验室可用草酸(H2C2O4)在浓硫酸的作用下分解制得一氧化碳和二氧化碳(化学方程式为:H2C2O4
 CO2↑+CO↑+H2O)。用县的实验装置见下图:
CO2↑+CO↑+H2O)。用县的实验装置见下图:
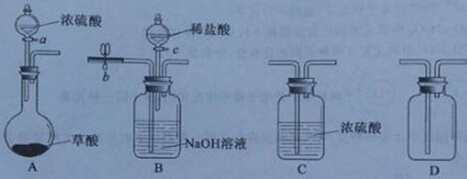
若分别得到一氧化碳和二氧化碳,请回答:
①装置A中,盛放浓硫酸的仪器名称是 ;
②收集一氧化碳时,打开a、b,关闭c,装置B的作用是 。由于一氧化碳有毒,多余的气体应 (填写具体处理办法);
③关闭 、打开 ,释放出二氧化碳,并通过装置 可收集到干燥的二氧化碳气体。
在二氧化锰的催化作用下,过氧化氢迅速分解生成氧气和水。哪些因素还影响着过氧化氢分解的速率?课外活动小组结些进行了更深入的探究:
探究实验一:浓度对化学反应速率的影响
| 实验步骤 | 现 象 | 结 论 |
| 取一支试管加入3~5mL5%的过氧化氢溶液,然后加入少量二氧化锰。 | 缓慢有少量气泡冒出 |
|
| 另取一支试管加入3~5mL15%的过氧化氢溶液,然后加入少量二氧化锰。 | 迅速有大量气泡冒出 |
请你设计:
实验用品:试管、烧杯、热水、冷水、5%过氧化氢溶液、15%过氧化氢溶液
探究实验二:温度对化学反应速率的影响
| 实验步骤 | 现 象 | 结 论 |
|
|
| 温度越高,过氧化氢分解的速率越大 |
|
|
|
化学兴趣小组设计的创新实验是“火龙生字”。在成果展示现场,某同学用硝酸钾的热饱和溶液先在白纸上书写“火”字,晾干后白纸上出现硝酸钾晶体(见图1)。用带火星的木条接触硝酸钾晶体,就会观察到白纸上写过字的地方燃烧并迅速蔓延,留下“火”字的黑色痕迹(间图2)。在场的同学对此产生了浓厚的兴趣,并进行了如下探究:
【提出问题】为甚附有硝酸钾的白纸更容易燃烧?
【查阅资料】硝酸钾受热易分解,生成亚硝酸钾(KNO2)和一种常见的气体单质。
【猜想与假设】对于生成的是什么气体,四位同学有如下猜想:
甲:二氧化氮;乙:氮气;丙:氧气;丁:氢气。
同学丙指出不可能是二氧化氮、氢气,理由是: ; 。
【进行实验】四位同学设计了实验对同学丙的猜想进行了验证,他们的操作方法是:
,观察到的现象是 ,说明同学丙的猜想正确。
硝酸钾分解的化学方程式是 :
【解释与结论】白纸上写过字的地方更容易燃烧的原因是: 。
【反思与评价】为什么要用“硝酸钾的热饱和溶液”书写文字?
已知硝酸钾在不同温度时的溶解度如下表:
| 温度/℃ | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 31.6 | 63.9 | 110 | 169 | 246 |
你对上述问题的解释: 。

 (4)写出甲烷燃烧的化学方程式_________________________________________。
(4)写出甲烷燃烧的化学方程式_________________________________________。 显中性。
显中性。