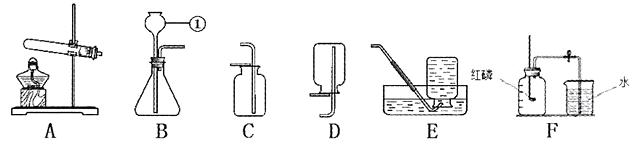
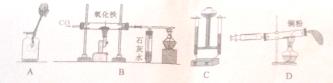
实验室可利用碱式碳酸铜(化学式:Cu2(OH)2CO3)制备氧化铜,并进行碳粉还原氧化铜的实验。
①制备氧化铜并检验产物,装置如下图所示(省略夹持仪器):
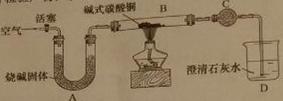
步骤一:连接A和B,打开活塞,通入空气。
步骤二:关闭活塞,连上C和D,开始加热。
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热。
| 加热时间(min) | 0 | t1 | t2 | t3 |
| B中固体质量(g) | 6.66 | 5.20 | 4.80 | 4.80 |
B中发生反应的化学方程式为: 1 Cu2(OH)2CO3 2CuO + 1 H2O + 1 CO2↑
2CuO + 1 H2O + 1 CO2↑
 请在 中填入配平后的系数 。
请在 中填入配平后的系数 。
C中试剂是 。A的作用是吸收空气中的 ,防止对产物检验造成干扰。选择t3时停止加热的理由是 。
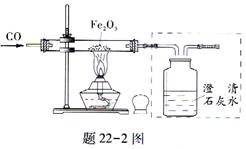
② 一定量碳粉还原①中制得的氧化铜并检验产物,装置如下图所示:
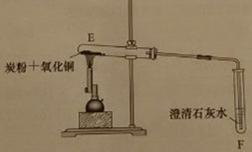
实验过程中,观察到F中溶液变浑浊,E中的现象是 。
反应完全后,若仅撤走酒精喷灯停止加热,可能导致的后果是 。
③ 分析:若①中省略步骤三,对②中反应产物判断可能产生的影响及其原因。
二十一世纪是海洋开发与利用的世纪,我市实施黄蓝两大国家战略形成新的发展格局,海洋化学资源的综合利用将是重点发展领域之一。
(1)海水晒盐:将海水引入蒸发池,经日晒蒸发到一定程度时,导入结晶池,继续日晒,海水就会成为食盐的饱和溶液,再晒就会逐渐析出粗盐,剩余的液体称为母液(也称卤水)。
1L海水在逐渐浓缩过程中不断析出的盐的种类和质量(单位:g)关系如下表所示:
| 海水密度(g/mL) | CaSO4 | NaCl | MgCl2 | MgSO4 |
| 1.20 | 0.91 | |||
| 1.21 | 0.05 | 3.26 | 0.004 | 0.008 |
| 1.22 | 0.015 | 9.65 | 0.01 | 0.04 |
| 1.26 | 0.01 | 2.64 | 0.02 | 0.02 |
| 1.31 | 1.40 | 0.54 | 0.03 |
I.海水晒盐是 (选填“物理”或“化学”)变化,包含蒸发. 等过程。
II.若得到纯度较高的粗盐和含浓度较高的卤水,卤水的密度应控制在什么范围 ,原因是 。
(2)海水制镁:海水晒盐后,以其母液(卤水)和贝壳(主要成分是CaCO3)为原料制镁,其工艺流程如下图所示:
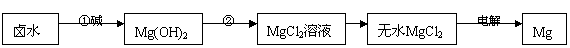

I.步骤①所加的碱应该是 (选填“氢氧化钠”或“石灰乳”),步骤②反应的化学方程式是 ;若要验证镁.铁.铜的活动性顺序,选择铁丝后,还要选择 . 两种溶液。
II.Mg(OH)2加热分解生成MgO和H2O,MgO是高熔点的化合物,某些阻燃剂(阻碍燃烧的物质)的有效成分是Mg(OH)2。你认为Mg(OH)2能够阻燃的原因可能是 (选填序号)
A.Mg(OH)2分解需要吸收大量的热,降低了可燃物的着火点
B.生成的氧化镁覆盖在可燃物表面,隔绝了空气
C.生成的水蒸气降低了可燃物周围氧气浓度
D.反应因吸热降低了环境温度,使可燃物不易达到着火点
通过下列实验操作和现象能得出相应结论的是( )
| 实验操作 | 现象 | 结论 | |
| A | 向收集满CO2的软塑料瓶中加入约1/3体积的NaCl溶液,旋紧瓶盖,振荡 | 塑料瓶变瘪 | CO2能与NaCl反应 |
| B | 50℃时,将17gKCl固体加入50g蒸馏水中,完全溶解后缓慢降温 | 降温至20℃时开始有晶体析出 | 20℃时,KCl的溶解度为17g |
| C | 将白磷浸没在热水中,再向热水中的白磷通氧气 | 通氧气前白磷不燃烧,通氧气后白磷燃烧 | 氧气是燃烧需要的条件之一 |
| D | 点燃从导管放出的某气体,在火焰上方罩一个冷而干燥的烧杯 | 烧杯内壁有无色液滴产生 | 该气体是CH4 |
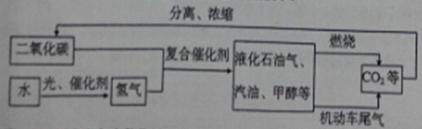
 甲醇均由碳、氢、氧三种元素组成
甲醇均由碳、氢、氧三种元素组成 4X↑+O2↑+2H2O,其中X的化学式为
4X↑+O2↑+2H2O,其中X的化学式为 
 (4)D图的装置可用来制取的气体是 (写—种),制取该气体的化学方程式为:
(4)D图的装置可用来制取的气体是 (写—种),制取该气体的化学方程式为: