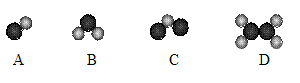为验证某混合气体中是否含有一氧化碳、二氧化碳 和水蒸气,同学设计了如下实验装置(装置

气密性良好),将混合气体依次通入。实验现象记录如下。(药品均足量且每步反应完全、夹持仪器省略)
| 装置 | 现象 |
| 甲 | 增重 |
| 乙 | 无明显现象 |
| 丙 | 粉末由 变红 |
| 丁 | 试液由紫变红,气球变大 |
甲 乙 丙 丁
Ⅰ.仪器a的名称 (21) 。
Ⅱ.丙中粉末由 (22) 变红,发生的化学反应方程式为 (23) ,其中氧化铜作
(24)  剂。
剂。
Ⅲ.根据上述现象,分析混合气体中一定含有水蒸气、一氧化碳,可能含有二氧化碳 。写出可能 含有二氧化碳的理由 (25) 。
含有二氧化碳的理由 (25) 。
Ⅳ.在不改变装置的前提下,只需将装置 (26) 中药品换成 (27) ,即可判断二氧化碳是否存在。
| |
 |

①该样品中碳酸钙的质量分数。(根据化学方程式列式计算)
(19)
②若取该样品10g,充分煅烧,最多可以产生CO2 (20) g。
硝酸钾的溶解度如下表所示,有关叙述正确的是
| 温度(℃) | 20 | 30 | 40 | 50 | 60 |
| 溶解度(g/100g水) | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
A.20℃时,可配成50g35%的硝酸钾饱和溶液
B.30℃和50℃时,等质量的硝酸钾饱和溶液,所含水的体积,前者大于后者
C.40℃时,50g硝酸钾饱和溶液降温至20℃,析出固体的质量为32.3g
D.60℃时,50g硝酸钾饱和溶液中,溶质与溶剂的质量比为11:21
 水是宝贵的自然资源,对于人类生活、工农业生产都具有重要意义。
水是宝贵的自然资源,对于人类生活、工农业生产都具有重要意义。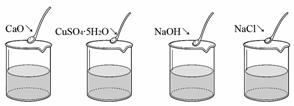 (12) 。(选填编号)
(12) 。(选填编号) 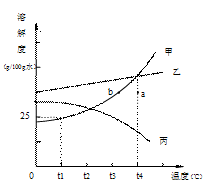 Ⅱ.先锋Ⅵ是一种抗生素,每瓶含先锋霉素0.5g。注射时,配成质量分数不高于20%的溶液,则加入的水至少需要 (13) mL。
Ⅱ.先锋Ⅵ是一种抗生素,每瓶含先锋霉素0.5g。注射时,配成质量分数不高于20%的溶液,则加入的水至少需要 (13) mL。 ③木炭具有还原性,可以冶炼金属。请在 内填入配平后的系数。
③木炭具有还原性,可以冶炼金属。请在 内填入配平后的系数。

 (8) Fe3O4+ C
(8) Fe3O4+ C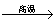 Fe+ CO2↑
Fe+ CO2↑


 1mol氮气和2mol氧气在一定条件下能生成2mol甲分子。若以“ ”表示氮原子、
1mol氮气和2mol氧气在一定条件下能生成2mol甲分子。若以“ ”表示氮原子、 “ ”表示氧原子,以下微粒图示中可以表示甲分子的是
“ ”表示氧原子,以下微粒图示中可以表示甲分子的是