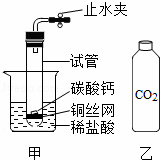
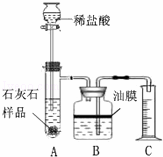
某科学兴趣小组同学为测定一种石灰石中碳酸钙的质量分数,组装了如图的实验装置进行实验.称取质量为1.2克的石灰石样品,将其与足量的稀盐酸反应,每隔10秒读出量筒中水的体积,得到的相关数据(见表格).请根据数据回答下列问题:
| 反应时间/s | 10 | 20 | 30 | 40 | 50 | 60 |
| 量筒中水的体积/ml | 70 | 125 | 170 | 205 | 220 | 220 |
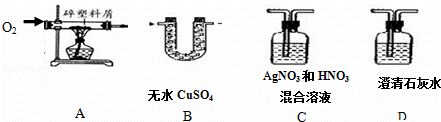
(1)实验装置B中油膜的作用是 .
(2)根据图中的数据,分析该反应速率如何变化并说明原因: .
(3)该样品中碳酸钙的质量分数是多少?(标准状况下二氧化碳的密度是2克/升,计算结果保留一位小数)
小明把过量锌粒加入有盐酸的试管中,发现随着反应的进行,产生气体的速度逐渐加快,一段时间后逐渐减慢,最后停止产生气体.在反应过程中,溶液的温度也先随之升高,最后下降到室温.于是,小明设计实验来探究“一定质量的某种金属和同体积盐酸反应快慢的影响因素”.测得实验数据如下:
某金属与同体积盐酸溶液反应实验数据表
| 盐酸溶液浓度 | 反应开始时酸 溶液的温度 | 反应开始到2分钟产生的气体体积 | 反应结束共产生气体体积 |
| 5% | 20℃ | 10mL | 60mL |
| 10% | 20℃ | 19mL | 118mL |
| 15% | 20℃ | 28mL | 175mL |
| 5% | 35℃ | 28mL | 60mL |
| 10% | 35℃ | 72mL | 118mL |
| 15% | 35℃ | 103mL | 175mL |
(1)分析实验数据得出:一定质量的某种金属和同体积盐酸反应,影响金属和酸反应快慢的主要因素有 、 .
(2)可以通过比较 实验数据来确定金属和酸反应的快慢.
(3)过量锌粒加入盐酸中,反应开始的一段时间,反应速率逐渐加快,而不是逐渐减慢.请分析原因. .
 醛和乙醇,消耗氧气的质量相等
醛和乙醇,消耗氧气的质量相等