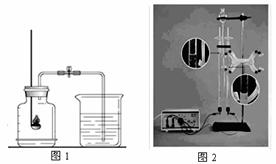
小 明发现一种淡黄色的粉末可以用于杀菌、消毒和漂白,于是想探究该固体的成分。
明发现一种淡黄色的粉末可以用于杀菌、消毒和漂白,于是想探究该固体的成分。
【提出问题】 该淡黄色固体的化学成分是什么?
【查阅资料】(1)硫单质是一种淡黄色固体,难溶于水,在空气中点燃硫单质,生成一种无色、有刺激性气味的气体。
(2)过氧化钠(Na2O2)是一种淡黄色固体,能与水反应,生成气体并放出大量的热。
【设计实验方案】
方案一:取少量该固体粉末于试管中,加2mL水,振荡并观察现象。
方案二:在燃 烧
烧 匙里放少量该固体,在酒精灯上加热,观察现象。
匙里放少量该固体,在酒精灯上加热,观察现象。
比较以上两方案,你认为的最佳方案是 ,理由是(从环保或操作角度分析) 。
【实验验证并得出结论】小明向盛有少量该固体的试管中加入2mL水,立刻观察到有无色气泡产生,并且验证出该反应同时生成了氢氧化钠(NaOH)。通过实验验证,确定该淡黄色粉末为过氧化钠。
小明想对生成的气体成分判断,他提出了以下两种假设:①该气体是CO ②该气体是O2
你认为上述假设哪个更合理 (填“①”或“②”)。理由是是 。
请设计一个实验,验证你的合理假设(写出简要操作步骤、实验现象和结论 )。
)。
| 操作步骤 | 实验现象 | 结论 |
|
|
|
|
【分析】 过氧化 钠与水反应的化学方程式为 。
钠与水反应的化学方程式为 。
【计算】 78克过氧化钠与多少克二氧化碳中所含氧元素的质量相等?
(列式计算)
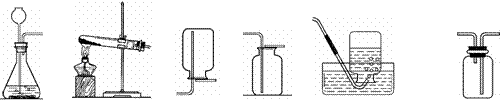
现有下列实验装置图,结合该图回答下列问题。
|
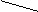
| ||||||
| ||||||
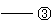 | ||||||
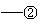 |
A B C D E  F
F
(1)写出图中标号仪器的名称:③ 。
(2)实验室采用分解过氧化氢溶液的方 法来制取氧气,可以选用的发生装置为 (填装置序号),发生反应的化学方程式为 ,若用F装置通过排水法来收集氧气,F装置的处理 。
法来制取氧气,可以选用的发生装置为 (填装置序号),发生反应的化学方程式为 ,若用F装置通过排水法来收集氧气,F装置的处理 。
(3)若用加热高锰酸钾的方法制取氧气,则可选用的装置组合为 ,在固定试管时,试管口必须 ,这是为了 。
(4)通过查阅资料得知:①氨气(NH3) 是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,其水溶液称为氨水;②氨水能使无色酚酞试液变红;③实验室用氯化铵(NH4Cl)和熟石灰两种固体反应物混合加热可制取氨气,同时生成氯化钙和水。则实验室制取氨气的装置组合可以选用 。小芳将收满氨气的集气瓶倒扣在滴有无色酚酞的水中,观察到的现象是__________________、________ _____。
是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,其水溶液称为氨水;②氨水能使无色酚酞试液变红;③实验室用氯化铵(NH4Cl)和熟石灰两种固体反应物混合加热可制取氨气,同时生成氯化钙和水。则实验室制取氨气的装置组合可以选用 。小芳将收满氨气的集气瓶倒扣在滴有无色酚酞的水中,观察到的现象是__________________、________ _____。
一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如下表所示下列叙述正确的是 ( )
| 物质 | A | B | C | D |
| 第一次测得的质量/g | 50 | 4 | 4.6 | 1 |
| 第二次测得的质量/g | 待测 | 20 | 23 | 4.2 |
A.上述反应属于化合反应 B.该反应B与C的质量变化之比为20:23
C.第二次测得A的质量为12.4g D.该反应中共生成D的质量为4.2g
下列由事实得出的结论正确的是 ( )
| 编号 | 事实 | 结论 |
| A. | 过滤后滤液依然浑浊 | 滤纸肯定破损了 |
| B. | 某物质只由一种元素组成 | 该物质不一定是单质 |
| C. | 给固体加热时试管破裂 | 试管口肯定没有略向下倾斜 |
| D. | 某物质完全燃烧,生成物只有CO2和H2O | 该物质一定由C、H、O三种元素组成 |
 )的反应过程,获得当年的诺贝尔化学奖。
)的反应过程,获得当年的诺贝尔化学奖。
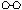
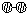
 N2和H2合成氨的
N2和H2合成氨的 反应过程可用下图表示(用 、 、 、 分别表示N2、H2、NH3 、在催化剂表面 )
反应过程可用下图表示(用 、 、 、 分别表示N2、H2、NH3 、在催化剂表面 )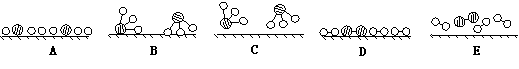
 (1)图中表示的合成氨反应过程的顺序为:E→( )→( )→( )→C(在括号中填写其它三张图示的字母);
(1)图中表示的合成氨反应过程的顺序为:E→( )→( )→( )→C(在括号中填写其它三张图示的字母); 嘴口检验反应产生的气体,其中负极端的玻璃管内产生气体的检验现象是 。
嘴口检验反应产生的气体,其中负极端的玻璃管内产生气体的检验现象是 。