小可同学为测 定某铁合金的含铁量,做了如下实验,称取11.4克样品,放入质量为50.0克的烧杯中,再往烧杯中加入100.0克的稀盐酸(杂质不与酸反应、不溶于水)并对烧杯进行了四次称量,记录数据如下:
定某铁合金的含铁量,做了如下实验,称取11.4克样品,放入质量为50.0克的烧杯中,再往烧杯中加入100.0克的稀盐酸(杂质不与酸反应、不溶于水)并对烧杯进行了四次称量,记录数据如下:
| 反应时间 | t1 | t2 | t3 | t4 |
| 烧杯总质量/克 | 161.4 | 161.2 | 161.0 | 161.0 |
求:(1)反应产生的氢气的质量
(2)该铁合金中铁的质量分数(保留一位小数)
已知一种固体化合物由C、H、O、Cu四种元素组成。向盛有该化合物的试管中加入稀盐酸,产生大量气泡,固体逐渐溶解,得到蓝绿色溶液。己知这种蓝绿色是氯化铜溶液。(1)探究产生的气体是什么。
【猜想】①可能是氢气;② ③ ……
【实验】请针对你②和③猜想中的一种,设计实验,验证你的猜想。
 。
。
(2) 从蓝绿色溶液中提取金属铜。现利用该溶液制取金属铜,过程如下:
 |
操作1的名称为 ,完成该实验需要的玻璃仪器有
加入过量的A的目的是 ,反应化学方程式为 。
②加入足量B的目的是 ,

 _(填“A”“B”或“C”),反应的化学方程式是__________________________________________。
_(填“A”“B”或“C”),反应的化学方程式是__________________________________________。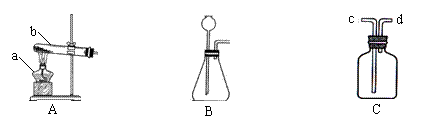 ③若B装置中装有石灰石和稀盐酸,则该装置可用于制取____________气体。如果用C装置收集
③若B装置中装有石灰石和稀盐酸,则该装置可用于制取____________气体。如果用C装置收集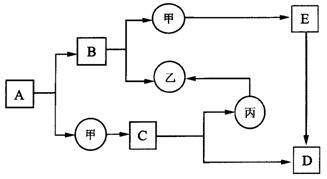
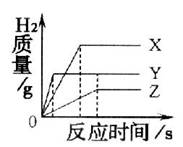 把相同体积、相同质量分数的稀盐酸,分别滴到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中,生成H2的质量与反应时间的关系如右图所示。这三种金属的活动性顺序为 ;假如X、Y、Z都是+2价金属,则相对原子质量由大到小的顺序为 。
把相同体积、相同质量分数的稀盐酸,分别滴到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中,生成H2的质量与反应时间的关系如右图所示。这三种金属的活动性顺序为 ;假如X、Y、Z都是+2价金属,则相对原子质量由大到小的顺序为 。