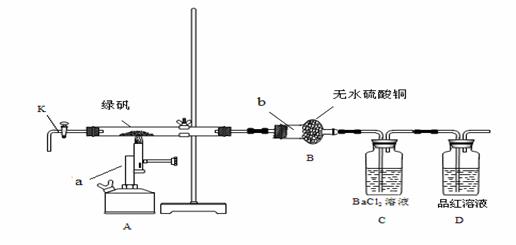
已知FeCl3与CuCl2对H2O2分解都有催化作用,为测定并比较二者的催化效率,需要控制的条件包括:①实验温度;②H2O2的浓度;③催化剂质量;④FeCl3与CuCl2的颗粒大小( )
|
| A. | ①② | B. | ②③ | C. | 全部 | D. | ①②④ |
某溶液溶质的质量分数为20%,加入50g水后变为10%,稀释后溶液中溶质的质量是( )
|
| A. | 50g | B. | 10g | C. | 100g | D. | 40g |
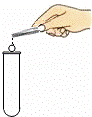
下列实验操作符合规范的是( )
|
| A. |
检验装置气密性 | B. |
给液体加热 | C. |
向试管中加固体 | D. |
取用固体药品 |
下列过程中,属于化学变化的是( )
|
| A. |
| B. | 火药爆炸 | C. | 水的蒸馏 | D. | 酒精溶于水 |
微粒是构成化学物质的基础,下列对微粒的描述正确的是( )
|
| A. | 仅有碳原子构成的物质属于纯净物 |
|
| B. | 原子中一定含有质子、中子、电子 |
|
| C. | NaCl是由离子构成的,所以HCl也是有离子构成的 |
|
| D. | Cl﹣的离子结构示意图为 |
化学物质正逐渐改变我们的生活,下列有关说法不正确的是( )
|
| A. | 为保障食品安全,应杜绝使用食品添加剂 |
|
| B. | 臭氧层可以保护地球生物免受过量紫外线伤害,但近地面过量的臭氧则对人体有害 |
|
| C. | 石油分馏出的成分可以可以用来制造合成纤维、合成橡胶、塑料等 |
|
| D. | 为了可持续发展,我们不仅要善用 |
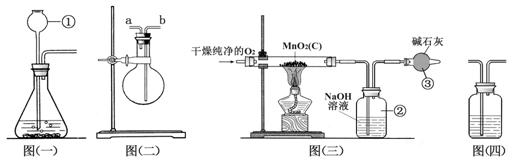
某二氧化锰样品中含有杂质炭,为测定该样品中二氧化锰的质量分数,某兴趣小组设计了如下实验方案:在一定量的样品中通入干燥纯净的氧气,使杂质炭在加热条件下反应生成CO2来进行分析测定。
|
(1)仪器①的名称是 。如果该实验选择图(一)装置来制取氧气,则所反应的化学方程式为 。
(2)用图(二)装置可用于干燥氧气,应在烧瓶中装入 (填试剂名称)进行干燥气体,气体应从 (“a”或“b”)端通入。
(3)图(三)是用干燥纯净的O2与样品反应来测定二氧化锰质量分数的装置,装置③中装有 碱石灰,其作用是_________________________________。
(4)为验证图(三)中装置②已将CO2吸收完全,可在装置②与③之间加入图(四)装置进行证明,则图(四)装置中加入的试剂为__________(填字母)。
A. NaOH溶液 B. 澄清石灰水 C. 浓硫酸
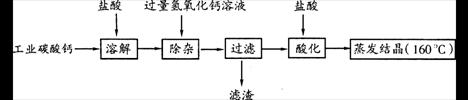
味精是常用的调味品,它的鲜味来自于其中的主要成分“谷氨酸钠”(化学式是C5H8NO4Na,易溶于水,与AgNO3不反应),另外还含有NaCl(其他成分不考虑)。请回答下列问题:
(1)称取5.0g味精配制成50g溶液,量取蒸馏水的量筒规格是 。(填字母)
A.10mL B.50mL C.100mL
(2)下图是配制过程,正确的操作顺序为 。(填序号)
 |
(3)为测定味精中NaCl的质量分数,进行如下实验:
①向所配制的50g溶液中加入过量的 溶液(填化学式)充分反应。
②然后进行 (填操作名称)、洗涤、干燥后称量AgCl固体。
③在其他操作均正确的情况下,若在配制溶液过程中,仰视刻度量取蒸馏水,则所配制溶液的谷氨酸钠质量分数 (填“偏大”、“偏小”或“无影响”),则测得的样品中氯化钠的质量分数 (填“偏大”、“偏小”或“无影响”)。
④经精确测定AgCl沉淀的质量为2.87g,则该味精中NaCl的质量分数为 。(计算结果保留一位小数)

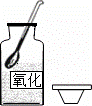
 碘升华
碘升华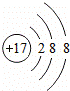
 金属材料和制品,更要有计划地开采金属资源
金属材料和制品,更要有计划地开采金属资源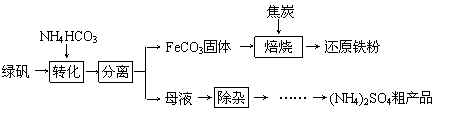

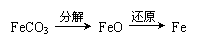
 ,实际作还原剂的是CO。写出“焙烧”过程中各步反应的化学方程式:
,实际作还原剂的是CO。写出“焙烧”过程中各步反应的化学方程式: ;
;