某实验小组利用废硫酸制备K2SO4并研究CaSO4·2H2O加热分解的产物。
一、K2SO4的制备
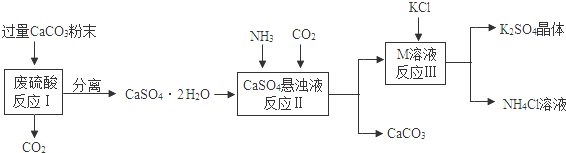
(1)将CaCO3研成粉末的目的是____________ _。
(2)上述流程中可循环使用的物质有CO2和__________(填写化学式)。
(3)反应III中相关物质的溶解度如下表。你认为反应III在常温下能实现的原因是________
____________。
| 物质 | KCl | K2SO4 | NH4Cl | M |
| 溶解度/g(常温) | 34.0 | 11.1 | 37.2 | 19.5 |
(4)不用水而用饱和K2SO4溶液洗涤反应III所得晶体的目的是_____________________。
二、研究CaSO4·2H2O加热分解的产物
(5)分离所得的CaSO4·2H2O含有CaCO3,可用盐酸除去,该化学反应方程式为
________________________。
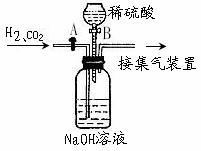
(6)为了测定CaSO4·2H2O和CaCO3的质量比x∶y,实验小组利用下图所示的装置(夹持仪器省略)进行实验。
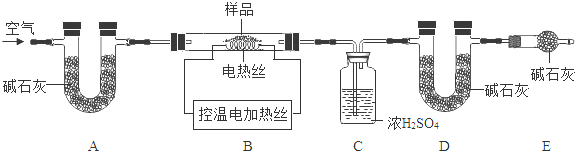
①实验前首先要________________,再装入样品。装置A的作用是_____________________。
②已知CaSO4·2H2O在160℃生成CaSO4,1350℃时CaSO4开始分解;CaCO3在900℃时分
解完全。现控制B装置900℃进行实验采集了如下数据:
a.反应前玻璃管与样品的总质量m1g b.反应后玻璃管中固体的质量m2g
c.装置C实验后增重m3g d.装置D实验后增重m4g
某同学选用b、d或c、d数据组合求出的值x∶y,若无装置E,则实验测定结果将________(填“偏大”“偏小”或“无影响”)。若实验测得m3=1.8g, m4=2.2g,求x∶y的值(写出计算过程)。(已知CaSO4·2H2O的相对分子质量是172)
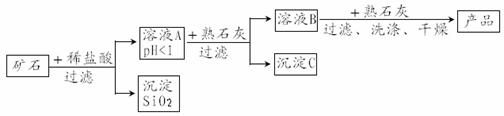 某矿石由MgO、Fe2O3、CuO、SiO2组成,用它制备氢氧化镁的流程示意图如图所示:
某矿石由MgO、Fe2O3、CuO、SiO2组成,用它制备氢氧化镁的流程示意图如图所示:
(1) 溶液A中共含有_____种阳离子。
(2) 在溶液A中加入熟石灰调节溶液的pH,可以使溶液中的金属阳离子转化为沉淀。该实验条件下,使金属阳离子沉淀的相关pH数据见下表。为保证产品纯度、减少产品损失,并便于操作,溶液B的pH可容许的范围为_________。
| 氢氧化物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 4.2 | 8.6 |
| 完全沉淀的pH | 3.2 | 6.7 | 11.1 |
(3)溶液B中一定含有的溶质为___________________。
(4)写出溶液B中加入熟石灰,生成产品的化学方程式:_________________。
(1)下图是某保健品标签的部分内容,请仔细阅读后回答下列问题:
| ××××(品牌名称) 帮助防治骨质疏松症 【每片主要成分】 碳酸钙1.5g 维生素D3200国际单位 (维生素D3能参与钙和磷代谢,促进其 吸收并对骨质形成有重要作用) 镁、锌、锰等矿物质 |
该保健品的功能是__________;其主要成分中,提供钙元素的物质是____________;参与钙的代谢,促进其吸收的物质是____________;矿物质中的锌元素属于人体必须的________(填“常量”或“微量”)元素。
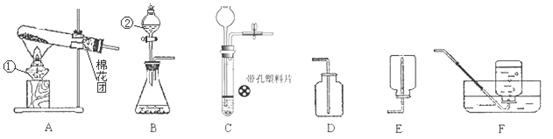
(2)实验室可用氯酸钾或过氧化氢制取氧气。
 ①过氧化氢分解的变化可以如此表示:过氧化氢 二氧化锰 水+氧气
①过氧化氢分解的变化可以如此表示:过氧化氢 二氧化锰 水+氧气
上述变化所涉及的物质中,属于金属氧化物的是___________,氧元素的化合价为-1价的是___________________。
②用氯酸钾或过氧化氢制取氧气的实验中,都需要加入少量二氧化锰,二氧化锰的作用是__________;若未加入二氧化锰,则反应生成的氧气的量__________(填“减少”或“不变”)。
下列鉴别两种不同物质的方法,不正确的是 ( )
| 序号 | 待鉴别的物质 | 鉴别方法 |
| A | CO2与O2 | 燃着的木条,观察燃烧情况 |
| B | 酒精与白醋 | 闻气味 |
| C | BaCO3与NaCl | 加水,观察是否溶解 |
| D | NaOH与Na2CO3 | 滴加酚酞溶液,观察溶液颜色的变化 |
 母编号)。
母编号)。
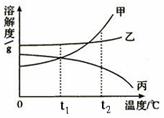 A.三种物质溶解度大小依次为:乙>丙>甲
A.三种物质溶解度大小依次为:乙>丙>甲