碳酸钠和碳酸氢钠是生活中常见的盐,通过实验验证、探究它们的化学性质。
【查阅资料】
①  Na2CO3 + CaCO3 = CaCO3↓+ 2NaCl
Na2CO3 + CaCO3 = CaCO3↓+ 2NaCl
② 2NaHCO3 Na2CO3 +CO2↑+ H2O
③ Ca(HCO3 )2 易溶于水。
④ CaCl2 溶液分别与 NaHCO3、Na2CO3 溶液等体积混合现象(表中的百分数为溶液中
溶质的质量分数):
| NaHCO3 | Na 2CO3 | ||||
| 0.1% | 1% | 5% | 0.1% | ||
| CaCl2 | 0.1% | 无明显现象 | 有浑浊 | 有浑浊 | 有浑浊 |
| 1% | 无明显现象 | 有浑浊 | 有浑浊,有微小气泡 | 有沉淀 | |
| 5% | 无明显现象 | 有浑浊 | 有浑浊,有大量气泡 | 有沉淀 |
 【进行实验】
【进行实验】
| 序号 | 实验装置 | 主要实验步骤 | 实验现象 |
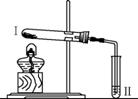
| 实验 1 | 向 2 支试管中分别加入少 量Na 2CO3 和NaHCO3 溶液,再分别滴加盐酸 | 2 支试管中均有气泡产生 | |
| 实验 2 |
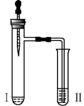
| 向Ⅱ中加入试剂 a,向Ⅰ中 加入少量Na 2CO3 或 NaHCO3 固体,分别加热一 段时间 | Na 2CO3 受热时Ⅱ中无明 显现象 NaHCO3 受热时Ⅱ中出现 浑浊 |
| 实验 3 |
| 向Ⅱ中加入试剂 a,向Ⅰ中 加入少量 5%的 NaHCO3 溶 液,再滴加 5%的 CaCl2 溶 液 | Ⅰ中出现浑浊,有气泡产 生Ⅱ中出现浑浊 |
【解释与结论】
(1)实验 1 中, NaHCO3 与盐酸反应的化学方程式为 。
(2)实验 2 中,试剂 a 为 。
(3)实验 3 中, NaHCO3 与 CaCl2 反应的化学方程式为:

 2NaHCO3 + CaCl2
2NaHCO3 + CaCl2
【反思与评价】
+ + H2 O 。
(1)实验 2 中,加热 NaHCO3 后,试管Ⅰ中残留固体成分可能为 (写出所有可能)。
(2)资料④中,NaHCO3 溶液与 CaCl2 溶液混合的现象中,有些只观察到浑浊、未观察
到气泡,原因可能是 。
(3)用 2 种不同的方法鉴别 Na 2CO3 和 NaHCO3 固体,实验方案分别为:
① 。
② 。

|
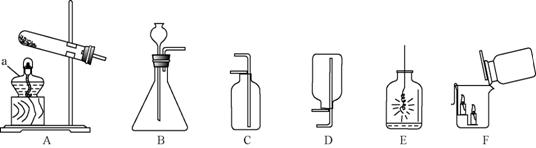
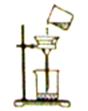
| 内容 步骤 | 【实验 1】研究燃烧条件 | 【实验 2】研究氧气性质 |
| Ⅰ | 烧杯中盛有 80℃的热水, 分别在燃烧匙和烧杯中导 管口放置一小块白磷,塞 紧瓶塞 | 烧杯中盛有 NaOH 溶液, 燃烧匙中放入木炭 点燃木炭后,迅速将燃烧 匙伸入瓶中,塞紧瓶塞 |
| Ⅱ | 推入适量 H2 O2 溶液 | 推入适量 H2 O2 溶液 |
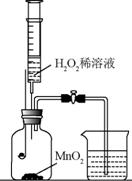
(1) H2 O2 稀溶液与 MnO2 接触时发生反应的化学方程式为 。
(2)实验 1 中,推入H2O2 溶液前,燃烧匙和水中的白磷均不燃烧,原因分别是 ; 推入 H2O2溶液后,观察到烧杯中的现象是 。
(3)实验 2 中,推入 H2 O2 溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质 是 ;木炭熄灭后冷却一段时间,烧杯中的部分溶液流入集气瓶。该实验中,集气瓶内压强的变化过程是
。



 建设如火如茶,许多村庄道路两侧安装了太阳能路灯。关于太阳能路灯所用材料的叙述不正确的是
建设如火如茶,许多村庄道路两侧安装了太阳能路灯。关于太阳能路灯所用材料的叙述不正确的是 4NaHSO3 + 3S↓。
4NaHSO3 + 3S↓。 ? 收氢气的质量。
? 收氢气的质量。