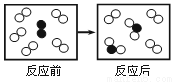
(8分)某实验小组的同学在整理实验仪器时,发现了一个盛有黑色固体的烧杯。在请教老师后,同学们得知烧杯中的固体是加热制取氧气的剩余物(反应完全),从中可以回收得到MnO2。小组同学将黑色固体取出,并对其进行了探究。
【查阅资料】
①实验室中可以加热二氧化锰和氯酸钾(KClO3)固体的混合物制取氧气,同时生成氯化钾。
②氯化钾溶于水,其水溶液呈无色;锰酸钾溶于水,其水溶液呈绿色。
Ⅰ.探究黑色固体是哪个化学反应的剩余物。
【猜想】猜想一:H2O2制取氧气;猜想二:KClO3制取氧气;猜想三: 。
根据所学知识判断,猜想一不成立,理由是_________________。
【进行实验】
取少量黑色固体于另一个烧杯中,加入足量蒸馏水溶解,振荡,过滤后得到黑色滤渣和无色滤液。
【得出结论】猜想 成立,理由是 。
Ⅱ.探究二氧化锰在氯酸钾固体加热制取氧气反应中的作用。
【猜想】猜想一:是反应物; 猜想二:是催化剂。
【进行实验】
实验操作 | 实验现象 |
1、取12.25g氯酸钾在试管中加热,把带火星的木条伸入试管。 | 固体融化,产生少量气体,木条上的火星变亮。 |
2、取12.25g氯酸钾和2.55g二氧化锰混合均匀后在试管中加热,把带火星的木条伸入试管。 | _______________。 |
3、待反应完全后,将试管中的剩余物加足量的水溶解,过滤,并将全部滤渣洗涤、干燥、称量。 | 称量固体的质量是_____g |
【实验结论】猜想二成立,二氧化锰在氯酸钾固体加热制取氧气的反应中起到催化作用。
【反思与交流】
小贝同学提出,前面的实验不足以证明二氧化锰在这个反应中起到了催化作用,因为①。
经过讨论,大家设计了一个补充实验,证明了猜想二成立,请你写出实验操作②。
(3分)某校化学实验课上,同学们用化学方法探究一种钢样品中铁的含量。同学们将11.4 g钢样品和30.0 g稀盐酸(足量)放入质量为130.0 g烧杯中。在化学反应过程中对烧杯及其中的剩余物进行了四次称量,记录如下表:
反应时间 | T0 | T1 | T2 | T3 |
烧杯和药品质量/ g | 171.4 | 171.3 | 171.0 |
|
(1)计算这种钢样品中铁的质量分数。(最后结果精确到0.1%)
(2)某钢厂欲冶炼1120 t这种钢材,需含氧化铁80%的赤铁矿多少吨?
 171.0
171.0