0 129940 129948 129954 129958 129964 129966 129970 129976 129978 129984 129990 129994 129996 130000 130006 130008 130014 130018 130020 130024 130026 130030 130032 130034 130035 130036 130038 130039 130040 130042 130044 130048 130050 130054 130056 130060 130066 130068 130074 130078 130080 130084 130090 130096 130098 130104 130108 130110 130116 130120 130126 130134 211419

 用化学符号和数字填空:
用化学符号和数字填空: 同学们依据物质类别和物质中某种元素的化合价构建了初中化学常见物质间的转化关系坐标图(图中“→”表示物质间的转化).
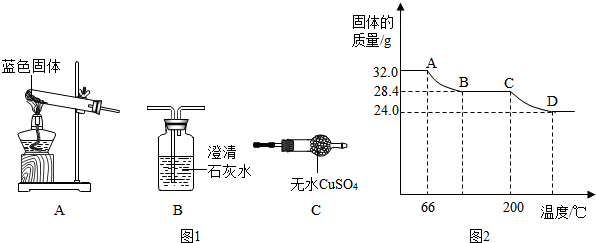
同学们依据物质类别和物质中某种元素的化合价构建了初中化学常见物质间的转化关系坐标图(图中“→”表示物质间的转化). 甲、乙、丙、丁为初中化学常见物质.由H、C、O、Cl、Na、Ca、Fe七种元素中的一种或几种组成.用如图所示装置进行实验.
甲、乙、丙、丁为初中化学常见物质.由H、C、O、Cl、Na、Ca、Fe七种元素中的一种或几种组成.用如图所示装置进行实验.