0 128915 128923 128929 128933 128939 128941 128945 128951 128953 128959 128965 128969 128971 128975 128981 128983 128989 128993 128995 128999 129001 129005 129007 129009 129010 129011 129013 129014 129015 129017 129019 129023 129025 129029 129031 129035 129041 129043 129049 129053 129055 129059 129065 129071 129073 129079 129083 129085 129091 129095 129101 129109 211419
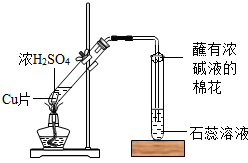 某校化学兴趣小组的同学在探究金属的化学性质时,发现铜与稀硫酸在常温或加热的条件下均不反应.那么,铜与浓硫酸能否发生反应呢?他们设计了如图所示装置进行探究.
某校化学兴趣小组的同学在探究金属的化学性质时,发现铜与稀硫酸在常温或加热的条件下均不反应.那么,铜与浓硫酸能否发生反应呢?他们设计了如图所示装置进行探究. 化学就在我们身边.请运用所学的化学知识,回答下列问题:
化学就在我们身边.请运用所学的化学知识,回答下列问题: