0 126983 126991 126997 127001 127007 127009 127013 127019 127021 127027 127033 127037 127039 127043 127049 127051 127057 127061 127063 127067 127069 127073 127075 127077 127078 127079 127081 127082 127083 127085 127087 127091 127093 127097 127099 127103 127109 127111 127117 127121 127123 127127 127133 127139 127141 127147 127151 127153 127159 127163 127169 127177 211419
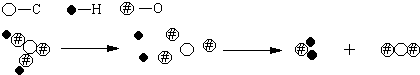
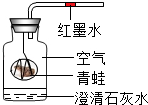 现有含碳物质:①金刚石、②石墨、③CO、④CO2、⑤Na2CO3,已见报道的还有:⑥C60、⑦C3O2、⑧C4O3、⑨C5O2、⑩C12O9等.其中属于碳的单质有(填序号)
现有含碳物质:①金刚石、②石墨、③CO、④CO2、⑤Na2CO3,已见报道的还有:⑥C60、⑦C3O2、⑧C4O3、⑨C5O2、⑩C12O9等.其中属于碳的单质有(填序号)